Fosforoxide (V) structuur, eigenschappen, verkrijgen, gebruik, risico's

- 1851
- 213
- Cecil Graham
Hij Fosforoxide (V) Het is een anorganische vaste stof gevormd door fosfor (P) en zuurstof (O). Zijn empirische formule is p2OF5, terwijl de juiste moleculaire formule P is4OF10. Het is een zeer hygroscopische witte vaste stof, dat wil zeggen dat het heel gemakkelijk lucht uit de lucht kan absorberen, onmiddellijk reageert. De reactie kan gevaarlijk zijn omdat deze een snelle temperatuurstijging veroorzaakt.
De hoge neiging om water te absorberen heeft ervoor gezorgd dat het wordt gebruikt als droogmiddel in chemische laboratoria, en sommige verbindingen uitdrogen, dat wil zeggen water uit zijn moleculen elimineren.
 Fosforoxide (v) poeder, p4OF10. Lhchem [cc by-s (https: // creativeCommons.Org/licenties/by-sa/3.0)]. Bron: Wikimedia Commons.
Fosforoxide (v) poeder, p4OF10. Lhchem [cc by-s (https: // creativeCommons.Org/licenties/by-sa/3.0)]. Bron: Wikimedia Commons. Fosforoxide (V) wordt ook gebruikt om de bindingsreacties van moleculen van verschillende koolwaterstoffen te versnellen, een reactie genaamd condensatie. Bovendien maakt het mogelijk bepaalde organische zuren om te zetten in esters.
Het is bijvoorbeeld gebruikt om benzine te verfijnen om fosforzuur H te bereiden3Po4, Om verbindingen te verkrijgen die dienen om brand uit te stellen, om glas te produceren voor vacuümtoepassingen, naast vele andere toepassingen.
Fosforoxide (V) moet in goed gesloten containers worden bewaard om contact met het vocht uit de lucht te voorkomen. Het is corrosief en kan ogen, huid en slijm schaden.
[TOC]
Structuur
Fosforoxide (V) wordt gevormd door fosfor (P) en zuurstof (O), waarbij fosfor valentie heeft van +5 en zuurstof -2. Het fosforoxidemolecuul (V) heeft vier fosfor- en tien zuurstofatomen en daarom is de juiste moleculaire formule P is p is p4OF10.
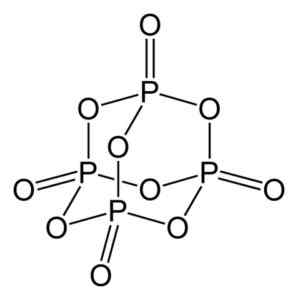 Structuur van het fosforoxidemolecuul (V), P4OF10. Auteur: Benjah-BMM27. Bron: Wikimedia Commons.
Structuur van het fosforoxidemolecuul (V), P4OF10. Auteur: Benjah-BMM27. Bron: Wikimedia Commons. Bestaat in drie kristallijne vormen, zoals amorf stof en in een glasachtige vorm (zoals glas). In de zeshoekige kristallijne vorm wordt elk van de fosforatomen gevonden in de hoekpunten van een tetraëder.
Nomenclatuur
- Fosforoxide (V)
- Fosfor pentoxide
- Difosfack pentoxide
Kan u van dienst zijn: oplosmiddel: concept, typen en voorbeelden- Fosfor pentoxide
- Fosforanhydride
- Tetrafosfor -verval
Eigenschappen
Fysieke staat
Kristallijne witte vaste stof. De meest voorkomende vorm is die van zeshoekige kristallen.
Molecuulgewicht
283.89 g/mol
Smeltpunt
562 ºC
Sublimatietemperatuur
360 ºC tot 1 drukatmosfeer. Het betekent dat bij deze temperatuur van de gasklasse gaat zonder door de vloeibare toestand te gaan.
Dikte
2.30 g/cm3
Oplosbaarheid
Zeer oplosbaar in water. Zwavelzuur oplosbaar. Onoplosbaar in aceton en ammoniak.
Chemische eigenschappen
Fosforoxide (V) absorbeert en reageert met lucht uit de lucht met extreem snel vormende fosforzuur H3Po4. Deze reactie is exotherme, wat betekent dat warmte wordt geproduceerd tijdens hetzelfde.
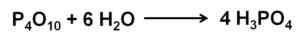 Fosfor (V) oxidereactie met water om fosforzuur H te vormen3Po4. Auteur: Marilú Stea.
Fosfor (V) oxidereactie met water om fosforzuur H te vormen3Po4. Auteur: Marilú Stea. De reactie van P4OF10 Met water leidt tot de vorming van een mengsel van fosforzuren waarvan de samenstelling afhankelijk is van de hoeveelheid water en omstandigheden.
De reactie met alcoholen leidt tot de vorming van fosforzuur of polymerezuuresters, afhankelijk van experimentele omstandigheden.
P4OF10 + 6 ROH → 2 (ro)2Po.OH + 2 RO.Po (oh)2
Met basisoxiden vormen vaste fosfaten.
Het is corrosief. Het kan gevaarlijk reageren met mierenzuur en anorganische basen zoals natriumhydroxide (NaOH), calciumoxide (CaO) of natriumcarbonaat NA2CO3.
Als een HCLO perclorinezuuroplossing wordt gegoten4 en CHCL -chloroform3 In fosforoxide (v) p4OF10 Er treedt een gewelddadige explosie op.
Andere eigenschappen
Het is niet ontvlambaar. Wist niet de verbranding. De waterreactie is echter zo gewelddadig en exotherme dat er een brandrisico kan zijn.
Het verkrijgen van
Het kan worden bereid door directe fosforoxidatie in een droge luchtstroom. Fosfor wanneer zuurstofteconair contact wordt geoxideerd en fosforoxide vormt (V).
P4 + 5 o2 → P4OF10
Aanwezigheid in de natuur
Fosforoxide (V) wordt gevonden in mineralen zoals ilmeniet, rutilo en zircón.
Kan u van dienst zijn: wat zijn anorganische chemische functies?Het ilmeniet is een mineraal dat ijzer en titanium bevat en soms fosfor (v) oxide heeft in concentraties die variëren tussen 0,04 en 0,33% per gewicht. Rutilo is een titaniumoxide -mineraal en kan ongeveer 0,02% bevatten door gewicht van P2OF5.
Zircón-zand (een zirkoniumelement mineraal) hebben fosfor (V) oxide bij 0,05-0,39% door gewicht.
Toepassingen
Als een uitdroging en secantagent
Vanwege de grote aviditeit voor water is het een van de bekendste en zeer effectieve uitdrogingsmiddelen bij temperaturen kleiner dan 100 ° C.
Kan water extraheren uit stoffen die worden beschouwd als uitdrogingsmiddelen. U kunt bijvoorbeeld water verwijderen uit zwavelzuur H2SW4 het zo maken3 en salpeterzuur hno3 verandert in n2OF5.
 Zwavelzuur uitdroging als gevolg van fosforoxide (V). Auteur: Marilú Stea.
Zwavelzuur uitdroging als gevolg van fosforoxide (V). Auteur: Marilú Stea. In principe kan het al die vloeistoffen en gassen drogen waarmee het niet reageert, dus het maakt het mogelijk om sporen van vocht uit vacuümsystemen te verwijderen.
In organische chemiereacties
Fosforoxide (V) dient om organische samengestelde ringen en andere condensatiereacties te sluiten.
Het maakt het mogelijk om organische zuren te sterifen met de mogelijkheid om onderscheid te maken tussen primaire alifatische carbonzuren (koolzuurhoudende keten zonder ringen met de -coo -groep aan één uiteinde) en aromatische zuren (groep -COH gekoppeld aan de benzeenring), omdat de laatste niet reageert.
Het dient ook om een H -molecuul te elimineren2Of van de amidas r (c = o) nh2 En het maakt ze nitriles r-cn. Bovendien, katalyseren of versnellen oxygenatie, dehydrogenering en polymerisatie van bitumenreacties.
 De P4OF10 Het wordt veel gebruikt in laboratoria voor organische chemie. Auteur: JDN2001CN0. Bron: Pixabay.
De P4OF10 Het wordt veel gebruikt in laboratoria voor organische chemie. Auteur: JDN2001CN0. Bron: Pixabay. Bij het raffineren van brandstof
Sinds de jaren dertig van de twintigste eeuw gaven bepaalde studies aan dat fosfor (V) oxide een werkingsactie van gasrefinitatie uitoefende, waardoor het octaan werd verhoogd.
De raffinageactie van P4OF10 Het is voornamelijk te wijten aan condensatiereacties (vereniging van verschillende moleculen) en niet van polymerisatie (binding van gelijke moleculen).
Kan u dienen: natriumacetaat: structuur, eigenschappen, synthese, gebruikDe P4OF10 Versnelt directe alomatische koolwaterstoffen met olefine -koolwaterstoffen, olefineconversie in naftens en gedeeltelijke polymerisatie. De alkylatiereactie verhoogt het octaanaantal benzine.
Op deze manier wordt een verfijnde benzine van hoge kwaliteit verkregen.
 Sommige oliederivaten kunnen worden verbeterd door de werking van P4OF10 In zijn moleculen. Auteur: DRPEPERSCOTT230. Bron: Pixabay.
Sommige oliederivaten kunnen worden verbeterd door de werking van P4OF10 In zijn moleculen. Auteur: DRPEPERSCOTT230. Bron: Pixabay. In verschillende toepassingen
Fosforoxide (V) dient:
- Bereid fosforzuur H voor3Po4
- Verkrijg acrylaat- en oppervlakteactieve esters
- Bereid fosfaatesters voor die worden gebruikt als vlamvertragers, oplosmiddelen en verdunningsmiddelen
- Fosfor trichloride -conversie naar fosfor oxychloride
- Laboratoriumreagens
- Fabrikant speciale bril voor vacuümbuizen
- Verhoog het smeltpunt van het asfalt
- Dienen als een standaardmolecuul bij de bepaling van fosfor of fosfaten in fosfatisch gesteente, meststoffen en Portland -cement, in de vorm van P2OF5
- Verbeter de verbanden tussen bepaalde polymeren en de ivoorlaag die de tanden bezitten
 Sommige speciale brillen zoals vacuümbuizen moeten P gebruiken4OF10 Tijdens de productie. Tvezymer [Public Domain]. Bron: Wikimedia Commons.
Sommige speciale brillen zoals vacuümbuizen moeten P gebruiken4OF10 Tijdens de productie. Tvezymer [Public Domain]. Bron: Wikimedia Commons. Risico's
Fosforoxide (V) moet worden gehandhaafd in afgesloten containers en op verse, droge en goed geventileerde plaatsen.
Dit dient om te voorkomen dat het geen contact opneemt met water, omdat het er gewelddadig op kan reageren, waardoor zeer warmte wordt gegenereerd, tot het punt van het verbranden van de nabijgelegen materialen die brandbaar zijn.
Fosforoxide (V) stof is irriterend oog en luchtwegen en corrosief voor de huid. Het kan brandwonden in de ogen produceren. Door inname te veroorzaken.
Referenties
- OF.S. Nationale bibliotheek van geneeskunde. (2019). Fosforanhydride. Hersteld van PubChem.NCBI.NLM.NIH.Gov.
- Nayler, p. (2001). Bitumens: gemodificeerd. Chemische aanpassing. In Encyclopedia of Materials: Science and Technology. Hersteld van Scientedirect.com.
- MALISHEV, B.W. (1936). Fosfor pentoxide als raffinagement voor benzine. Industrial & Engineering Chemistry 1936, 28, 2, 190-193. Hersteld van pubs.ACS.borg.
- Epps, JR. EN.NAAR. (1950). Fotometrische bepaling van beschikbare fosfor pentoxide bij mestlizers. Analytische chemie 1950, 22, 8, 1062-1063. Hersteld van pubs.ACS.borg.
- Banerjee, a. et al. (1983). Gebruik van fosfor pentoxide: verestering van organische zuren. J. Borg. Chem. 1983, 48, 3108-3109. Hersteld van pubs.ACS.borg.
- Katoen, f. Albert en Wilkinson, Geoffrey. (1980). Geavanceerde anorganische chemie. Vierde druk. John Wiley & Sons.
- Kirk-othmer (1994). Encyclopedie van chemische technologie. Vierde druk. John Wiley & Sons.
- Ogliari, f.NAAR. et al. (2008). Synthese van fosfaatmonomeren en binding aan dentine: veresteringsmethoden en gebruik van fosfor pentoxide. Journal of Dentistry, Volume 36, nummer 3, maart 2008, pagina's 171-177. Hersteld van Scientedirect.com.
- « Aluminium acetaat (AL (CH3CO) 3) structuur, eigenschappen, gebruik
- Notatie ontwikkeld wat is, voorbeelden en oefeningen »

