Aluminium acetaat (AL (CH3CO) 3) structuur, eigenschappen, gebruik
- 1280
- 256
- Lonnie Rohan
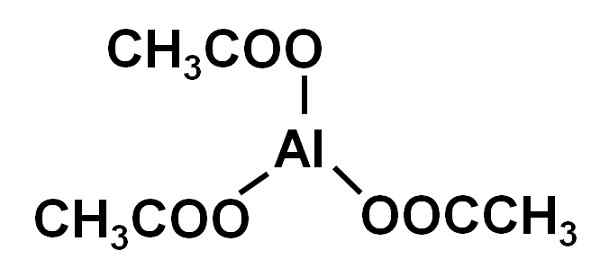
Hij aluminium acetaat Het is een organische verbinding gevormd door een aluminium ion naar de3+ en drie acetaat -ionen cho3Coo-. De chemische formule is al (cho3COO)3. Het is ook bekend als aluminium triacetaat. Het is een enigszins hygroscopisch en oplosbaar water vast in water.
Om deze verbinding te verkrijgen, moeten volledig watervrije omstandigheden worden gebruikt, dat wil zeggen, vrij van water, anders is het aluminium diapeaat bij (OH) (CH) de neiging om te vormen3COO)2.
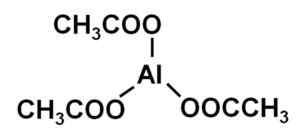 Aluminium triacetate AL (ch3COO)3. Auteur: Marilú Stea.
Aluminium triacetate AL (ch3COO)3. Auteur: Marilú Stea. Aluminium acetaatoplossingen hebben antibacteriële en antischimmelige eigenschappen, dus sinds de negentiende eeuw werden ze gebruikt om infecties te behandelen, vooral van de oren.
De bekendste is de oplossing van Burow, ontworpen door een Duitse arts. Het gebruik ervan heeft echter soms gedreven om schade aan het middenoor te schaden.
Deze oplossing is ook gebruikt om huidproblemen zoals jeuk en uitbarstingen te behandelen. Het wordt zelfs gebruikt als solury soothing.
Aluminiumacetaat en zijn derivaten worden gebruikt om zeer kleine structuren of aluminiumoxide te verkrijgen aan de2OF3. Deze structuren of nanodeeltjes kunnen de vorm hebben van bladeren, bloemen of nanobuisjes.
[TOC]
Structuur
Aluminium triaceaat wordt gevormd door een aluminium kation aan de3+ en drie acetaat anions cho3Coo-. Het is het aluminiumzout van azijnzuur ch3COOH.
Aluminium is gekoppeld aan acetaatanionen door de zuurstof hiervan. Met andere woorden, het is gekoppeld aan drie zuurstof. Deze vakbonden zijn ionisch.
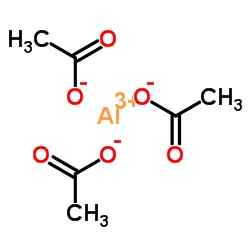 Ionische structuur van aluminiumacetaat. N4TR!Umbr [cc by-s (https: // creativeCommons.Org/licenties/by-sa/4.0)]. Bron: Wikimedia Commons.
Ionische structuur van aluminiumacetaat. N4TR!Umbr [cc by-s (https: // creativeCommons.Org/licenties/by-sa/4.0)]. Bron: Wikimedia Commons. Nomenclatuur
- Aluminium acetaat
- Aluminium triacetaat
- Aluminium ethanoaat
- BUROW OPLOSSING (Engelse vertaling BUROW's oplossing): Het is een aluminium acetaatoplossing.
Eigenschappen
Fysieke staat
Wit vaste stof.
Molecuulgewicht
204.11 g/mol
Oplosbaarheid
Oplosbaar in water.
Chemische eigenschappen
In waterige oplossing wordt aluminium triaceate opgelost en heeft de neiging het (OH) diacetaat te vormen (CH)3COO) en soms monoacetaat bij (oh)2(Ch3COO). Het hangt allemaal af van de pH en de hoeveelheid azijnzuur ch3COOH aanwezig in de oplossing.
Kan u van dienst zijn: oppervlaktespanning: oorzaken, voorbeelden, toepassingen en experimentenAL (Ch3COO)3 + H2Of ⇔ al (oh) (cho3COO)2 + Ch3COOH
AL (Ch3COO)3 + 2 H2Of ⇔ al (oh)2(Ch3COO) + 2 ch3COOH
Andere eigenschappen
Aluminiumacetaat is enigszins hygroscopisch, dat wil zeggen dat het de neiging heeft luchtwater te absorberen.
Het verkrijgen van
Aluminiumacetaat wordt bij voorkeur verkregen in strikt watervrije omstandigheden, dat wil zeggen in totale afwezigheid van water. Dit omvat ook afwezigheid van lucht, omdat dit vocht kan bevatten.
Een mengsel van ijs azijnzuur CH wordt verwarmd3COOH en azijnzuuranhydride (CH3CO)2Of in dergelijke omstandigheden die het huidige water kunnen elimineren. Aan dit hete mengsel wordt aluminium chloride alcl toegevoegd3 Ashidro Solid (zonder water).
Een witte vaste stof van Al (ch3COO)3.
Alcl3 + 3 ch3COOH → AL (Ch3COO)3 + 3 HCl
De totale afwezigheid van water is belangrijk om de vorming van aluminium monoacetaatzouten te vermijden bij (OH)2(Ch3COO) en aluminium diacetaat op (OH) (Cho3COO)2.
Het kan ook worden verkregen door reactie van aluminiumhydroxide op (OH)3 en azijnzuur ch3COOH.
Gebruik in de geneeskunde
Oor infecties
Aluminiumacetaat wordt sinds de negentiende eeuw gebruikt om otitis te behandelen, wat een ontsteking is van het externe of gemiddelde oor, meestal gepaard met infectie. Het gebruik ervan is te wijten aan het antibacteriële en antischimmeleffect.
Het is gebruikt in de vorm van een 13%aluminiumacetaatoplossing, oorspronkelijk bedacht door de Duitse arts Karl August von Burow, dus het wordt Burow Solution genoemd.
Er is gebleken dat de groei van micro -organismen remt die vaak worden aangetroffen bij medium of externe otitis, zoals Pseudomonas aeruginosa, Hij Staphylococcus aureus en de Proteus Mirabilis.
 Oorinfecties worden al vele jaren behandeld met aluminiumacetaat. Auteur: Ulrike Mai. Bron: Pixabay.
Oorinfecties worden al vele jaren behandeld met aluminiumacetaat. Auteur: Ulrike Mai. Bron: Pixabay. Er zijn echter mensen die melden dat deze oplossingen schadelijk kunnen zijn voor het oor. Sommige studies bij dieren onderzoeken hun toxische effecten voor het oor, maar hebben tegenstrijdige resultaten gemeld.
Het kan u van dienst zijn: zinkhydroxide (Zn (OH) 2)Bepaalde onderzoekers bevelen aan om aluminiumacetaat niet te gebruiken wanneer het trommelvliesmembraan is geperforeerd, omdat is waargenomen dat het een ontstekingseffect op het middenoor heeft.
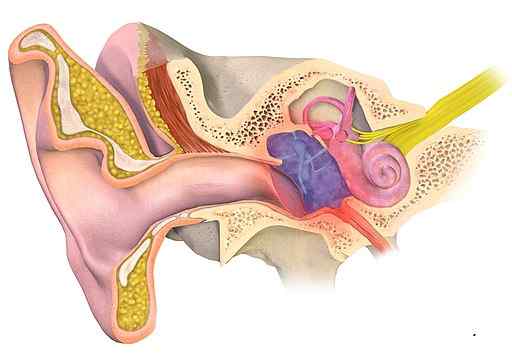 Het is niet handig om otitis media (blauwachtige zone in de figuur) te behandelen met aluminiumacetaat. Bruceblaus [CC BY-SA (https: // creativeCommons.Org/licenties/by-sa/4.0)]. Bron: Wikimedia Commons.
Het is niet handig om otitis media (blauwachtige zone in de figuur) te behandelen met aluminiumacetaat. Bruceblaus [CC BY-SA (https: // creativeCommons.Org/licenties/by-sa/4.0)]. Bron: Wikimedia Commons. Huidziektes
De oplossing van Burow wordt gebruikt als een antiseptisch, samentrekkend en als een actuele oplossing om ernstige uitbarstingen, dermatitis, ontsteking, jeuk, brandend en zonnebrand te behandelen. Oefent een rustgevend en verminderd effect van irritaties uit.
 Soms kunnen zonnebrand worden behandeld met een aluminiumacetaatoplossing. Auteur: Tumisu. Bron: Pixabay.
Soms kunnen zonnebrand worden behandeld met een aluminiumacetaatoplossing. Auteur: Tumisu. Bron: Pixabay. Andere gebruiken
Aluminium triaceate en zijn derivaten worden gebruikt voor veel kwalitatieve en kwantitatieve chemische experimenten.
Een afgeleide van aluminium triacetaat, diacetaat bij (OH) (CH3COO)2 Ook aluminiumhydroxideacetaat genoemd, wordt het gebruikt als een voorloper om gamma-alumina nanostructuren te verkrijgen (y-al2OF3)).
In dit geval betekent voorloper dat uit het aluminiumdiacetaat (op een bepaalde manier verkregen) de γ-Al-nanostructuren worden bereid2OF3, En dit wordt bereikt door het bij zeer hoge temperaturen te verwarmen.
Nanostructuren zijn zeer kleine deeltjes die alleen kunnen worden waargenomen via speciale microscopen zoals elektronische microscopen. Met aluminiumacetaat als voorloper zijn nanostructuren van γ-to-to-verkregen2OF3 Vergelijkbaar met bladeren, bloemen, vezels en zelfs nanobuisjes.
 Aluminiumoxide nanofribos kan worden verkregen met behulp van een aluminiumacetaatderivaat. Aleksei TR [CC BY-SA (https: // creativeCommons.Org/licenties/by-sa/4.0)]. Bron: Wikimedia Commons.
Aluminiumoxide nanofribos kan worden verkregen met behulp van een aluminiumacetaatderivaat. Aleksei TR [CC BY-SA (https: // creativeCommons.Org/licenties/by-sa/4.0)]. Bron: Wikimedia Commons. Stopgezet gebruik
Aan het begin van de 20e eeuw werd aluminiumacetaat gebruikt als voedselconservatief zoals ingeblikte worstjes.
Een aluminiumacetaatoplossing werd bereid door aluminiumsulfaat te mengen2(SW4))3, Caco calciumcarbonaat3, Azijnzuur ch3COOH en Agua H2Of, en toegevoegd aan voedsel.
Wanneer deze oplossing in contact komt met vlees, wordt aluminium in de bestanddelen ervan gefixeerd in de vorm van een verbinding die onoplosbaar is in kokend water, maar die in maagsappen oplost met ongeveer 80%.
Het kan u van dienst zijn: bromous acid (hbro2): fysische en chemische eigenschappen en gebruikAl in 1904 was het bekend dat aluminium zouten de spijsvertering vertonen, zowel in maag als in darm. Daarom is het een niet -convenient -praktijk om aluminium acetaatoplossingen toe te voegen aan ingeblikt voedsel.
 In het verleden werd aluminiumacetaat gebruikt als conserveermiddel in ingeblikte worst. Het is momenteel bekend dat het schadelijk is en er niet meer voor wordt gebruikt. Auteur: Changglc. Bron: Wikimedia Commons.
In het verleden werd aluminiumacetaat gebruikt als conserveermiddel in ingeblikte worst. Het is momenteel bekend dat het schadelijk is en er niet meer voor wordt gebruikt. Auteur: Changglc. Bron: Wikimedia Commons. Schadelijke effecten
Aangezien er onderzoeken zijn die melden dat aluminiumacetaat giftig kan zijn, zijn er tests uitgevoerd waarin aluminiumacetaat is geïnjecteerd in laboratoriummuizen.
De resultaten geven aan dat deze verbinding schade veroorzaakt aan de ruggengraat van deze dieren, evenals schade aan de chromosomen en sperma van de dieren. Met andere woorden, het is genotoxisch.
Dit waarschuwt voor mogelijke gezondheidsrisico's die overbelichting kunnen veroorzaken aan aluminiumacetaat en de zorg die tijdens het gebruik moet worden gebracht.
Referenties
- Mac-kay chace, en. (1904). Het gebruik van basisaluminiumacetaat als een conserveermiddel in worst. Journla of the American Chemical Society 1904, 26, 6: 662-665. Hersteld van pubs.ACS.borg.
- Hood, g.C. en ihde, een.J. (1950). Aluminiumacetaten en propionaten - de voorbereiding en compositie. Journal of the American Chemical Society 1950, 72, 5: 2094-2095. Hersteld van pubs.ACS.borg.
- Pitaro, J. et al. (2013). Ototoxiciteit van aluminium acetaat/benzenethoniumchloride otic oplossing in het chinchilla -diermodel. Laryngoscope, 2013; 123 (10): 2521-5. NCBI hersteld.NLM.NIH.Gov.
- Thorp, m.NAAR. et al. (2000). Burow's oplossing bij de behandeling van actieve muchosale chronische supuritieve otitis media: het bepalen van een effectieve verdunning. The Journal of Laryngology & Otology, juni 2000, vol. 114, PP.432-436. NCBI hersteld.NLM.NIH.Gov.
- D'Uza, Mr.P. et al. (2014). Beoordeling van genotoxy van studie -achetaat in beenmerg, mannelijke kiemcellen en foetale levercellen van Zwitserse albinomuizen. Mutation Research 766 (2014) 16-22. NCBI hersteld.NLM.NIH.Gov.
- Basaal, en. et al. (2015). De effecten van de oplossingen van Topical Burow en Castellani op het Midden -oorslijmvlies van ratten. J. Int Adv otol 2015; 11 (3): 253-6. Hersteld van geavanceerdeotologie.borg.
- OF.S. Nationale bibliotheek van geneeskunde. (2019). Stilling acetaat. Hersteld van PubChem.NCBI.NLM.NIH.Gov.
- Buttaravoli, P. En Leffler, s.M. (2012). Zonnebrand. Wat moeten we doen. In Minor Emergency (derde editie). Hersteld van Scientedirect.com.
- Thompson, E. en kalus, aan. (2017). Acte huidreacties en bacteriële infecties. Behandeling. In de Travel and Tropical Medicine Manual (vijfde editie). Hersteld van Scientedirect.com.
- Kim, T. et al. (2010). Morfologie Controleerbare synthese van gamma-alumin. Crystal Growth & Design, vol.10, nee. 7, 2010, pp.2928-2933. Hersteld van pubs.ACS.borg.
- Rajala, J.W. et al. (2015). Kern-shell elektrospun holle aluminiumoxide keramische vezels. Vezels 2015, 3, 450-462. MDPI hersteld.com.
- « Componenten van de vermelde geografische ruimte en hoe ze zich verhouden
- Fosforoxide (V) structuur, eigenschappen, verkrijgen, gebruik, risico's »

