Zinkoxide (ZnO) structuur, eigenschappen, gebruik, risico's
- 1343
- 140
- Irving McClure I
Hij zinkoxide Het is een anorganische verbinding waarvan de chemische formule ZnO is. Het bestaat alleen uit Zn -ionen2+ I2- in een verhouding van 1: 1; Het kristallijne netwerk kan echter een vacature van of presenteren2-, die plaats geeft structurele defecten die in staat zijn om de kleuren van de synthetische kristallen te veranderen.
Commercieel wordt het verkregen als een stoffige witte vaste stof (lager beeld), die rechtstreeks voorkomt door de oxidatie van het metalen zink door het Franse proces; of onderworpen aan carbotherme reductie tot zinkerts, zodat hun dampen vervolgens oxideren en eindigen.
 Klokglas met zinkoxide. Bron: Adam Rędzikowski [CC BY-SA 4.0 (https: // creativeCommons.Org/licenties/by-sa/4.0)]
Klokglas met zinkoxide. Bron: Adam Rędzikowski [CC BY-SA 4.0 (https: // creativeCommons.Org/licenties/by-sa/4.0)] Andere ZnO -voorbereidingsmethoden bestaan uit het neerslaan van hun hydroxide, Zn (OH)2, Van de waterige oplossingen van zinkzouten. Ook kunnen fijne films of morfologisch gevarieerde nanodeeltjes worden gesynthetiseerd door meer geavanceerde technieken zoals de chemische afzetting van hun dampen.
Dit metaaloxide wordt in de natuur gevonden als een zinietmineraal, waarvan de kristallen meestal geel of oranje zijn door metaalonzuiverheden. ZnO -kristallen worden gekenmerkt door piëzo -elektrische, thermochromatische, luminescerende, polaire en ook een zeer brede energieband in hun halfgeleider -eigenschappen te hebben.
Structureel is isomorf voor zinksulfide, ZnS, die hexagonale en kubieke kristallen overnemen vergelijkbaar met die van respectievelijk Wurzita en Blenda. Hierin is er een bepaald covalent karakter in de interacties tussen de Zn2+ I2-, die een heterogene verdeling van belastingen in het ZnO -kristal maakt.
De studies van de eigenschappen en het gebruik van de ZnO strekken zich uit tot de gebieden van fysica, elektronica en biomedicine. Het eenvoudigste en meest dagelijkse toepassingen blijven onopgemerkt in de samenstelling van gezichtscrèmes en persoonlijke hygiëneproducten, evenals in zonnebrandcrème.
[TOC]
Structuur
Polymorfen
ZnO kristalliseert in normale druk- en temperatuuromstandigheden in een hexagonale structuur van wurziet. In deze structuur de Zn -ionen2+ I2- Ze zijn gerangschikt in alternatieve lagen, zodat elk wordt omringd door een tetraëder, met ZnO4 of ozn4, respectievelijk.
Met behulp van een "sjabloon" of kubieke ondersteuning kan de ZnO ook worden gekristalliseerd in een kubieke structuur van zinkblenda; die, net als Wurzita, overeenkomt met isomorfe structuren (identiek in de ruimte maar met verschillende ionen) van zinksulfide, ZnS.
Naast deze twee structuren (Wurzita en Blenda) kristalliseert de ZnO onder hoge drukken (ongeveer 10 GPa) in de SAL GEMA -structuur, dezelfde als die van NaCl.
Kan u bedienen: referentie -elektrode: kenmerken, functie, voorbeeldenInteracties
De interacties tussen de Zn2+ I2- Ze presenteren een bepaald karakter van covalentie, dus er is gedeeltelijk een Zn-O covalente binding (beide atomen met SP-hybridisatie3), en vanwege de vervorming van de tetrahedra, manifesteren ze een dipoolmoment dat bijdraagt aan de ionische attracties van de ZnO -kristallen.
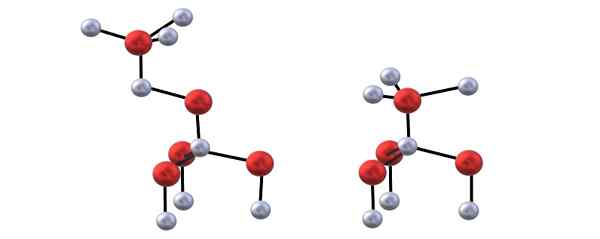
 Blenda -structuur (links) en Wurzita (rechts) van ZnO. Bron: Gabriel Bolívar.
Blenda -structuur (links) en Wurzita (rechts) van ZnO. Bron: Gabriel Bolívar. Je hebt het bovenste beeld om de bovengenoemde tetrahedra voor de ZnO -structuren te visualiseren.
Het verschil tussen de Blenda- en Wurzita -structuren ligt ook in wat u van bovenaf kunt zien, de ionen worden niet overschaduwd. In de Wurzita is bijvoorbeeld te zien dat de witte bollen (Zn2+) zijn net boven de rode bollen (of2-)). Aan de andere kant, in de kubieke structuur van Blenda gebeurt het niet omdat er drie lagen zijn: A, B en C in plaats van slechts twee.
Nanodeeltje morfologie
Zno's kristallen, hoewel ze de neiging hebben om hexagonale structuren van wurziet te hebben, met betrekking tot de morfologie van hun nanodeeltjes is een ander verhaal. Afhankelijk van de parameters en synthesemethoden kunnen deze vormen aannemen die zo gevarieerd zijn als staven, platen, bladeren, bollen, bloemen, riemen, naalden, onder andere.
Eigenschappen
Fysiek uiterlijk
Massief wit, toilet en bittere smaak vaste smaak. In de natuur kan het worden gekristalliseerd, met metaalonzuiverheden, als een zincita -mineraal. Als dergelijke kristallen wit zijn, hebben ze thermochromisme, wat betekent dat wanneer ze van kleur veranderen: van wit naar geel.
Evenzo kunnen hun synthetische kristallen roodachtige of groenachtige kleuren vertonen, afhankelijk van hun stoichiometrische zuurstofsamenstelling; dat wil zeggen de gaten of vacatures veroorzaakt door het gebrek aan anionen of2- beïnvloedt direct de weg in hoe licht interageert met ionennetwerken.
Molaire massa
81,406 g/mol
Smeltpunt
1974 ºC. Bij deze temperatuur lijdt thermische ontleding door het vrijgeven van zink- en moleculaire zuurstof of gasvormige zuurstof.
Dikte
5.1 g/cm3
Oplosbaarheid in water
ZnO is praktisch onoplosbaar in het water en geeft nauwelijks oplossingen met een concentratie van 0,0004% tot 18 ° C.
Anfoterisme
ZnO kan zowel reageren met zuren als met basen. Wanneer het reageert met een zuur in waterige oplossing, neemt de oplosbaarheid toe wanneer een oplosbaar zout wordt gevormd waar de Zn2+ uiteindelijk complexeren met watermoleculen: [Zn (OH2))6]2+. Het reageert bijvoorbeeld met zwavelzuur om zinksulfaat te produceren:
ZnO + H2SW4 → ZnSo4 + H2OF
Reageert op dezelfde manier met vetzuren voor hun respectieve zouten, zoals stearate en zinkpalmitaat.
Kan u van dienst zijn: onomkeerbare reactie: kenmerken en voorbeeldenEn wanneer het reageert met een basis, in aanwezigheid van water, worden chisal zouten gevormd:
ZnO + 2naOH + H2O → NA2[Zn (OH)4]
Warmte capaciteit
40.3 J/K · Mol
Directe energiekloof
3.3 eV. Deze waarde wordt gemaakt door een breedband halfgeleider, in staat om onder intense elektrische velden te werken. Het vormt ook kenmerken van een type halfgeleider N, die niet in staat is geweest om de redenen te verklaren dat er een extra bijdrage is van elektronen in zijn structuur.
Dit oxide onderscheidt zich door zijn optische, akoestische en elektronische eigenschappen, waarmee het wordt beschouwd als een kandidaat voor mogelijke toepassingen met betrekking tot de ontwikkeling van opto -elektronische apparaten (sensoren, lasers, fotovoltaïsche cellen). De reden voor dergelijke eigenschappen ontsnapt aan het veld van de fysica.
Toepassingen
Geneeskrachtig
Vijf oxide is gebruikt als additief in tal van witte crèmes voor de behandeling van irritaties, acnes, dermatitis, schaafwonden en scheuren in de huid. In dit gebied is het gebruik ervan om de irritaties te verlichten die worden veroorzaakt door luiers in babys -skins populair.
Het is ook een onderdeel van zonnebrandcrème, omdat samen met titaniumdioxide nanodeeltjes2, Help ultraviolette straling van de zon te blokkeren. Evenzo fungeert het als een dikker agent, dus het is in bepaalde duidelijke make -up, lotions, email, talk en zeep.
Aan de andere kant is ZnO een vijftien bron die wordt gebruikt in voedingssupplementen en vitamineproducten, evenals in granen.
Antibacterieel
Volgens de morfologie van zijn nanodeeltjes kan de ZnO worden geactiveerd onder ultraviolette straling om waterstofperoxiden of reactieve soorten te genereren die de celmembranen van micro -organismen verzwakken.
Wanneer dit gebeurt, kruisen de resterende nanodeeltjes van ZnO het cytoplasma en beginnen ze te interageren met het compendium van biomoleculen die de cel vormen, als gevolg daarvan als gevolg ervan de apoptose.
Dat is de reden waarom niet alle nanodeeltjes kunnen worden gebruikt in zonnebrandcomposities, maar alleen die welke antibacteriële activiteit missen.
Producten met dit type ZnO worden toegewezen, bedekt met oplosbare polymere materialen, om infecties, wonden, zweren, bacteriën en zelfs diabetes te behandelen.
Pigmenten en coatings
Het pigment dat bekend staat als Cinco Blanco is de ZnO, die wordt toegevoegd aan verschillende schilderijen en coatings om de metalen oppervlakken te beschermen tegen corrosie waar ze worden aangebracht. Bijvoorbeeld, verslaafde ZnO -coatings worden gebruikt om gegalvaniseerd ijzer te beschermen.
Aan de andere kant zijn deze coatings ook op het glas van de ramen gebruikt om te voorkomen dat warmte doordringen (als het in het buitenland is) of binnenkomen (indien binnen). Het beschermt ook enkele polymere en textielmaterialen tegen zijn verslechtering door werking van zonnestraling en warmte.
Kan u van dienst zijn: kalium (k)Bio -imagement
De luminescentie van ZnO -nanodeeltjes is bestudeerd om te worden gebruikt in bio -imaging, waardoor ze worden bestudeerd door de blauwe, groene of oranje lichten die uitstralen, de interne structuren van de cellen.
Additief
ZnO vindt ook gebruik als een additief in rubbers, cement, dentifric materialen, glas en keramiek, vanwege het lagere smeltpunt en zich daarom gedragen als een stichtingsmiddel.
Waterstofsulfide -eliminator
ZnO elimineert de onaangename gassen van h2S, helpen om enkele gase -emanaties te ontwerpen:
ZnO + H2S → Zns + H2OF
Risico's
Finch -oxide als zodanig is een niet -toxische en onschadelijke verbinding, dus de voorzichtige manipulatie van zijn vaste stof is geen risico.
Het probleem ligt echter in zijn rook, want hoewel het bij hoge temperaturen ontleedt, vervuilen de Rav -dampen de longen en veroorzaken ze een soort "metaalkoorts". Deze ziekte wordt gekenmerkt door de symptomen van hoest, koorts, gevoel van onderdrukking in de borst en een constante metaalachtige smaak in de mond.
Noch is Cancerigen, en de crèmes die het bevatten, hebben niet aangetoond dat ze de absorptie van zink in de huid verhogen, zodat ZnO -gebaseerde zonnen als veilig worden beschouwd; Tenzij er allergische reacties zijn, die in dat geval het gebruik ervan moeten stoppen.
Wat betreft bepaalde nanodeeltjes die bestemd zijn om bacteriën te bestrijden, kunnen deze negatieve effecten hebben als ze niet goed worden getransporteerd naar hun werkplaats.
Referenties
- Shiver & Atkins. (2008). Anorganische scheikunde. (Vierde druk). MC Graw Hill.
- Wikipedia. (2019). Zinkoxide. Opgehaald uit: in.Wikipedia.borg
- Hadis Morkoç en ümit Özgur. (2009). Zinkoxide: fundamentele, materialen en apparaattechnologie. [PDF]. Hersteld van: aanvraag.Wiley-VCH.van
- Parihar, m. Raja en r. Paulose. (2018). Een kort overzicht van structurele, elektrische en elektrochemische eigenschappen van zinkoxide nanodeeltjes. [PDF]. Hersteld van: ipme.Ru
- NAAR. Rodnyi en ik. V. Khodyuk. (2011). Optische en luminescentie -eigenschappen van zinkoxide. Hersteld van: arxiv.borg
- Siddiqi, k. S., Ur rahman, aan., Tajuddin, & Husen, een. (2018). Eigenschappen van zinkoxide nanaparticles en ES -activiteit tegen microben. Research Letters op nanoschaal, 13 (1), 141. Doi: 10.1186/S11671-018-2532-3
- ChemicalSafetyFacts. (2019). Zinkoxide. Teruggewonnen uit: chemicalsafetyfacts.borg
- Jinhuan Jiang, Jiang Pi en Jiye Cai. (2018). Het bevorderen van zinkoxide -nanodeeltjes voor biomedische toepassingen. Bioinorganische chemie en toepassingen, vol. 2018, artikel ID 1062562, 18 pagina's. doen.org/10.1155/2018/1062562
- « Waterstofperoxide (H2O2) structuur, eigenschappen, gebruik, verkrijgen
- Natriumsulfaat (Na2SO4) structuur, eigenschappen, gebruik, verkrijgen »

