Kalium tiocianaat (kscn) structuur, eigenschappen, gebruik

- 4110
- 1114
- Kurt Aufderhar Jr.
Hij Kalium tiocianaat Het is een anorganische verbinding gevormd door het kalium (k), zwavel (s), koolstof (c) en stikstof (n) elementen (n). De chemische formule is KSCN. Het is een kleurloze of witte oplosbare vaste stof in water. Wordt gevormd door een ionkalium k+ en een scn tiocianaat -ion-. De KSCN wordt op een overvloedige manier in speeksel gevonden.
Kalium Tiocianaat wordt gebruikt als laboratoriumreagens voor verschillende soorten chemische analyse. Het wordt ook gebruikt in inkten en schilderijen.
 Solid KSCN -kalium tiocyanaat. OF.Luci/cc by-sa (https: // creativeCommons.Org/licenties/by-sa/3.0). Bron: Wikimedia Commons.
Solid KSCN -kalium tiocyanaat. OF.Luci/cc by-sa (https: // creativeCommons.Org/licenties/by-sa/3.0). Bron: Wikimedia Commons. De KSCN is gebruikt om de dentinegelei (materiaal onder het tandenglazuur) op te lossen voordat het materiaal of hars wordt aangebracht dat de tanden herstelt. Het wordt ook gebruikt in vaccinonderzoek, omdat het ons in staat stelt bepaalde biochemische elementen uit bacteriën te extraheren.
Het wordt gebruikt in de vorm van een oplossing waar metalen oploven tijdens het polijstproces door elektriciteit of elektropulide. Hij is ook gebruikt bij het verkrijgen van vals bloed voor films en toneelstukken.
Soms wordt het onjuist gebruikt om de melkstabiliteit te vergroten wanneer het niet wordt gekoeld wordt gehouden. Maar het heeft het nadeel van het veroorzaken van hypothyreoïdie, een ziekte waarbij de schildklier slecht werkt.
[TOC]
Structuur
Kalium tiocianaat wordt gevormd door een kaliumkation k+ en een ncs tiocianaat anion-. De laatste wordt gevormd door een stikstof (N) bevestigd aan een koolstof (C) door een drievoud.
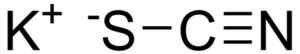 KSCN kalium tiocyanaat chemische structuur. Edgar181 / pub -domein. Bron: Wikimedia Commons.
KSCN kalium tiocyanaat chemische structuur. Edgar181 / pub -domein. Bron: Wikimedia Commons. Nomenclatuur
- Kalium tiocianaat
- Kaliumsulfocyanaat
- Potasic Tiociaans zuurzout
- Kalium rodanato
- Kalium rodanuro
Eigenschappen
Fysieke staat
Kleurloos of witte vaste stof.
Molecuulgewicht
97.18 g/mol
Smeltpunt
173 ºC
Ontledingstemperatuur
500 ºC
Dikte
1,88 g/cm3
Oplosbaarheid
Zeer oplosbaar in water: 217 g/100 ml bij 20 ° C, 238 g/100 ml bij 25 ° C. Oplosbaar in ethanol.
pH
Een KSCN -oplossing van 5% heeft een pH tussen 5,3 en 8,7.
Andere eigenschappen
De monsters van puur en droog kaliumthiocyanaat zijn voor onbepaalde tijd stabiel als ze in het donker worden bewaard in goed bedekte glazen potten. In contact met direct licht van de zon worden de kleurloze kristallen echter snel geelachtig.
De puur beschermde KSCN -zoutoplossingen zijn volledig stabiel.
De KSCN kan de gelatine en collageen opzwellen. Kalium tiocyanaat waterige oplossingen bij het reageren met mangaandioxide2 Ze oxideren en vormen tiocianogeen (SCN)2.
Het kan u van dienst zijn: Silver Yoduro (AGI): structuur, eigenschappen, verkrijgen, gebruikHet verkrijgen van
Kalium tiocianaat kan smeltende kaliumcyanide (kcn) bereiden met zwavel (s). De reactie is snel en kwantitatief.
KCN + S → KSCN
Het kan worden verkregen bij het oplossen van zwavel (s) in benzeen of aceton en het toevoegen van een kaliumcyanide -oplossing (KCN) in isopropanol. Deze reactie dient om de hoeveelheid zwavel van een oplossing te analyseren.
Kalium tiocianaat kan puur worden verkregen door opeenvolgende herkristallisaties uit water of ethanol.
Aanwezigheid in de natuur
Kalium tiocianaat is overvloedig in speeksel (15 mg/100 ml), maar is afwezig in het bloed.
Ook de melk van sommige zoogdieren (zoals de koe) heeft op een natuurlijke manier zeer kleine hoeveelheden tiocianato.
Toepassingen
In verschillende toepassingen
Kalium Tiocianaat is gebruikt in verschillende chemische analyses. Het is gebruikt voor de analyse of titratie van zilverionen, ook als een reagens en indicator van andere analyses.
KSCN wordt gebruikt in kleurstoffen en pigmenten. Het wordt gebruikt in schilderijen en inkten.
In de fotografie -industrie wordt het vooral gebruikt bij de productie van films voor fotografie, omdat het dient om de vaste afzetting van de gelei van plastic films mogelijk te maken.
De concentratie van tiocyanaat in bloed is gebruikt in medische ervaringen om te bepalen in welke mate sommige mensen roken, omdat tiocyanaat een product is dat is afgeleid van waterstofcyanide (HCN) aanwezig in tabaksrook.
In tandheelkundige toepassingen
Kalium tiocianaat is gebruikt bij herstel van dierentanden. Het is met succes toegepast op het oppervlak van de dentine als voorbehandeling voordat de agent wordt aangebracht om het open gat te krijgen of aan te sluiten.
Dentine is de laag die onder het glazuur van de tanden ligt.
 De KSCN heeft gediend om het tanden dentine -oppervlak te behandelen voordat het materiaal wordt aangebracht dat de cariësgaten vult. Auteur: Mudassar Iqbal. Bron: Pixabay.
De KSCN heeft gediend om het tanden dentine -oppervlak te behandelen voordat het materiaal wordt aangebracht dat de cariësgaten vult. Auteur: Mudassar Iqbal. Bron: Pixabay. Kalium tiocyanaat bevordert de zwelling van de gelatine die op het dentine staat, dus deze laag is gemakkelijk te verwijderen en is een betere hechting of bevestigd aan het materiaal dat de tand wordt waargenomen (hars).
In medische wetenschapslaboratoria
KSCN wordt gebruikt bij de bereiding van vaccins of bacterie -extracten.
Pathogene bacteriën groeit door incubatie in adequate laboratoriumcontainers. Vervolgens worden een fosfaat -pH -regulator en KSCN toegevoegd aan de container waar de bacterie -teelt zich bevindt.
Kan u van dienst zijn: chloorbenzeen (c6h5cl) Bacteriegewassen worden geëxtraheerd met KSCN om vaccins te verkrijgen voor medische ervaringen. Auteur: Wikiimages. Bron: Pixabay.
Bacteriegewassen worden geëxtraheerd met KSCN om vaccins te verkrijgen voor medische ervaringen. Auteur: Wikiimages. Bron: Pixabay. Een deel van deze bacteriebereiding wordt genomen en in een fles geplaatst. Het wordt op een voldoende tijd geroerd en de suspensie wordt gecentrifugeerd om de vloeistof van het vaste materiaal te scheiden. De supernatant (vloeistof) wordt verzameld en diad.
Het resultaat is een extract dat wordt gebruikt om wetenschappelijke ervaringen met laboratoriumdieren te vaccineren.
In de metaalindustrie
Kalium tiocianaat wordt gebruikt in metaalelektropulide. Elektropulide is een chemisch proces waardoor het oppervlak van een metaal kan worden behandeld om de micoruguestiteit te verminderen, dat wil zeggen, glad het metaaloppervlak gladstrijken.
Dit wordt gedaan met elektriciteit, waardoor het metaal een gladde werking is als een positieve pool of elektrolytische celanode. De ruwheid lost op in de kaliumtiocyanaatoplossing en het metaal is dus glad.
In het filmen of het filmen van theater
KSCN wordt gebruikt in bloedsimulatie in film- en televisiefilms of toneelstukken.
Een oplossing van kaliumtiocyanaat (KSCN) wordt bijvoorbeeld toegepast op het lichaamsgebied dat de gesimuleerde snit of agressie zal "lijden". Het plastic mes of de simulatie van het snijobjecten wordt gebaad in een ijzerchloride -oplossing (FECL3)).
Het "afschuif" object dat FADL heeft, wordt zachtjes doorgegeven3 op de huid bevochtigd in KSCN. Onmiddellijk zal een rode vlek of vlek zich zeer vergelijkbaar zijn met die van bloed.
 De KSCN is gebruikt om vals bloed te verkrijgen in films of theater. Auteur: Corey Ryan Hanson. Bron: Pixabay.
De KSCN is gebruikt om vals bloed te verkrijgen in films of theater. Auteur: Corey Ryan Hanson. Bron: Pixabay. Dit komt door de vorming van een ijzer- en watertiocyanaatcomplex [Fe (NCS) (h2OF)5]2+ die intens rood is, lijkt erg op bloed:
KSCN + FECL3 + 5 H2O → [fe (nc) (h2OF)5]2+ + 2 Cl- + KCL
 KSCN kalium tiocyanaat gemengd met ijzerchloride in water vormt een intense rode verbinding vergelijkbaar met bloed. Auteur: Clker-vrije-vector-afbeeldingen. Bron: Pixabay.
KSCN kalium tiocyanaat gemengd met ijzerchloride in water vormt een intense rode verbinding vergelijkbaar met bloed. Auteur: Clker-vrije-vector-afbeeldingen. Bron: Pixabay. Onjuist gebruik van kaliumtiocyanaat
Kaliumtiocyanaat wordt ongeldig gebruikt om te voorkomen dat melk wordt aangevallen door bacteriën of schimmels, verliest zijn eigenschappen en verslechtert.
In tropische landen wordt een methode genaamd "lacto-butxidasesysteem" of LP-systeem gebruikt, waardoor de opslagstabiliteit voor opslag bij hoge omgevingstemperaturen verhoogt, wanneer de koeling ervan niet mogelijk is.
 In sommige landen is er geen mogelijkheid om melk in de koelkast te zetten en daarom wordt kaliumtiocyanaat gebruikt om te voorkomen dat het verslechtert. Auteur: Thomas B. Bron: Pixabay.
In sommige landen is er geen mogelijkheid om melk in de koelkast te zetten en daarom wordt kaliumtiocyanaat gebruikt om te voorkomen dat het verslechtert. Auteur: Thomas B. Bron: Pixabay. Deze methode maakt gebruik van het natuurlijke antibacteriële melksysteem, dat wordt geactiveerd door de concentratie van tiocyanaat (al aanwezig in kleine hoeveelheden in melk) en waterstofperoxide (h (h2OF2)).
Deze methode is echter niet toegestaan in veel landen door de autoriteiten die bewerkte voedingsmiddelen reguleren.
Kan u dienen: Titanium: geschiedenis, structuur, eigenschappen, reacties, gebruikSommige gewetenloze mensen voegen KSCN toe om irrationeel te melken met of zonder H2OF2, Wat een gevaar vormt voor de gezondheid van de consument, aangezien Tiociaanse stoffen zijn die schade aan de schildklier veroorzaken en hypothyreoïdie kunnen veroorzaken wanneer ze in hoge concentraties worden ingenomen.
 Kalium tiociaanse melk kan schade veroorzaken aan de gezondheid van degenen die het innemen. Auteur: TakeApic. Bron: Pixabay.
Kalium tiociaanse melk kan schade veroorzaken aan de gezondheid van degenen die het innemen. Auteur: TakeApic. Bron: Pixabay. Risico's
Het moet worden vermeden om kalium thiocyanaatstof te bevorderen. Het is handig om handschoenen en beschermingsen te gebruiken bij het manipuleren van het. Na korte blootstelling aan kalium tiocyanato kan het effect veroorzaken op het zenuwstelsel, zoals overmatige emotie zonder motieven, agitatie en aanvallen.
Na een lange blootstelling kunnen de schildklier en het centrale zenuwstelsel worden beïnvloed, wat zich manifesteert als hypothyreoïdie en achteruitgang van sommige functies respectievelijk. Bij ingenomen kan verwarring, misselijkheid, braken, aanvallen en zwakte veroorzaken.
Als de KSCN ingeschakelt of brandt, worden zeer giftige cyanidegassen vrijgegeven; Dit gebeurt ook bij het toevoegen van zuren. In het laboratorium moet het worden gemanipuleerd in een zeer goed geventileerde extractiebel.
Referenties
- Jarvinen, l.Z. et al. (1998). Inductie van bescherming -immuniteit bij konijnen door COAD -toediening van geïnactiveerd Multocide pasteurella Toxine en kaliumthiocyanaatextract. Infectie en immuniteit, augustus 1998, p. 3788-3795. NCBI hersteld.NLM.NIH.Gov.
- Tani, en. en Togaya, T. (negentienvijfennegentig). Dentine -oppervlaktebehandeling zonder zuur. Dental Materials Journal 14 (1): 58-69, 1995. Hersteld van JSTAGE.JST.Gaan.JP.
- Kolthoff, ik.M. en Lingane, J.J. (1935). Kaliumthiocyanaat als een primaire standaardstof. Journal of the American Chemical Society 1935, 57, 11, 2126-2131. Hersteld van pubs.ACS.borg.
- Balmasov, een.V. et al. (2005). Elektropopolishing van zilver in water-organische oplossingen van kaliumthiocyanaat. Prot Met 41, 354-357 (2005). Link hersteld.Springer.com.
- Katoen, f. Albert en Wilkinson, Geoffrey. (1980). Geavanceerde anorganische chemie. Vierde druk. John Wiley & Sons.
- Lead, D.R. (redacteur) (2003). CRC Handbook of Chemistry and Physics. 85e CRC Press.
- Tyner, T. en Francis, J. (2017). Kalium thiocyanaat. ACS -reagenschemicaliën. Hersteld van pubs.ACS.borg.
- Kanthale, p. et al. (2015). Kwalitatieve test voor de detectie van extern thiocyanaat in melk. J Food Sci Technol (maart 2015) 52 (3): 1698-1704. NCBI hersteld.NLM.NIH.Gov.
- Roy, D. et al. (2018) Silicium kwantum dot-gebaseerde fluorescerende sonde: synthesekarakterisering en herkenning van thiocyanaat in menselijk bloed. ACS Omega 2018, 3, 7, 7613-7620. Hersteld van pubs.ACS.borg.
- Gammon, K. (2018). De wetenschap van nepbloed. Inside Science. Opgehaald uit insidescece.borg.
- « Cerebrale atrofie -kenmerken, symptomen en oorzaken
- Pijnfysiologie, hersenprocessen en receptoren »

