Hypertonische oplossing
- 3346
- 615
- Miss Herman Russel
We leggen uit wat hypertone oplossingen zijn, hun kenmerken, wat het nut zijn, de verschillen met de hypotonische en geven verschillende voorbeelden
Velen zullen verbaasd zijn om te weten dat de manier waarop planten water door hun wortels absorberen en de manier waarop de vingers van de handen zijn gerimpeld bij het baden in zeewater, ze zijn nauw verwant.
Beide dingen gebeuren dankzij het bestaan van een membraan dat functioneert als een filter, en een hypertone oplossing die er letterlijk water doorheen zuigt. Maar wat is een hypertone oplossing?
In dit artikel zal deze vraag worden beantwoord en zullen de meest relevante kenmerken van hypertone oplossingen ook worden gepresenteerd, waar ze voor zijn, hoe ze worden onderscheiden van andere soorten oplossingen en enkele voorbeelden van hetzelfde.
Wat is een hypertone oplossing?
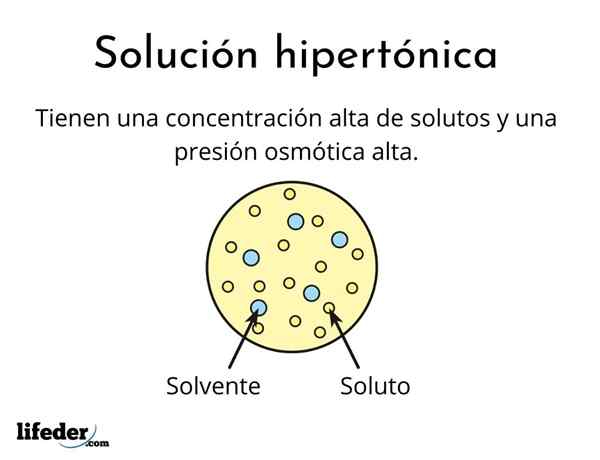
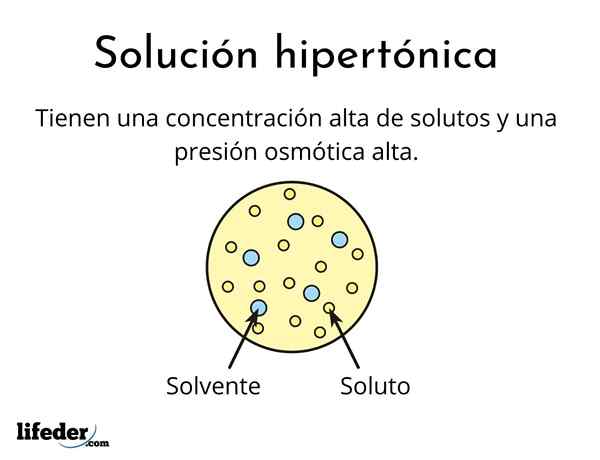
A hypertonische oplossing Het is er een die een totale concentratie osmolair actieve opgeloste opgeloste opgeloste stoffen bevat dan die van een andere referentieoplossing. Osmolair actief betekent dat opgeloste stoffen geen speciaal type membraan (vergelijkbaar met een stof) niet kunnen kruisen dat fungeert als een zeef of filter, dat wil zeggen, laat het water passeren, en niet naar de opgeloste deeltjes.
Deze hoge concentratie opgeloste stoffen zorgt ervoor dat hypertone oplossingen een hoge osmotische druk hebben. Deze druk is wat praktisch het water door het membraan zuigt, dat osmose wordt genoemd.
Het hypertonische woord komt van het Griekse voorvoegsel hyper-, wat "op of boven" en "tonen" betekent, wat betekent spanning of druk, dus hypertone betekent letterlijk "dat het meer druk of spanning heeft".
Het is belangrijk om in gedachten te houden dat, in de biologie en geneeskunde, op voorwaarde dat er sprake is van hypertone oplossing, het verwijst naar een oplossing die meer geconcentreerd is dan de oplossing in bloed, dat bloedplasma wordt genoemd.
Kenmerken van hypertone oplossingen
Hypertonische oplossingen hebben enkele basiskenmerken:
Ze worden gevormd door een oplosmiddel en ten minste één opgeloste stof
Geen enkele oplossing kan hypertone zijn, maar zo is het erg geconcentreerd. De opgeloste stof moet niet in staat zijn om het membraan over te steken, terwijl het water het zonder probleem moet kunnen passeren, anders wordt de osmotische druk niet gegenereerd.
Ze hebben hoge concentraties opgeloste stoffen
Dit is wat hen hypertone oplossingen maakt. Zoals een moment geleden vermeld, zijn hypertone oplossingen meer geconcentreerd dan bloed.
Het kan u van dienst zijn: fractionele destillatie: proces, apparatuur, toepassingen, voorbeeldenZe kunnen verschillende composities hebben
Een hypertone oplossing kan een enkele opgeloste stof zoals zout bevatten, of kan een mengsel van opgeloste stoffen bevatten zoals zouten en suikers, bijvoorbeeld.
Soluto's kunnen ionisch, neutraal of beide zijn
De verkoop bevat ionen met elektrische ladingen die hen niet het membraan laten oversteken, dus ze zijn klein. Andere opgeloste stoffen hebben geen ionen, maar ze zijn groot en dik en passen niet door de gaten.
Ze hebben een hoge osmotische druk
Zoals hierboven vermeld, hebben hypertone oplossingen een osmotische druk groter dan bloed.
Ze kunnen cellen uitdrogen
Hypertonische oplossingen extraheren het water uit cellen waardoor ze als rozijnen achterlaten. Daarom zijn onze handen en voeten gerimpeld als we baden op het strand.
Waar zijn hypertone oplossingen voor?
Hypertonische oplossingen hebben veel toepassingen in het dagelijks leven, en ook in de geneeskunde. Sommige van de meest voorkomende toepassingen zijn:
Ze worden gebruikt om voedsel te bewaren
- Voorbeeld: de perziken in siroop rotten niet omdat de siroop veel opgeloste suiker heeft en een zeer hypertone oplossing is. Door cellen uit te uitdragen, staan hypertone oplossingen niet toe dat schimmels en bacteriën in voedsel zijn, omdat ze sterven aan dorst. Hierdoor kan voedingsmiddelen meer meegaan.
Ze dienen om ontstekingen te verminderen
- Voorbeeld: wanneer iemand een ongeluk heeft en het hoofd raakt, zijn er vele malen een ontsteking in de hersenen. Om de patiënt te genezen, injecteren artsen een oplossing van 7,5% zoutoplossing. Deze oplossing zuigt praktisch water, waardoor ontstekingen in de hersenen worden verminderd.
Ze dienen om elektrolyten te vervangen.
- Voorbeeld: natrium is een elektrolyt die we moeten leven, en wanneer een patiënt weinig natrium in het bloed heeft, wordt een zoutoplossing van 7,5% geïnjecteerd om het verloren natrium aan te vullen.
Ze worden gebruikt voor parenteraal voedsel
- Voorbeeld: wanneer mensen niet door de mond of door een buis kunnen eten, voeden ze in een hypertone oplossing die een soort suiker bevat die glucose wordt genoemd.
Verschillen met hypotone en isotone oplossingen
Net zoals er hypertone oplossingen zijn, zijn er ook hypotone en isotone oplossingen. Het verschil tussen de laatste en hypertone oplossingen is de concentratie. Hypotone oplossingen zijn die die minder geconcentreerd zijn dan bloed, en isotonisch hebben dezelfde concentratie als bloed.
Zuiver water is bijvoorbeeld, omdat het niets opgelost heeft, hypotonisch is, terwijl kokoswater zouten en suikers heeft met een concentratie die bijna gelijk is aan die van bloed, dus het is isotonisch.
Naast het onderscheiden van hun concentratie verschillen hyper-, hypo- en isotone oplossingen in de manier waarop ze cellen beïnvloeden.
Het volgende beeld toont het effect van de verschillende soorten oplossingen op rode bloedcellen (de kleine cellen die het bloed rood maken).
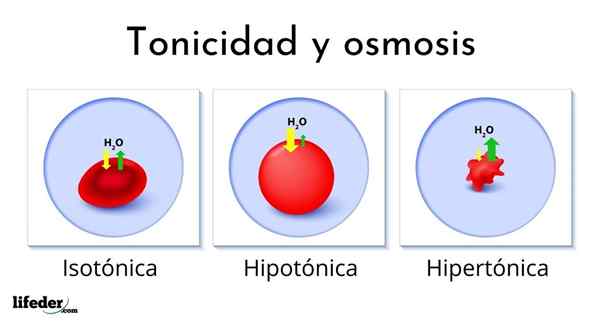
Als rode bloedcellen in een hypertone oplossing worden geïntroduceerd, extraheert het water, ontdidt het en laat ze gerimpeld als een pass.
Aan de andere kant, als ze worden geïntroduceerd in een hypotone oplossing, absorberen rode bloedcellen water en zwellen, zelfs barsten als een ballon die te veel opblaast. Ten slotte, als ze worden geïntroduceerd in een isotone oplossing, zullen water binnen en buiten de rode bloedcellen in evenwicht zijn, zodat er niets gebeurt.
Voorbeelden van hypertone oplossingen
Suikersiroop
 Perziken in siroop
Perziken in siroop De siroop waarin perziken en andere vruchten worden bewaard, bevat zeer hoge suikerconcentraties, dus het is een hypertone oplossing.
De pekel
De pekel is een oplossing van water en zout met zeer hoge concentraties tussen 3,5% en 25%, die bijna 30 keer meer geconcentreerd kan worden dan bloed (dat wil zeggen, het is erg hypertonisch).
De azijn
Een gewone azijn is een hypertone oplossing, omdat deze een concentratie heeft van tussen 3% en 5% azijnzuur. Balsamico -azijnreducties zijn nog meer geconcentreerd.
Kan u van dienst zijn: dimethylamine ((CH3) 2NH): structuur, eigenschappen, gebruik, risico'sHetzelfde bloed van onze aderen, na veel zweten.
Bij het sporten en zweten elimineert het lichaam water en zouten, maar elimineert meer water dan zouten (zweet is hypotonisch) zodat het bloed concentreert en hypertone wordt.
Zeewater
Zeewater bevat veel opgeloste zouten, met een totale concentratie van ongeveer 3,5%, waardoor het hypertonisch is. Daarom rimpelt zeewater onze vingers.
Suikerachtige drankjes
Cola -dranken en andere suikerhoudende dranken kunnen tot 10% suiker bevatten, evenals zouten en andere opgeloste stoffen met concentraties groter dan bloed.
5% dextrose -oplossing en 0,45% natriumchloride (D5 ½ ns)
Dit is een voorbeeld van een hypertone oplossing die wordt gebruikt om mensen te voeden die normaal niet bij de mond kunnen eten.
25% mannitol
Dit is een oplossing die vaak wordt gebruikt om schokken op het hoofd te behandelen. Het is vier keer meer geconcentreerd dan bloed.
7,5% zoutoplossing
Het is een vrij geconcentreerde zoutoplossing die ook wordt geïnjecteerd bij sommige patiënten met bepaalde ziekten in de aderen.
Commerciële sappen
Alle sappen die in de supermarkt worden gekocht en die niet natuurlijk zijn, hebben zeer hoge suikerconcentraties die ze hypertonisch maken.
Referenties
- Sweeney J. Hypernatremie beheren. Verzorging. September 2010; 40 (9): 63.
- Pekel. Wikipedia. 2021. Genomen van.Wikipedia.org/wiki/pekel.
- Zeewater. Wikipedia. 2021. Genomen van.Wikipedia.Org/wiki/zeewater.
- Chavaltamrong B, Pidatcha P, Thavisri U. Elektrolyten, suiker, calorieën, osmolariteit en pH van dranken en kokoswater. Zuidoost -Aziatische J Trop Med Public Health. September 1982; 13 (3): 427-431.
- 5% dextrose en 0.45% natriumchloride -injectie, USP. FDA. 2006. Genomen van AccessData.FDA.Gov/drugsatfda_docs/label/2006/017607S123LBL.PDF.
- Llorente G, Niño MC. Manitol versus hypertone zoutoplossing in neuroanesthesie. Colombiaanse anesthesiologie magazine. Januari-maart 2015; 43 (1): 29-39.
- Heiligen mm, e. Behandeling van acute pensioninezuur met intraveneus hypertone natriumchloride of bicarbonaatoplossingen geneukt door intrauminaal water. Onderzoek in de diergeneeskunde. Februari 2020; 128: 24-34.
- Dini-g. E, Abreu-C. JD, López-M. EN. Osmolaliteit van frequente consumptiedranken. Klinisch onderzoek. December 2004; 45 (4).

