Organische zouten
- 627
- 13
- Lonnie Rohan
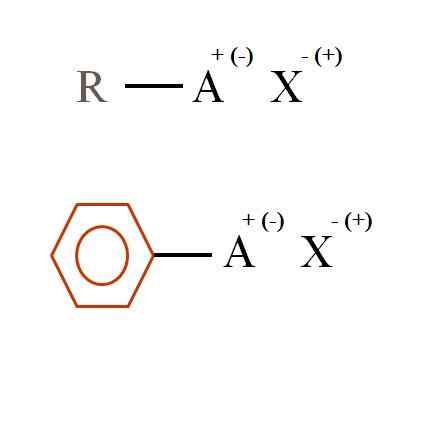 Twee algemene chemische formules voor organische zouten. Bron: Gabriel Bolívar
Twee algemene chemische formules voor organische zouten. Bron: Gabriel Bolívar Wat zijn biologische zouten?
De Organische zouten Ze zijn een dicht aantal ionische verbindingen met ontelbare kenmerken. Eerder afgeleid van een organische verbinding, die een transformatie heeft ondergaan waarmee het een lading kan zijn, en dat de chemische identiteit ervan afhangt van de bijbehorende ion.
In het superieure beeld worden twee zeer algemene chemische formules getoond voor organische zouten. De eerste, R-AX, wordt geïnterpreteerd als een verbinding in wiens koolstofstructuur een atoom of groep A, draagt een positieve + of negatieve belasting (-).
Zoals te zien is, is er een covalente binding tussen R en A, R-A, maar op zijn beurt heeft het een formele belasting die aan trekt (of afstoot) naar het ion x. Het laadbord hangt af van de aard van A en de chemische omgeving.
Als het positief was, hoeveel x zou kunnen communiceren? Met één, gezien het principe van elektroneutraliteit (+1-1 = 0). Wat is echter de identiteit van x? Anion X zou de CO kunnen zijn32-, Vereist twee kationen RA+; Een halogenide: f-, Klet-, BR-, enz.; of zelfs een andere compound-. De opties zijn niet te overzienbaar.
Evenzo kan een organisch zout aromatisch zijn, geïllustreerd in de benzenische bruine ring. Koper benzoaat zout (ii), (c6H5COO)2Cu bestaat bijvoorbeeld uit twee aromatische ringen met negatief geladen carboxy -groepen, die interageren met de kation cu2+.
Fysische en chemische eigenschappen van organische zouten
Uit de afbeelding kan worden bevestigd dat organische zouten bestaan uit drie componenten: de organische, R of AR (de aromatische ring), een atoom- of groepsdrager van de ionische belasting a en een tegenion x.
Net zoals chemische identiteit en structuur worden gedefinieerd door dergelijke componenten, zijn hun eigenschappen op dezelfde manier van hen afhankelijk.
Uit dit feit kunnen bepaalde algemene eigenschappen die aan de overgrote meerderheid van deze zouten voldoen, worden samengevat.
Kan u van dienst zijn: oxidatienummer: concept, hoe u het uit kunt halen en voorbeeldenHoge moleculaire massa's
Uitgaande van mono- of veelzijdige anorganische anionen, hebben organische zouten meestal veel grotere moleculaire massa's dan anorganische zouten. Dit is voornamelijk te wijten aan het koolzuurhoudende skelet, waarvan de eenvoudige C-C-bindingen, en zijn waterstofatomen, veel massa voor de compound bieden.
Daarom zijn zij degenen die verantwoordelijk zijn voor hun hoge moleculaire massa.
Amfiphylische en oppervlakteactieve stoffen
Organische zouten zijn amfifiele verbindingen, dat wil zeggen dat hun structuren zowel hydrofiele als hydrofobe uitersten hebben.
Wat zijn zulke uitersten? R of AR vertegenwoordigen het hydrofobe uiteinde, omdat hun atomen van C en H geen grote affiniteit hebben voor watermoleculen.
NAAR+(-), De atoom- of vrachtdragergroep is het hydrofiele einde, omdat het bijdraagt aan het dipoolmoment en interageert met het water dat dipool vormt (ra+ Oh2)).
Wanneer hydrofiele en hydrofobe gebieden gepolariseerd zijn, wordt amfifiele zout een oppervlakteactieve stof, een stof die veel wordt gebruikt voor de uitwerking van wasmiddelen en onverstoorheden.
Hoog kookpunten of fusie
Net als anorganische zouten hebben organische zouten ook hoge smelt- en kookpunten, vanwege de elektrostatische krachten die regeren in vloeibare of vaste fase.
Met een organische component R of AR nemen echter andere soorten van der Waals (Londen, Dipolo-Dipolo, waterstofbruggen) op een of andere manier deel met elektrostatisch.
Om deze reden zijn de vaste of vloeibare structuren van organische zouten in eerste instantie complexer en gevarieerder. Sommigen van hen kunnen zich zelfs gedragen zoals vloeibare kristallen.
Zuurgraad en basiciteit
Organische zouten zijn meestal sterkere zuren of basen dan anorganische zouten. Dit komt omdat het bijvoorbeeld in aminezouten een positieve belasting heeft vanwege de link met een extra waterstof: a+-H. Doneer vervolgens, in contact met een basis, het proton opnieuw om opnieuw een neutrale verbinding te zijn:
Het kan u van dienst zijn: Strontium: geschiedenis, structuur, eigenschappen, reacties en gebruikRa+H + b => ra + hb
De H behoort tot A, maar is geschreven, omdat het tussenbeide komt in de neutralisatiereactie.
Aan de andere kant, ra+ Het kan een groot molecuul zijn, niet in staat om vaste stoffen te vormen met een kristallijn netwerk stabiel met hydroxylanion of oxhydrilo oh-.
Als dit zo is, het zoutraam+Oh- Het gedraagt zich als een sterke basis; Zelfs zo eenvoudig als NaOH of KOH:
Ra+Oh- + Hcl => racl + h2OF
Opmerking in de chemische vergelijking dat het anion CL- Vervang OH-, het vormen van de zout ra+Klet-.
Gebruik van organische zouten
Het gebruik van organische zouten zal variëren afhankelijk van de identiteit van R, AR, A en X. Bovendien hangt de toepassing waaraan ze worden toegewezen ook af van het type vaste stof of vloeistof die ze vormen. Sommige algemeenheden in dit opzicht zijn:
- Ze dienen als reagentia voor de synthese van andere organische verbindingen. Rax kan fungeren als een "gever" van de R -keten om toe te voegen aan een andere verbinding die een goede uitgaande groep vervangt.
- Het zijn oppervlakteactieve stoffen, dus ze kunnen ook als smeermiddelen worden gebruikt. Metalen carboxylalaatzouten worden voor dit doel gebruikt.
- Ze staan het toe om een breed scala aan kleurstoffen te synthetiseren.
Voorbeelden van biologische zouten
Carboxyleert
Carbonzuren reageren met een hydroxide in een neutralisatiereactie, waardoor carboxylalaatzouten worden veroorzaakt: RCOO- M+; waar m+ Het kan elk metaalkation zijn (NA+, PB2+, K+, enz.) of het ammonium NH -kation4+.
Vetzuren zijn lange keten carbonzuren, ze kunnen verzadigd en onverzadigd zijn. Palmitinezuur behoren tot de verzadigde (kies3(Ch2))14COOH). Dit is het palmitaatzout, terwijl het stearinezuur (cho3(Ch2))16COOH vormt het stear -zout. Zepen worden uit deze zouten gevormd.
Kan u van dienst zijn: algemene gaswetgevingIn het geval van benzoëzuur, c6H5COOH (waar C6H5- Het is een benzeenring), wanneer het reageert met een basis vormt de zouten van benzoaat. In alle carboxilateert de groep -co- Vertegenwoordigt een (rax).
Lithium diaquilcupratos
Lithium Day is nuttig bij de organische synthese. De formule is [R-Cu-R]-Li+, waarin het koperatoom een negatieve belasting draagt. Hier vertegenwoordigt koper het atoom van de afbeelding.
Sulfoniumzouten
Ze worden gevormd uit de reactie van een organisch sulfide met een alkylhalogenide:
R2S + r'x => r2R's+X
Voor deze zouten heeft het zwavelatoom een positieve formele belasting (s+) met drie covalente links.
Oxyio zouten
Evenzo reageren de ethers (de geoxygeneerde analogen van de sulfiden) met de hydrasiden om de oxykamers te vormen:
Ror ' + hbr ro+HR ' + BR-
Het HBR -zuurproton is consequent gekoppeld aan het ether -zuurstofatoom (r2OF+-H), het positief opladen.
Amina -zouten
Amines kunnen primair, secundair, tertiair of quaternair zijn, net als hun zouten. Ze worden allemaal gekenmerkt door een atoom van H te hebben gekoppeld aan het stikstofatoom.
Dus, rnh3+X- Het is een primair aminezout; R2NH2+X-, van secundaire Amina; R3NH+X-, van tertiair amine; en r4N+X-, van quaternair amine (quaternair ammoniumzout).
Diazoniumzouten
Eindelijk, diazoniumzouten (rn2+X-of arildiazonium (RNA2+X-), ze vertegenwoordigen het startpunt van veel organische verbindingen, vooral de azoïsche kleurstoffen.
Referenties
- Francis a. Schildpad. Organic Chemistry (zesde editie, PP. 604-605, 697-698, 924). MC Graw Hill.
- Graham Solomons T.W., Craig B. Friteuse. Organische chemie. Amines (10e editie.)). Wiley Plus.
- Wikipedia (2018). Zout (chemie). Genomen van: in.Wikipedia.borg
- Steven A. Hardinger (2017). Geïllustreerde woordenlijst van organische chemie: zouten. Hersteld van: chem.UCLA.Edu
- Chevron Oronite (2011). Carboxyleert. [PDF]. Hersteld van: Oronite.com

