Monomeren
- 1927
- 418
- Miss Herman Russel
 Het monomeer is een moleculair massamolecuul gekoppeld aan andere monomeren door chemische links
Het monomeer is een moleculair massamolecuul gekoppeld aan andere monomeren door chemische links Wat zijn monomeren?
De monomeren Het zijn kleine of eenvoudige moleculen die de basis- of essentiële structurele eenheid vormen van grotere of complexe moleculen die polymeren worden genoemd. Monomeer is een woord van Griekse afkomst dat betekent knobbeltje, een en Louter, deel.
Terwijl een monomeer zich bij een andere aansluit, wordt een dimeer gevormd. Door dit op zijn beurt aan te sluiten met een ander monomeer, vormt het een trimeer, enzovoort, om korte ketens te vormen die oligomeren worden genoemd, of langere ketens, die de zo -called polymeren zijn.
Monomeren binden of polymeriseren door chemische bindingen te vormen door elektronenparen te delen; dat wil zeggen, ze voegen zich aan bij covalente links.
Deze unie van monomeren staat bekend als polymerisatie. Monomeren van hetzelfde type of anders kunnen worden verbonden, en het aantal covalente bindingen dat ze kunnen vaststellen met een ander molecuul zal de structuur van het polymeer die vormt (lineaire, hellende ketens of drie -dimensionale structuren) bepalen).
Er is een breed scala aan monomeren, waaronder die van natuurlijke oorsprong. Deze behoren en ontwerpen de organische moleculen die biomoleculen worden genoemd, aanwezig in de structuur van levende wezens.
Bijvoorbeeld aminozuren die eiwitten vormen; De koolhydraat- en mononucleotide -monosaccharideneenheden die nucleïnezuren vormen. Er zijn ook synthetische monomeren, waardoor een ontelbare verscheidenheid aan inerte polymere producten, zoals schilderijen of kunststoffen, uitwerkt.
Kenmerken van monomeren
Monomeren binden door covalente bindingen
De atomen die deelnemen aan de vorming van een monomeer blijven verenigd door sterke en stabiele links zoals de covalente link. Evenzo polymeriseren of binden monomeren met andere monomere moleculen door deze links, waardoor kracht en stabiliteit voor polymeren.
Deze covalente bindingen tussen de monomeren kunnen worden gevormd door chemische reacties die zullen afhangen van de atomen die het monomeer vormen, de aanwezigheid van dubbele bindingen en andere kenmerken die de structuur van het monomeer presenteren.
Het polymerisatieproces kan worden gegeven door een van de volgende drie reacties: door condensatie, toevoeging of vrije radicalen. Elk van hen brengt hun eigen mechanismen en groeimodus in.
Monomeerfunctionaliteit en polymeerstructuur
Een monomeer kan worden verbonden met ten minste twee andere monomere moleculen. Deze eigenschap of kenmerk is wat bekend staat als monomerenfunctionaliteit, en dat is wat hen in staat stelt de structurele eenheden van macromoleculen te zijn.
Het kan u van dienst zijn: kaliumnitriet (kno2): structuur, eigenschappen en gebruikMonomeren kunnen bifunctioneel of polyifunctioneel zijn, afhankelijk van de actieve of reagensplaatsen van het monomeer; dat wil zeggen van de atomen van het molecuul die kunnen deelnemen aan de vorming van covalente bindingen met de atomen van andere moleculen of monomeren.
Dit kenmerk is ook belangrijk, omdat het nauw verbonden is met de structuur van de polymeren die zich conformeren, zoals hieronder gedetailleerd.
Bifunctionaliteit: lineair polymeer
De monomeren zijn bifunctioneel wanneer ze slechts twee vakbondssites hebben met andere monomeren; Dat wil zeggen, de monomeer kan slechts twee covalente bindingen vormen met andere monomeren en alleen lineaire polymeren vormen.
Onder lineaire polymeren kunnen ethylenglycol en aminozuren als voorbeeld worden genoemd.
Polyifunctionele monomeren - drie -dimensionale polymeren
Er zijn monomeren die kunnen worden verbonden met meer dan twee monomeren en de structurele eenheden van grotere functionaliteit vormen.
Ze worden polyifunctioneel genoemd en zijn die geproduceerd door vertakte, netwerk- of drie -dimensionale polymere macromoleculen; Zoals polyethyleen bijvoorbeeld.
Skelet of centrale structuur
Met dubbele binding tussen koolstof en koolstof
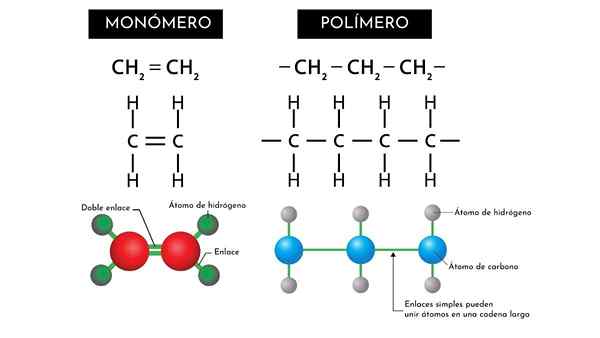
Er zijn monomeren die in hun structuur een centraal skelet vormen dat wordt gevormd door ten minste twee koolstofatomen verenigd door een dubbele binding (C = C).
Op zijn beurt presenteert deze centrale keten of structuur verenigde atomen lateraal die kan veranderen door een ander monomeer te vormen (r2C = Cr2)).
Als een van de R -ketens wordt gewijzigd of vervangen, wordt een ander monomeer verkregen. Ook wanneer deze nieuwe monomeren zich aansluiten bij een ander polymeer.
Het kan worden genoemd als een voorbeeld van deze groep monomeren het propyleen (h2C = Ch3H), tetrluorethyleen (f2C = CF2) en vinylchloride (h2C = CCLH).
Twee functionele groepen in de structuur
Hoewel er monomeren zijn met een enkele functionele groep, is er een brede groep monomeren met twee functionele groepen in hun structuur.
Aminozuren zijn hier een goed voorbeeld van. Ze hebben een amino functionele groep (-nh2) en de functionele groep carbonzuur (-cooh) verenigd tot een centraal koolstofatoom.
Dit kenmerk van het zijn van een diffuncties monomeer geeft het ook het vermogen om lange polymeerketens te vormen, zoals de aanwezigheid van dubbele links.
Functionele groepen
Over het algemeen worden de door de polymeren gepresenteerde eigenschappen gegeven door de atomen die de laterale ketens van de monomeren vormen. Deze ketens vormen de functionele groepen organische verbindingen.
Kan u van dienst zijn: wet van meerdere verhoudingenEr zijn families van organische verbindingen waarvan de kenmerken worden gegeven door functionele groepen of zijketens. Als voorbeeld is de functionele functionele groep R-Cooh carbonzuur, de amino R-NH-groep2, R-OH-alcohol, onder vele anderen die deelnemen aan polymerisatiereacties.
Vereniging van monomeren gelijk of van verschillende typen
Unie van gelijke monomeren
Monomeren kunnen verschillende klassen van polymeren vormen. Ze kunnen lid worden van gelijke monomeren of hetzelfde type en de zo -aangedreven homopolymeren genereren.
Als voorbeeld kunt u het stuk vermelden, een monomeer dat het polystyreen vormt. Zetmeel en cellulose zijn ook voorbeelden van homopolymeren gevormd door lange vertakte ketens van de glucosemonomeer.
Unie van verschillende monomeren
De unie van verschillende monomeren vormen de copolymeren. De eenheden worden herhaald in verschillende getallen, volgorde of sequentie in de structuur van de polymere ketens (A-B-B-B-B-A-A-B-A-A- ……).
Als een voorbeeld van copolymeren kan het nylon worden genoemd, een polymeer gevormd door repetitieve eenheden van twee verschillende monomeren. Dit zijn dicarbonzuur en een diaminemolecuul, dat bindt via condensatie in equimolaire (gelijke) verhoudingen.
Verschillende monomeren kunnen ook worden samengevoegd in ongelijke verhouding, zoals het geval van de vorming van een gespecialiseerd polyethyleen dat als basisstructuur het 1-octone monomeer plus het ethyleenmonomeer heeft.
Soorten monomeren
Er zijn veel kenmerken die het mogelijk maken om verschillende soorten monomeren te vestigen, waaronder hun oorsprong, functionaliteit, structuur, het type polymeer dat ze vormen, hoe ze polymeriseren en hun covalente bindingen vallen op.
Natuurlijke monomeren
- Er zijn monomeren van natuurlijke oorsprong zoals isopreen, dat wordt verkregen uit het sap of latex van planten, en die ook de monomere structuur is van natuurlijk rubber.
- Sommige aminozuren geproduceerd door insecten vormen fibroine of zijde -eiwit. Het zijn ook aminozuren die het keratinepolymeer vormen, het wollen eiwit geproduceerd door dieren zoals schapen.
- Onder de natuurlijke monomeren zijn de fundamentele structurele eenheden van biomoleculen. Het glucosemonosaccharide verbindt bijvoorbeeld andere glucosemoleculen om verschillende soorten koolhydraten zoals zetmeel, glycogeen, cellulose te vormen.
- Aminozuren kunnen daarentegen een breed scala aan polymeren vormen die bekend staat als eiwitten. Dit komt omdat er twintig soorten aminozuren zijn, die in elke willekeurige volgorde kunnen worden gekoppeld; En daarom vormen ze uiteindelijk een of ander eiwit met hun eigen structurele kenmerken.
- De mononucleotiden, die de macromoleculen vormen die respectievelijk nucleïnezuren worden genoemd, zijn ook zeer belangrijke monomeren in deze categorie.
Synthetische monomeren
- Onder de kunstmatige of synthetische monomeren (die talrijk zijn) kunnen sommige worden vermeld waarmee verschillende soorten kunststoffen worden uitgewerkt, zoals vinylchloride, dat het chloride of PVC polyvinil vormt; en ethyleengas (h2C = Ch2), en zijn polyethyleenpolymeer. Het is bekend dat u met deze materialen een breed scala aan containers, flessen, thuisobjecten, speelgoed, bouwmaterialen kunt bouwen, onder andere.
- Het tetrluorethyleenmonomeer (f2C = CF2) vormt het polymeer dat wordt genoemd en commercieel bekend als Teflon.
- Tolueen -afgeleide caprolactam -molecuul is essentieel voor nylon -synthese, onder vele anderen.
- Er zijn verschillende groepen acrylmonomeren die zijn geclassificeerd volgens samenstelling en functie. Onder deze zijn onder andere acrylamide en metacrylamide, acrylaat, acryl met fluor.
Apolar en polaire monomeren
Deze classificatie wordt uitgevoerd volgens het elektronegativiteitsverschil van de atomen die de monomeer vormen. Wanneer er een merkbaar verschil is, worden polaire monomeren gevormd; Polaire aminozuren zoals Treonine en Asparagine bijvoorbeeld.
Wanneer het elektronegativiteitsverschil nul is, zijn monomeren apolair. Er zijn onder andere niet -polaire aminozuren zoals tryptofaan, alanine, Valina; en ook apolaire monomeren zoals vinylacetaat.
Cyclische of lineaire monomeren
Volgens de vorm of organisatie van atomen binnen de structuur van de monomeren kunnen deze worden geclassificeerd als cyclische monomeren, zoals proline- of ethyleenoxide; en lineair of alifatisch, zoals aminozuur valine of ethyleenglycol, onder vele anderen.
Voorbeelden van monomeren
Naast de reeds genoemde, zijn er de volgende aanvullende voorbeelden van monomeren:
- Formaldehyde
- Furfural
- Cardanol
- Galactose
- Rekken
- Polyvinylalcohol
- Isopreen
- Vetzuren
- Epoxiden
- En hoewel ze niet werden genoemd, zijn er monomeren waarvan de structuren niet zijn koolzuurhoudend, maar gesulfuriseerd, gefosforeerd of siliciumatomen hebben.
Referenties
- Carey F. (2006). Organische chemie. (6e. ED.)). Mexico: Mc Graw Hill.
- De redacteuren van Encyclopedia Britannica (2015). Monomeer: chemische verbinding. Uitgebracht van: Britannica.com
- Mathews, Holde en Ahern (2002). Biochemie (3e. ED.)). Madrid: Pearson
- Polymeren en monomeren. Hersteld van: materiaalsworldmodules.borg
- Wikipedia (2018). Monomeer. Genomen van: in.Wikipedia.borg

