Moleculaire zuurstofstructuur, eigenschappen, gebruik
- 3951
- 41
- Cecil Graham
Hij Moleculaire zuurstof of Dioxygen, Ook wel diatomic of gasvormige zuurstof genoemd, het is de meest voorkomende elementaire vorm waarin dit element wordt gevonden op de planeet aarde. De formule is of2, Daarom een diatomee en homonucleair molecuul zijn, volledig apolair.
De lucht die we inademen bestaat uit ongeveer 21% zuurstof als moleculen of2. Hoe meer we stijgen, de concentraties van gaszuurstof nemen af en verhogen de aanwezigheid van ozon, of3. Ons lichaam maakt gebruik van de O2 Om uw weefsels te oxygen en cellulaire ademhaling uit te voeren.
 Zonder zuurstof zou het verrijken van onze sfeer het leven een onhoudbaar fenomeen zijn. Bron: Pixabay.
Zonder zuurstof zou het verrijken van onze sfeer het leven een onhoudbaar fenomeen zijn. Bron: Pixabay. De O2 Hij is ook verantwoordelijk voor het bestaan van vuur: zonder hem zou het bijna onmogelijk zijn om branden en verbrandingen te hebben. Dit komt omdat zijn belangrijkste eigenschap een krachtig oxidatiemiddel moet zijn, elektronen zal winnen of een watermolecuul, of in oxide -anionen, of2-.
Moleculaire zuurstof is essentieel voor talloze aerobe processen, met toepassingen in metallurgie, geneeskunde en afvalwaterbehandeling. Dit gas is praktisch synoniem met warmte, ademhaling, oxidatie en aan de andere kant van bevroren temperaturen wanneer het in zijn vloeibare toestand heeft.
[TOC]
Moleculaire zuurstofstructuur
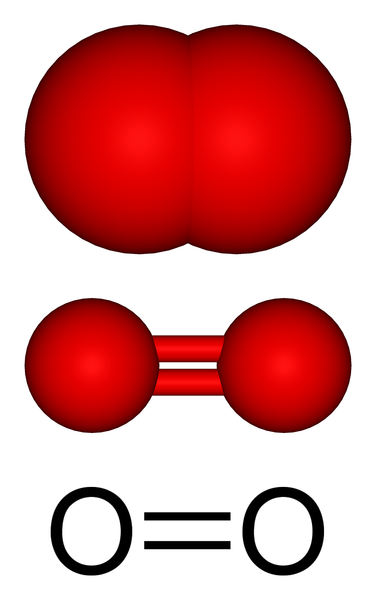
 Gasvormige zuurstofmoleculaire structuur. Bron: Benjah-bmm27 via Wikipedia.
Gasvormige zuurstofmoleculaire structuur. Bron: Benjah-bmm27 via Wikipedia. In het bovenste beeld hebben we de moleculaire structuur van de gasvormige zuurstof weergegeven met verschillende modellen. In de laatste twee worden de kenmerken van de covalente binding die de zuurstofatomen behoudt, bewezen: een dubbele binding o = o, waarin elk zuurstofatoom zijn octet van Valencia voltooit.
Kan u van dienst zijn: diastreomerenHet molecuul of2 Het is lineair, homonucleair en symmetrisch. De dubbele binding heeft een lengte van 121 uur. Deze korte afstand maakt een bepaalde aanzienlijke energie vereist (498 kJ/mol) om de link o = o te verbreken, en is daarom een relatief stabiele molecuul.
Als dat zo is, zou de zuurstof van de atmosfeer in de loop van de tijd volledig zijn afgebroken, anders zou de lucht op niets vatten.
Eigenschappen
Fysiek uiterlijk
Moleculaire zuurstof is een kleurloos, smakeloos en geurloos gas, maar wanneer condensatie en kristallisatie blauwachtige tonen verwerft.
Molaire massa
32 g/mol (afgeronde waarde)
Smeltpunt
-218 ºC
Kookpunt
-183
Oplosbaarheid
Moleculaire zuurstof is niet erg oplosbaar in water, maar genoeg om mariene fauna te ondersteunen. Als uw oplosbaarheid groter zou zijn, zou het minder snel sterven van verdrinking. Aan de andere kant is de oplosbaarheid ervan veel groter in oliën en apolaire vloeistoffen, die ze langzaam kunnen oxideren en dus hun oorspronkelijke eigenschappen kunnen beïnvloeden.
Energy States
Moleculaire zuurstof is een stof die niet volledig kan worden beschreven door Valencia Link Theory (TEV).
De elektronische zuurstofconfiguratie is als volgt:
[Hij] 2s² 2p⁴
Het heeft een paar ontbrekende elektronen (of :). Wanneer twee zuurstofatomen worden gevonden, zijn ze gekoppeld om een dubbele binding o = o te vormen, waardoor beide octet van Valencia wordt voltooid.
Daarom het molecuul of2 Het zou diamagnetisch moeten zijn, met al zijn gepaarde elektronen. Het is echter een paramagnetisch molecuul, en dit wordt verklaard door het diagram van zijn moleculaire orbitalen:
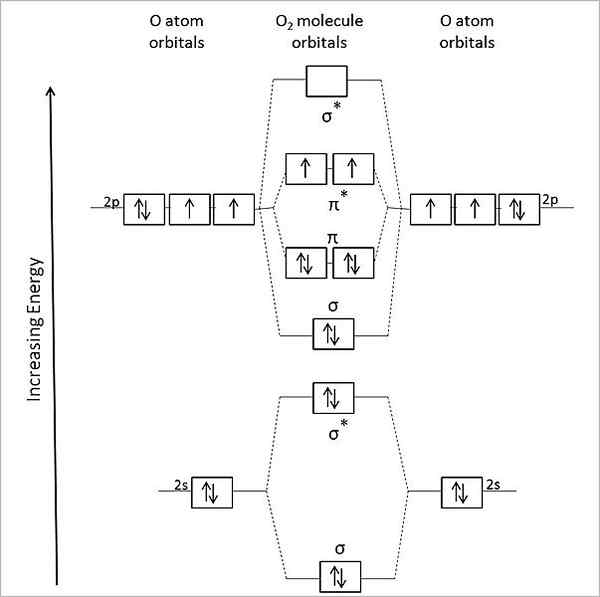 Moleculair orbitaal diagram voor gaszuurstof. Bron: Anthony.Sebastian/cc by-sa (https: // creativeCommons.Org/licenties/by-sa/3.0)
Moleculair orbitaal diagram voor gaszuurstof. Bron: Anthony.Sebastian/cc by-sa (https: // creativeCommons.Org/licenties/by-sa/3.0) Aldus beschrijft de moleculaire orbitale theorie (TOM) beter de OK2. De twee ontbrekende elektronen bevinden zich in de moleculaire orbitalen π*, van grotere energie, en geven zuurstof met hun paramagnetisch karakter.
Kan u dienen: methylamine: structuur, eigenschappen, productie, gebruikIn feite komt deze energietoestand overeen met triplet -zuurstof, 3OF2, De meest overheersende van allemaal. De andere energietoestand van zuurstof, minder overvloedig op aarde, is de single, 1OF2.
Transformaties
Moleculaire zuurstof is aanzienlijk stabiel zolang het niet in contact is met een stof die vatbaar is voor oxideren, veel minder als er geen nauwe bron van intense warmte is, zoals een vonk. Dit komt omdat O2 Het heeft een hoge neiging om te verminderen, elektronen te verkrijgen van andere atomen of moleculen.
Wanneer het wordt verminderd, kan het een breed spectrum van links en vormen vaststellen. Als het covalente bindingen vormt, zal het het doen met minder elektronegatieve atomen dan hij, inclusief waterstof, om water te origineren, h-o-h. Het kan ook koolstofuniversum zijn, om C-O-bindingen en verschillende soorten geoxygeneerde organische moleculen te veroorzaken (Éteres, ketonen, aldehyden, enz.)).
De O2 U kunt ook elektronen krijgen om te transformeren in peroxiden en superoxiden, of22- I2-, respectievelijk. Wanneer het peroxide wordt in het organisme, wordt waterstofperoxide verkregen, h2OF2, H-O-O-H, een schadelijke verbinding die wordt verwerkt door de werking van specifieke enzymen (peroxidasen en catala's).
Aan de andere kant, en niet in het minst, de O2 reageert met anorganisch materiaal om oxide -anion te worden, of2-, Een eindeloze lijst samenstellen van mineralogische massa's die de schors en landmantel opzwellen.
Toepassingen
Lassen en verbranding
 Zuurstof wordt gebruikt om acetyleen te verbranden en een vlam van intense warmte af te vuren die waardevol is in lassen. Bron: Sheila/CC door (https: // creativeCommons.Org/licenties/door/2.0)
Zuurstof wordt gebruikt om acetyleen te verbranden en een vlam van intense warmte af te vuren die waardevol is in lassen. Bron: Sheila/CC door (https: // creativeCommons.Org/licenties/door/2.0) Zuurstof wordt gebruikt om de verbrandingsreactie uit te voeren, waardoor een stof exotherm het vuur afgeeft. Deze brand en de temperatuur variëren afhankelijk van de stof die brandt. Aldus kunnen zeer hete vlammen worden verkregen, zoals acetyleen (hierboven), waarmee metalen en legeringen worden gelast.
Kan je van dienst zijn: enthalpieZonder zuurstof konden brandstoffen niet branden en al hun calorie -energie leveren, gebruikt om raketten af te doen of om auto's te starten.
Oxidatiemiddel in groene chemie
Dankzij dit gas worden een eindeloze organische en anorganische oxiden gesynthetiseerd of industrieel geproduceerd. Deze reacties zijn gebaseerd op het oxiderende vermogen van moleculaire zuurstof, zijn ook een van de meest haalbare reagentia van groene chemie voor het verkrijgen van farmaceutische producten.
Geholpen ademhaling en afvalwaterbehandeling
Zuurstof is van vitaal belang om aan de ademhalingsvraag te voldoen bij patiënten met ernstige gezondheidstoestanden, bij duikers wanneer ze afdalen op lage diepten, en in bergklimmers, op wiens hoogtes de zuurstofconcentratie er dramatisch uitziet.
Evenzo "voedt" de zuurstof -aerobe bacteriën, die het verontreinigende afval van afvalwater helpen afbreken, of helpen om vissen te ademen, in waterige gewassen voor bescherming of handel.
Referenties
- Shiver & Atkins. (2008). Anorganische scheikunde. (vierde druk). MC Graw Hill.
- Wikipedia. (2020). Oxygen allotropen. Opgehaald uit: in.Wikipedia.borg
- Hone, c.NAAR., Kappe, c.OF. (2019). Het gebruik van moleculaire zuurstof voor vloeistoffase aerobe oxidaties in continue stroming. Top Curr Chem (Z)377, 2. doen.org/10.1007/S41061-018-0226-Z
- Kevin Beck. (28 januari 2020). 10 gebruik voor zuurstof. Hersteld van: wetenschap.com
- Cliffsnotes. (2020). Biochemistry I: De chemie van moleculaire zuurstof. Hersteld van: cliffsnotes.com
- GZ industriële benodigdheden. (2020). Industriële voordelen van zuurstofgas. Opgehaald uit: GZ-Supplies.com
- « Cultuur van Portugal -tradities, gebruiken, gastronomie, religie
- Destructieve interferentieformule en vergelijkingen, voorbeelden, oefening »

