Thomson Atomic Model -kenmerken, postulaten, subatomaire deeltjes
- 2702
- 342
- Lonnie Rohan
Hij Thomson Atomic Model Het is gemaakt door de Engelse fysieke gevierde J. J. Thomson, die het elektron ontdekte. Vanwege deze ontdekking en zijn werken over elektrische geleiding in gassen, werd het in 1906 toegekend met de Nobelprijs in de natuurkunde.
Uit zijn werk met de kathodestralen werd onthuld dat het atoom geen ondeelbare entiteit was, zoals Dalton in het voorgaande model had gepostuleerd, maar dat het een goed gedefinieerde interne structuur bevatte.

Thomson ontwikkelde een atoommodel op basis van de resultaten van zijn experimenten met kathodestralen. In hem bevestigde hij dat het atoom, elektrisch neutraal, werd gevormd uit positieve en negatieve ladingen van gelijke magnitude.
[TOC]
Wat was de naam van het atoommodel van Thomson en waarom?
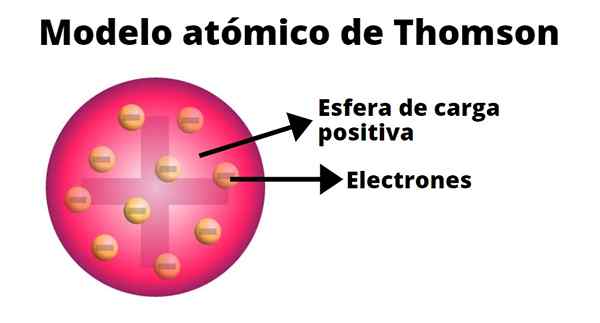
Volgens Thomson werd de positieve belasting verdeeld over het atoom en waren de negatieve ladingen erin ingebed alsof ze de rozijnen van een pudding waren. Uit deze vergelijking ontstond de term "Raisin Pudding", omdat het model informeel bekend was.
 Joseph John Thomson
Joseph John Thomson Hoewel het idee van Thomson momenteel vrij primitief is, vertegenwoordigde hij voor zijn tijd een nieuwe bijdrage. Tijdens de korte validiteit van het model (van 1904 tot 1910) had hij de steun van veel wetenschappers, hoewel vele anderen het als ketterij beschouwden.
Uiteindelijk ontstond in 1910 er nieuw bewijs over de atomaire structuur en bleef het model van Thomson snel opzij. Dit gebeurde zodra Rutherford de resultaten van zijn dispersie -experimenten publiceerde, die het bestaan van de atoomkern aantoonden.
Het model van Thomson was echter de eerste die het bestaan van subatomaire deeltjes postuleerde en hun resultaten waren de vrucht van een fijne en rigoureuze experimenten. Op deze manier vestigde hij het precedent voor alle ontdekkingen die volgden.
Kenmerken en postulaten van het Thomson -model
Thomson arriveerde op zijn atoommodel op basis van verschillende observaties. De eerste was dat de X -Rays nieuw ontdekt door Roentgen in staat waren om luchtmoleculen te ioniseren. Tot die tijd was de enige manier om ionen te ioniseren, ionen chemisch in een oplossing scheiden.
Maar de Engelse natuurkundige ioniseert met succes zelfs monoatomische gassen zoals helium, via x -reeks. Dit bracht hem ertoe te geloven dat de lading in het atoom kon worden gescheiden en dat het daarom niet ondeelbaar was.Hij merkte ook op dat kathodestralen konden worden afgeleid door elektrische en magnetische velden.
 J.J. Thomson, ontdekker van het elektron. Bron: Lafer.
J.J. Thomson, ontdekker van het elektron. Bron: Lafer. Toen bedacht Thomson een model dat correct uitlegde dat het atoom elektrisch neutraal is en dat de kathodestralen zijn samengesteld uit deeltjes met negatieve belasting.
Onderzoeker experimenteel bewijsmateriaal kenmerkte Thomson het atoom als volgt:
-Het atoom is een elektrisch neutrale vaste bol, met een geschatte straal van 10-10 M.
-De positieve belasting wordt min of meer uniform verdeeld door de bol.
-Het atoom bevat "corpuscles" negatief geladen, wat hun neutraliteit waarborgt.
-Deze lorpjes zijn hetzelfde voor alle materie.
-Wanneer het atoom in evenwicht is, is er N lorpjes regelmatig gerangschikt in ringen binnen de positieve laadsfeer.
-De massa van het atoom is uniform verdeeld.
Kathodestralen
 Elektronenstraal worden van de kathode naar de anode gericht.
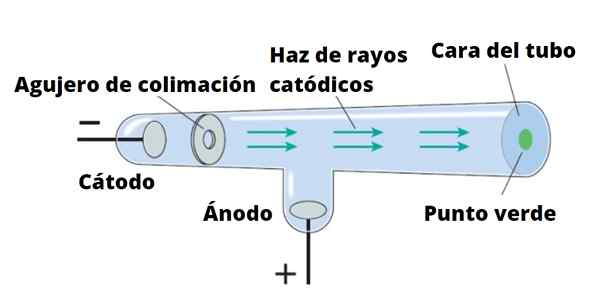
Elektronenstraal worden van de kathode naar de anode gericht. Thomson voerde zijn experimenten uit met behulp van kathodestralen, ontdekt in 1859. Kathodestralen zijn negatief geladen deeltjes. Om ze te produceren, worden vacuümkristalbuizen gebruikt, waarbij twee elektroden worden geplaatst, genoemd kathode En anode.
Kan u van dienst zijn: magnetisme: magnetische eigenschappen van materialen, gebruikVervolgens wordt een elektrische stroom doorgegeven die de kathode verwarmt, die dus onzichtbare straling uitzendt die rechtstreeks naar de tegenoverliggende elektrode wordt gericht.
Om straling te detecteren, wat niets anders is dan kathodestralen, is de buiswand bedekt met een fluorescerend materiaal. Wanneer straling daar komt, geeft de buiswand een intense helderheid af.
Als een solide object wordt geplaatst op het pad van kathodestralen, gooit het een schaduw op de buiswand. Dit geeft aan dat de stralen in een rechte lijn reizen, en ook dat ze ze gemakkelijk kunnen blokkeren.
De aard van de kathodestralen werd breed besproken, omdat de aard ervan een onbekende was. Sommigen dachten dat ze elektromagnetische golven waren, terwijl anderen beweerden dat ze deeltjes waren.
Subatomaire deeltjes van Thomson Atomic Model
Het atoommodel van Thomson is, zoals we zeiden, de eerste om het bestaan van subatomaire deeltjes te postuleren. Thomson's lijkschouwers zijn niets anders dan elektronen, de fundamentele deeltjes van het negatief geladen atoom.
We weten momenteel dat de andere twee fundamentele deeltjes het proton zijn, positief geladen, en het neutron zonder belasting.
Maar deze werden niet ontdekt op het moment dat Thomson zijn model uitwerkte. De positieve lading in het atoom werd erin verdeeld, hield geen rekening met enig deeltje dat de lading droeg en op dit moment was er geen bewijs van het bestaan ervan.
Om deze reden had zijn model een vluchtig bestaan, omdat de dispersie -experimenten van Rutherford in de loop van een paar jaar de weg openden voor de ontdekking van het proton. En wat betreft het neutron, Rutherford zelf stelde zijn bestaan een paar jaar voordat hij uiteindelijk werd ontdekt.
De boerenbuis
Sir William Crookes (1832-1919) ontwierp de buis die zijn naam rond 1870 draagt, met de bedoeling zorgvuldig de aard van kathodestralen te bestuderen. Hij voegde elektrische velden en magnetische velden toe en merkte op dat de stralen door deze werden afgeleid.
 Cathode Ray Tube -schema. Bron: Knight, r.
Cathode Ray Tube -schema. Bron: Knight, r. Op deze manier ontdekten Crookes en andere onderzoekers, waaronder Thomson, dat:
- Een elektrische stroom werd gegenereerd in de kathodestraalbuis
- De stralen werden afgeweken door de aanwezigheid van magnetische velden, op dezelfde manier dat de negatief geladen deeltjes waren.
- Elk metaal dat werd gebruikt om de kathode te produceren was even goed om kathodestralen te produceren, en hun gedrag was onafhankelijk van het materiaal.
Deze observaties voedden de discussie rond de oorsprong van de kathodestralen. Degenen die beweerden dat ze golven waren, waren gebaseerd op het feit dat de kathodestralen in een rechte lijn konden reizen. Bovendien legde deze hypothese heel goed de schaduw uit dat een tussenstopige object op de wand van de buis gooide en onder bepaalde omstandigheden was bekend dat de golven fluorescentie konden veroorzaken.
Maar in plaats daarvan werd het niet begrepen hoe het mogelijk was dat de magnetische velden de kathodestralen afleiden. Dit had alleen verklaring als deze stralen als deeltjes werden beschouwd, een hypothese die Thomson deelde.
Deeltjes geladen in uniforme elektrische en magnetische velden
Een deeltje geladen met Q -belasting, ervaart een geloofskracht in het midden van een uniform elektrisch veld en, van grootte:
Kan u van dienst zijn: golvende lichttheorie: uitleg, toepassingen, voorbeeldenGeloof = qe
Wanneer een geladen deeltje loodrecht een uniform elektrisch veld kruist, zoals dat tussen twee platen met tegengestelde belastingen, ervaart het een afwijking en dus een versnelling:
QE = MA
A = QE/M
Aan de andere kant, als het geladen deeltje beweegt met grootte V -snelheid, in het midden van een uniform magnetisch veld van grootte B, heeft de magnetische kracht FM die ervaart de volgende intensiteit:
FM = QVB
Zolang de snelheids- en magnetische veldvectoren loodrecht zijn. Wanneer een geladen deeltje loodrecht in een homogeen magnetisch veld beïnvloedt, ervaart het ook een afwijking en de beweging ervan is uniform circulair.
Centripetale versnelling totC In dit geval is het:
Qvb = maC
Op zijn beurt is centripetale versnelling gerelateerd aan de snelheid van deeltje V en de straal R van het cirkelvormige traject:
naarC = V2/R
Daarom:
QVB = MV2/R
De straal van het cirkelvormige traject kan als volgt worden berekend:
R = MV/QB
Later zullen deze vergelijkingen worden gebruikt om de manier waarop Thomson de elektronenbelastingsverhouding heeft afgerond, opnieuw te creëren.
Thomson's experiment
Thomson passeerde een straal kathodestralen, een elektronenstraal, hoewel hij het nog steeds niet wist, door uniforme elektrische velden. Deze velden worden gemaakt tussen twee geleidende platen geladen en gescheiden op een kleine afstand.
Kathodestralen gingen ook door een uniform magnetisch veld en observeerden het effect dat dit op de balk had. Zowel op het ene veld als het andere, was er een afbuiging in de stralen, waardoor Thomson terecht werd gedacht dat de balk bestond uit geladen deeltjes.
Om te controleren, voerde Thomson verschillende strategieën uit met de kathodestralen:
- Varieer de elektrische en magnetische velden totdat de krachten werden geannuleerd. Op deze manier gingen de kathodestralen door zonder afbuiging te experimenteren. Bijpassende elektrische en magnetische krachten slaagde Thomson erin om de snelheid van de straaldeeltjes te bepalen.
- De intensiteit van het elektrische veld geannuleerd, op deze manier volgden de deeltjes een cirkelvormig traject in het midden van het magnetische veld.
- Combineerden de resultaten van stappen 1 en 2 om de load-mandy verhouding van de "corpuscles" te bepalen.
De elektronenladingmassa-verhouding
Thomson heeft vastgesteld dat de lading-mandy ratio van de deeltjes die de kathodestralenstraal vormden de volgende waarde heeft:
Q/m = 1.758820 x 10 11 C.kg-1.
Waarbij q de belasting van de "corpuscle" vertegenwoordigt, wat eigenlijk het elektron is en M Het is de massa van hetzelfde. Thomson volgde de procedure die in de vorige sectie is beschreven, die we hier stap voor stap opnieuw creëren, met de vergelijkingen die hij gebruikte.
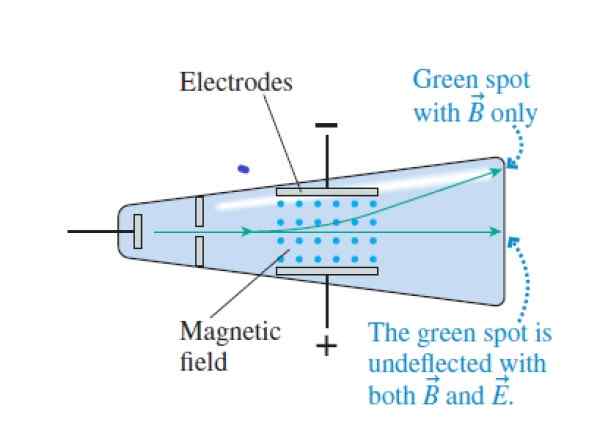 Wanneer de kathodestralen het kruis oversteken en magnetische velden zijn gekruist, passeren ze zonder afbuiging. Wanneer het elektrische veld wordt geannuleerd, beïnvloeden ze de bovenkant van de buis (het magnetische veld wordt aangegeven met de blauwe punten tussen de elektroden). Bron: Knight, r.
Wanneer de kathodestralen het kruis oversteken en magnetische velden zijn gekruist, passeren ze zonder afbuiging. Wanneer het elektrische veld wordt geannuleerd, beïnvloeden ze de bovenkant van de buis (het magnetische veld wordt aangegeven met de blauwe punten tussen de elektroden). Bron: Knight, r. Stap 1
Match elektrische kracht en magnetische kracht, passeer de balk door de loodrechte elektrische en magnetische velden:
QVB = QE
Stap 2
Bepaal de snelheid verkregen door de bundeldeeltjes wanneer ze rechtstreeks zonder afbuiging passeren:
V = E/B
Stap 3
Annuleer het elektrische veld en laat alleen het magnetische veld achter (nu is er afbuiging):
R = MV/QB
Met V = E/B -resultaten:
R = me/qb2
De straal van de baan kan daarom worden gemeten:
Q/m = v/rb
O goed:
Q/m = e/rb2
Volgende stappen
Het volgende dat Thomson deed, was het quotiënt Q/M meten met behulp van kathoden gemaakt van verschillende materialen. Zoals hierboven vermeld, stoten alle metalen kathodestralen uit met identieke kenmerken.
Kan u van dienst zijn: inductieve reactantieToen vergeleek Thomson zijn waarden met die van de Q/M -verhouding van het waterstofion, verkregen door elektrolyse en waarvan de waarde ongeveer 1 x 10 is8 C/kg. Het elektronenbelastingsmasa-quotiënt is ongeveer 1750 keer groter dan waterstofionen.
Daarom hadden de kathodestralen veel grotere belasting, of misschien een massa die veel kleiner is dan het waterstofion. Waterstofion is gewoon een proton, wiens bestaan bekend was tijd na de dispersie -experimenten van Rutherford.
Tegenwoordig is het bekend dat het proton bijna 1800 keer massiever is dan het elektron en met een belasting van gelijke grootte en teken in strijd met die van het elektron.
Een ander belangrijk detail is dat met Thomson's experimenten de elektrische lading van het elektron niet werd bepaald, noch de waarde van zijn massa afzonderlijk. Deze waarden werden bepaald door de experimenten van Millikan, die in 1906 begonnen.
Thomson en Dalton modellen verschillen
Het fundamentele verschil van deze twee modellen is dat Dalton dacht dat het atoom een bol is. In tegenstelling tot Thomson stelde hij het bestaan van positieve of negatieve ladingen niet voor. Voor Dalton was een atoom zo:
 Dalton Atom
Dalton Atom Zoals we eerder hebben gezien, dacht Thomson dat het atoom deelbaar was en wiens structuur wordt gevormd door een positieve bol en elektronen rondom.
Modelstoringen en beperkingen
Destijds slaagde het atoommodel van Thomson erin om het chemische gedrag van stoffen zeer goed uit te leggen. Hij legde ook terecht de fenomenen uit die plaatsvonden in de kathodestraalbuis.
Maar in feite noemde Thomson niet eens zijn "elektronen" -deeltjes, hoewel de term al eerder was bedacht door George Johnstone Stoney. Thomson noemde ze eenvoudigweg "corpuscles".
Hoewel Thomson gebruik maakte van alle kennis die hij op dit moment had, zijn er verschillende belangrijke beperkingen in zijn model, die al snel duidelijk waren:
-De positieve belasting is niet verdeeld over het atoom. De dispersie -experimenten van Rutherford toonden aan dat de positieve belasting van het atoom noodzakelijkerwijs beperkt is tot een klein gebied ervan, dat later bekend werd als de atoomkern.
-Elektronen hebben een specifieke verdeling binnen elk atoom. De elektronen zijn niet uniform verdeeld, zoals de rozijnen van de beroemde boeddijn, maar hebben een dispositie in orbitalen die de volgende modellen hebben aangetoond.
Het is precies de opstelling van elektronen in het atoom waarmee de elementen voor hun kenmerken en eigenschappen in het periodiek systeem kunnen worden georganiseerd. Dit was een belangrijke beperking van het Thomson -model, dat niet kon verklaren hoe het mogelijk was om de elementen op deze manier te bestellen.
-De atoomkern is degene die het grootste deel van het deeg bevat. Thomson's model stelde dat de massa van het atoom uniform was verdeeld binnen. Maar vandaag weten we dat de massa van het atoom praktisch geconcentreerd is in de protonen en neutronen van de kern.
Het is ook belangrijk om te benadrukken dat dit atoommodel niet toestond om het type beweging te leiden dat elektronen binnen de atoom hadden.
Interessante artikelen
Schrödinger atomair model.
Broglie Atomic Model.
Chadwick Atomic Model.
Heisenberg Atomic Model.
Perrin Atomic Model.
Dalton Atomic Model.
Dirac Jordan Atomic Model.
Democritus Atomic Model.
Leucipo -atoommodel.
Bohr Atomic Model.
Sommend Atomic Model.
Huidig atoommodel.
Referenties
- Andriessen, m. 2001. HSC -cursus. Natuurkunde 2. Jacaranda HSC Science.
- Arfken, G. 1984. Universiteitsfysica. Academische pers.
- Ridder, r. 2017. Fysica voor wetenschappers en engineering: een strategiebenadering. Pearson.
- Rex, a. 2011. Fundamentals of Physics. Pearson.
- Wikipedia. Thomson Atomic Model. Hersteld van: het is.Wikipedia.borg.
- « Algemene formule kwadratische vergelijkingen, voorbeelden, oefeningen
- Aomic model van Dirac Jordan -kenmerken en postulaten »

