Gecondenseerde formule wat is en voorbeelden (methaan, ethaan, glucose ...)
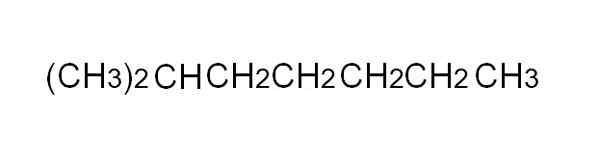
- 4290
- 534
- Aaron Okuneva
De gecondenseerde formule Het is een puur tekstuele weergave van een molecuul waarin de links worden weggelaten. Het doel is om te weten wat het ordenen van atomen is. In het algemeen hebben lineaire of vertakte moleculen gecondenseerde formules, behalve cyclisch of die die sterk vertakt zijn.
In organische chemie is er meestal verwarring van wat het verschil is tussen deze formule en moleculair. Het is in feite gebruikelijk om ze als synoniemen te vinden. Ondertussen worden in anorganische chemie de moleculaire formules meer gebruikt, omdat in de meeste gevallen de covalente verbindingen terecht beschrijven; Zoals water, h2OF.
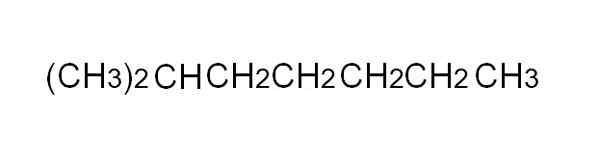 Gecondenseerde formule van 2-methylheptano. Bron: Gabriel Bolívar.
Gecondenseerde formule van 2-methylheptano. Bron: Gabriel Bolívar. [TOC]
Wat is de gecondenseerde formule?
Om het gemakkelijker te definiëren, is de gecondenseerde formule een vereenvoudigde weergave van de semi -ontwikkelde. Het is niet nodig om de eenvoudige links te schrijven, noch moet het meer dan één regel in een tekst behandelen. De 2-methylheptano, een vertakt alkaan, kan bijvoorbeeld worden weergegeven in dezelfde lijn als in de bovenste afbeelding.
Gecondenseerde formules zijn nuttig om sommige moleculen weer te geven zonder ze te hoeven tekenen. Dit is uitstekend wanneer chemische vergelijkingen worden geschreven waar cyclische of zeer vertakte moleculen niet deelnemen. Men zal zien dat deze formules hun toevlucht nemen tot haakjes om de weergave van een molecuul verder te vereenvoudigen.
Voorbeelden
Methaan
Methaan is de enige chemische verbinding die een enkele formule heeft: CH4. Dit komt overeen met het empirische, moleculaire, gecondenseerde en semi -ontwikkeld tegelijkertijd. Dat is de reden waarom mensen vaak, om een verwarring tussen al deze concepten te besparen, liever eenvoudig en onnauwkeurig verwijzen naar de 'chemische formule' van een compound.
Etano
Estano heeft een moleculaire formule C2H6. De gecondenseerde formule is in plaats daarvan cho3Ch3. Merk op dat de C-C-link en C-H-links zijn weggelaten. Het idee is om de formule te kunnen schrijven alsof het een "woord" is, zonder strepen te hoeven tekenen of structuren te tekenen.
Kan u van dienst zijn: pycnometerPer definitie is de moleculaire formule c2H6 En niet ch3Ch3; Voor eenvoudige moleculen zijn beide formules echter gebruikelijk om uit te wisselen, hoewel het nog steeds onjuist is. Dit is een discrepantiepunt tussen verschillende bronnen, waar blijkbaar specifieke regels in dit opzicht zijn.
Glucose en fructose
Hier is een voorbeeld waarbij een fout onmiddellijk wordt waargenomen wanneer u de moleculaire formule voor het condensaat wilt uitwisselen.
Het zoete, glucose- en fructosekoppel hebben dezelfde moleculaire formule: C6H12OF6, En daarom dient dit niet om ze te onderscheiden. Structurele en semi -ontwikkelde formules daarentegen vestigen verschillende moleculen in het zicht.
Glucose of fructose hebben echter een gecondenseerde formule. Dit komt omdat, ongeacht hun weergave of projectie, hun structuren niet in dezelfde lijn kunnen worden geschreven; of tenminste, op een manier die aangenaam en eenvoudig is in de ogen van de lezer.
Butaan
Butano heeft een moleculaire formule C4H10. Het heeft twee isomeren: de lineaire, N-Butano, en vertakt 2-methylpropaan. Beide kunnen worden weergegeven door hun gecondenseerde formules. Hij N-Butano is ch3Ch2Ch2Ch3 of ch3(Ch2))2Ch3, En het 2-methylpropaan is cho3CH (Ch3))2 of (ch3))3Ch.
In het 2-methylpropaan hebben we een groep CH omringd door drie cho3. De twee formules zijn geldig en haakjes worden gebruikt om de vertakkingen te benadrukken, waarbij het abonnement een indicator is van hoeveel groepen deze tak vormen.
Ethanol
Ethanol heeft een gecondenseerde formule ch3Ch2Oh. Merk op hoeveel het lijkt op zijn semi -ontwikkelde formule: CH3-Ch2-Oh. Op dezelfde manier wordt het gedaan met propanol, cho3Ch2Ch2Oh, de N-Butanol, ch3Ch2Ch2Ch2Oh, en met alle andere alcoholen.
Kan u dienen: natriumfosfaat: structuur, eigenschappen, synthese, gebruikAls ze een tak hebben, wordt deze binnen een haakjes aan de rechterkant van het atoom waarmee het is gekoppeld, worden aangegeven. De 2-methylbutanol kan bijvoorbeeld worden geschreven als: ch3Ch2CH (Ch3) Ch2Oh. Merk op dat het voor veel moleculen gemakkelijker begint te zijn om hun toevlucht te nemen tot een structurele of semi -ontwikkelde formule.
Pentano
De lineaire isomeer van de pentan, N-Pentano, het is gemakkelijk te vertegenwoordigen vanwege zijn gecondenseerde formule: Cho3Ch2Ch2Ch2Ch3. Deze formule kan ook worden vereenvoudigd met haakjes: ch3(Ch2))3Ch3, wat aangeeft dat tussen de twee ch3 Er zijn drie ch2.
De andere twee isomeren van de Pentan zijn echter een beetje ingewikkelder: Ch3Ch2CH (Ch3))2, Voor de 2-methylbutaan en C (CH3))4 Voor 2.2-dimethylpropaan of neopantum. Merk op dat het koolstofatoom links van de haakjes is die links vormt naar substituenten of gevolgen.
Octaan
Het lineaire isomeer van het octaan, N-Octaan, vanwege zijn lengte, is het nu gepast om zijn gecondenseerde formule als cho te vertegenwoordigen3(Ch2))6Ch3. Het is op dit punt waar iets vrij van gecondenseerde formules zou moeten zijn: ze proberen tijd te besparen bij het vertegenwoordigen van moleculen of verbindingen, zonder zoveel op papier te schrijven.
Cyclohexan
Het geval van de cyclohexan is vergelijkbaar met die van glucose en fructose: mist formeel een gecondenseerde formule als een cyclische verbinding. Een manier om te proberen het te vertegenwoordigen zou zijn: (ch2))6, wat impliceert dat zes groepen cho2 Ze moeten worden gekoppeld, alleen mogelijk zijn als ze sluiten in een zeshoekige ring. Het is echter beter om de ring te tekenen.
Aceton
Aceton presenteert de eigenaardigheid om een carbonylgroep te bezitten, C = O. Daarom hebben we om uw gecondenseerde formule te schrijven drie opties: (Ch3))2CO, Ch3C (O) CH3 of ch3(C = o) ch3.
Kan u serveren: koffiezuur: structuur, eigenschappen, biosynthese, gebruikIn feite wordt in grotere moleculen de carbonylgroep meestal weergegeven als (o), rekening houdend met dat het koolstofatoom links is die de dubbele binding vormt met zuurstof, c = o.
Azijnzuur
De gecondenseerde formule van azijnzuur is cho3COOH O CH3CO2H. Hier is een belangrijk punt: de functionele groepen die in dezelfde lijn zijn geschreven, zijn delen van een gecondenseerde formule. Dit was het geval van ethanol en aceton, en is ook van toepassing op thiolen (-sh), aldehydos (-cho) de esters (-co2R o -coor) en amines (-nh2)).
Algemene opmerking
Er zijn veel verwarring tussen moleculaire en gecondenseerde formules. Misschien is het omdat deze representaties alleen al een geschat beeld van het molecuul bieden, dus we denken dat het de moleculaire formule is.
Ook formules zoals C6H12OF6 Ze worden ook beschouwd als condensaat, omdat ze worden vereenvoudigd, "condenseren" het molecuul in atomen en subscripts. Daarom is het gebruikelijk om te zien hoe de twee formules worden vermeld alsof ze synoniemen zijn.
In veel bronnen, waaronder Wikipedia -artikelen, worden de termen 'chemische formule' gebruikt om te verwijzen naar moleculair (type C6H12OF6 en anderen), en 'formule' om naar het condensaat te verwijzen.
Referenties
- Whitten, Davis, Peck & Stanley. (2008). Scheikunde. (8e ed.)). Cengage leren.
- Helmestine, Anne Marie, pH.D. (18 november 2019). Gecondenseerde formuledefinitie in chemie. Hersteld van: Thoughtco.com
- James Ashenhurst. (11 december 2019). Condenseerde formules: ontcijferen wat de ruggen betekenen. Master Organic Chemistry. Hersteld van: MasterGanicChemistry.com
- Copolingenieria. (2 mei 2016). Empirische, structurele en condensate formule. Opgehaald uit: chemiotecablog.WordPress.com
- Inleiding tot chemie: algemeen, organisch en biologisch. (S.F.)). Gecondenseerde structurele en lijnhoekformules. Hersteld van: 2012 boeken.Lardbucket.borg

