Aluminium fosfaat (ALPO4) structuur, eigenschappen, verkrijgen, gebruik

- 4388
- 8
- Nathan Wiegand
Hij Aluminium fosfaat Het is een anorganische vaste stof gevormd door een aluminium ion aan de3+ en een fosfaat -ion po43-. De chemische formule is alpo4. Het is een witte vaste stof waarvan de kristallijne structuur vergelijkbaar is met die van silica Sio2. Het is onoplosbaar in water.
Het kan worden verkregen uit aluminiumoxide (tot2OF3) en fosforzuur (h3Po4)). Het kan ook worden verkregen op basis van waterige aluminiumchloride -oplossingen (ALCL3) en natriumfosfaat (NA3Po4)).
 Alpo aluminium fosfaat4. Ondřej Mangl [Public Domain]. Bron: Wikimedia Commons.
Alpo aluminium fosfaat4. Ondřej Mangl [Public Domain]. Bron: Wikimedia Commons. Aluminiumfosfaat heeft een zeer hoog fusiepunt, dus het wordt veel gebruikt als een component van vuurvast keramiek, dat wil zeggen keramiek die zeer hoge temperaturen doorstaan.
Het wordt ook gebruikt als een antacida voor de maag, in mengsels voor het repareren van de tanden en als een adjuvans van vaccins, dat wil zeggen de immuunrespons van het organisme stimuleren.
Sommige vuurvast beton hebben ALPO4 In zijn samenstelling, die de mechanische en ondersteuningseigenschappen van hoge temperaturen van dit type cement verhoogt.
Het is gebruikt als een beschermend schild om brandbare materialen als bepaalde polymeren te voorkomen.
[TOC]
Structuur
De alpo4 Het wordt gevormd door een aluminium kation aan de3+ en een fosfaatanion po43-.
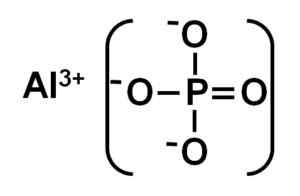 Ionische structuur van aluminium fosfaat. Auteur: Marilú Stea.
Ionische structuur van aluminium fosfaat. Auteur: Marilú Stea. Kristallijn aluminiumfosfaat wordt ook wel Berlinite of alfasfase genoemd (α-Alpo4) en de kristallen zijn vergelijkbaar met kwarts.
 Synthetische Berliniet-kristallen (α-Alpo4)). Dmgualtieri [cc by-sa (https: // creativeCommons.Org/licenties/by-sa/3.0)]. Bron: Wikimedia Commons.
Synthetische Berliniet-kristallen (α-Alpo4)). Dmgualtieri [cc by-sa (https: // creativeCommons.Org/licenties/by-sa/3.0)]. Bron: Wikimedia Commons. De alfase fase van aluminiumfosfaat is een vaste stof gevormd door een covalent netwerk van Po Tetrahedra4 en Alpo4 die afwisselen en worden verenigd door zuurstofatomen.
Deze structuur is isomorf met silica, dat wil zeggen, het heeft dezelfde vorm als die van de SIO2.
Nomenclatuur
- Aluminium fosfaat
- Aluminium monofosfaat
- Fosforzuur aluminium zout.
Eigenschappen
Fysieke staat
Kristallijne witte vaste stof.
Molecuulgewicht
121,93 g/mol
Smeltpunt
1800 ºC
Dikte
2,56 g/cm3
Oplosbaarheid
Onoplosbaar in water
Andere eigenschappen
De Alpo -structuur4 Het lijkt erg op dat van het Sio Silica2, Dus het deelt hiervan veel fysische en chemische eigenschappen.
Kan u van dienst zijn: gedisioneerd waterAluminiumfosfaat is een zeer vuurvast materiaal, dat wil zeggen dat het een zeer hoge temperaturen is zonder de fysieke conditie of de structuur te veranderen en zonder ontbinden.
De alpo4 Kristallijn of beriniet wanneer het wordt verwarmd, wordt het een structuur van het thundimiet type en vervolgens het type Christobalite, andere vormen van deze verbinding die er op het silica -sio lijken2.
 Aluminium fosfaat. ChemicalInterest [Public Domain]. Bron: Wikimedia Commons.
Aluminium fosfaat. ChemicalInterest [Public Domain]. Bron: Wikimedia Commons. Het verkrijgen van
Alpo aluminium fosfaat4 Het kan worden verkregen door reactie tussen fosforzuur h3Po4 en aluminiumoxide2OF3. Temperatuurtoepassing is vereist, bijvoorbeeld tussen 100 en 150 ° C.
Naar de2OF3 + 2 H3Po4 = 2 Alpo4 + 3 H2OF
Het kan ook worden verkregen door een waterige oplossing van aluminiumchloride alcl te verbinden3 met een waterige oplossing van natriumfosfaat na3Po4:
Alcl3 + NA3Po4 = Alpo4 + 3 NaCl
Gebruik in keramiek
Alpo aluminium fosfaat4 Het wordt vaak gevonden in de samenstelling van aluminiumkeramiek.
Keramiek met een hoog aluminiumoxide -gehalte is een van de materialen die wordt gebruikt in toepassingen waarin het nodig is om hoge belastingen en ernstige omstandigheden te weerstaan.
Dit type keramiek is corrosiebestendig, met hoge temperatuuromgevingen, voor de aanwezigheid van hete stoom of bij het verminderen van atmosferen zoals koolmonoxide (CO).
Alumina -keramiek heeft ook een lage elektrische en thermische geleidbaarheid, dus het wordt gebruikt om refractaire bakstenen en isolerende componenten van elektriciteit te maken.
 Refractaire bakstenen coating die alpoo aluminium fosfaat kan bevatten4. Deze stenen beschermen tegen hoge temperaturen. Alexknight12 [CC BY-SA (https: // creativeCommons.Org/licenties/by-sa/3.0)]. Bron: Wikimedia Commons.
Refractaire bakstenen coating die alpoo aluminium fosfaat kan bevatten4. Deze stenen beschermen tegen hoge temperaturen. Alexknight12 [CC BY-SA (https: // creativeCommons.Org/licenties/by-sa/3.0)]. Bron: Wikimedia Commons. Omdat aluminiumfosfaat wordt gevormd bij een veel lagere temperatuur dan Sio Silica2, De productie is goedkoper, wat een voordeel vormt bij de productie van keramiek die geschikt is voor veeleisende diensten.
Aluminium fosfaat keramische productie
Alumina is gewend2OF3 en fosforzuur h3Po4 In waterig medium.
De voorkeursvorming pH is 2-8, omdat er een overvloed is van opgeloste fosforzuursoorten, zoals h2Po4- en HPO42-. Een zure ionenconcentratie bij3+ Het is hoog, van de ontbinding van aluminiumoxide tot de2OF3.
Kan u van dienst zijn: koolstoftetrachloride (CCL4)In de eerste plaats een alh -gehydrateerde aluminium diphardrogen Trihydrogen -gel3(PO4))2.H2OF:
Naar de3+ + H2Po4- + HPO42- + H2Of ⇔ alh3(PO4))3.H2OF
Er komt echter een tijd dat de pH van de lage oplossing wordt en neutraal wordt, waarbij aluminiumoxide naar de2OF3 presenteert een lage oplosbaarheid. Op dit moment vormt de onoplosbare aluminiumoxide een laag op het oppervlak van de deeltjes die voorkomen dat de reactie doorgaat.
Daarom is het noodzakelijk om de oplosbaarheid van aluminiumoxide te verhogen en dit wordt soepel bereikt. Door op 150 ° C te verwarmen, zet de gel de reactie voort met aluminiumoxide naar de2OF3 Water vrijgeven en de kristallijne Berlinita vormt (Alpha-Alpo4)).
Naar de2OF3 + 2 Alh3(PO4))3.H2O → Alpo4 + 4 H2OF
Berlinita sluit zich aan bij individuele deeltjes en keramiek wordt gevormd.
Andere gebruiken
De alpo4 Het wordt gebruikt als een antacida, als een adsorbens, als een moleculaire zeef, zoals katalysatorondersteuning en als een coating om de weerstand van hete corrosieresistentie te verbeteren. Hier zijn andere toepassingen.
Bij het verkrijgen van beton
Aluminiumfosfaat is een ingrediënt van warmte -resistent vuurvast of beton.
Biedt uitstekende mechanische eigenschappen en refractanten aan dit beton, zoals hittebestendigheid. In het temperatuurinterval tussen 1400-1600 ° C is het cellulaire beton op basis van aluminiumfosfaat een van de meest efficiënte materialen zoals thermische isolator.
Het vereist niet drogen, de verharding wordt bereikt door een exotherme reactie zelf gepropageerd. Het is mogelijk om bakstenen van dit materiaal in elke vorm en grootte voor te bereiden.
In tandheelkundige cement
Aluminiumfosfaat maakt deel uit van tandheelkundige of materiële cement die worden gebruikt om het verzorgde prothese te genezen.
In tandcement wordt aluminiumoxide gebruikt als een moderator van zuurbasisreacties, waarbij het modererende effect te wijten is aan de vorming van aluminiumfosfaat op de deeltjes van andere materialen.
Deze cementen hebben een zeer hoge compressie- en spanningsweerstand, wat te wijten is aan de aanwezigheid van aluminiumfosfaat.
 Tandheelkundige cementen die worden gebruikt om cariës te genezen, kunnen aluminiumfosfaat bevatten. Auteur: Gerber Challenge. Bron: Pixabay.
Tandheelkundige cementen die worden gebruikt om cariës te genezen, kunnen aluminiumfosfaat bevatten. Auteur: Gerber Challenge. Bron: Pixabay. In vaccins
De alpo4 Het wordt al vele jaren gebruikt in verschillende menselijke vaccins om de immuunrespons van het lichaam te verbeteren. Er wordt gezegd dat Alpo4 Het is een "adjuvans" van vaccins. Het mechanisme wordt nog niet begrepen.
Kan u van dienst zijn: lithiumchloride (licl): eigenschappen, risico's en gebruikHet is bekend dat het immunostimulerende effect van Alpo4 Het hangt af van het adsorptieproces van het antigeen tegen het adjuvans, dat wil zeggen de manier waarop het zich hieraan houdt. Een antigeen is een verbinding dat bij het binnendringen van het lichaam de vorming van antilichamen genereert om een specifieke ziekte te bestrijden.
Antigenen kunnen worden geadsorbeerd naar Alpo4 door elektrostatische interacties of door de binding met liganden. Adsorb op het oppervlak van het adjuvans.
Er wordt ook aangenomen dat de grootte van de Alpo -deeltjes4 Het heeft ook invloed. Een lagere deeltjesgrootte De antilichaamrespons is groter en duurzamer.
 Vaccins kunnen alpoo aluminium fosfaat bevatten4 Om de effectiviteit ervan te vergroten. Auteur: Tumisu. Bron: Pixabay.
Vaccins kunnen alpoo aluminium fosfaat bevatten4 Om de effectiviteit ervan te vergroten. Auteur: Tumisu. Bron: Pixabay. Als een polymeervlam achterlijk
De alpo4 Het is gebruikt als ontstekingsgebied en vermijd verbranding of verbrand van bepaalde polymeren.
De toevoeging van Alpo4 Voor een polypropyleenpolymeer dat al een vlamvertrager heeft, veroorzaakt een synergetisch effect tussen beide achterlijken, wat betekent dat het effect veel groter is dan dat van beide door afzonderlijke.
Wanneer het polymeer wordt onderworpen aan verbranding of verbrand in aanwezigheid van Alpo4, Er wordt een aluminiummetafosfaat gevormd dat het gecarboniseerde oppervlak doordringt en de poriën en scheuren hiervan vult.
Dit leidt tot de vorming van een zeer efficiënt beschermend schild om het verbranden of verbranding van het polymeer te voorkomen. Met andere woorden de Alpo4 Sluit het gecarboniseerde oppervlak af en voorkomt dat het polymeer verbrandt.
 Met de Alpo4 De verbranding van bepaalde polymeren kan worden vertraagd. Auteur: Hans Braxmeier. Bron: Pixabay.
Met de Alpo4 De verbranding van bepaalde polymeren kan worden vertraagd. Auteur: Hans Braxmeier. Bron: Pixabay. Referenties
- Abyzov, V.NAAR. (2016). Lichtgewicht vuurvast beton op basis van aluminium-magnesium-fosfaatbinder. Procedure Engineering 150 (2016) 1440-1445. Hersteld van Scientedirect.com.
- Wagh, a.S. (2016). Aluminium fosfaat keramiek. In chemisch gebonden fosfaat keramiek (tweede editie). Hoofdstuk 11. Hersteld van Scientedirect.com.
- Mei, c. et al. (2019). Aluminium fosfaatvaccin attjuvant: analyse van samenstelling en grootte van offline en in-line tools gebruiken. Comput struct biotechnol j. 2019; 17: 1184-1194. NCBI hersteld.NLM.NIH.Gov.
- Qin, Z. et al. (2019). Synergistisch barrière -effect van aluminiumfosfaat op vlamvertragende polypropyleen op basis van ammoniumpolyfosfaat/dipentaerythitol -systeem. Materialen en ontwerp 181 (2019) 107913. Hersteld van Scientedirect.com.
- Vrieling, h. et al. (2019). Gestabiliseerde aluminium fosfaat nanapartikelen die worden gebruikt als vaccin atjuvant. Colloïden en oppervlakken B: BioInterfaces 181 (2019) 648-656. Hersteld van Scientedirect.com.
- Schaefer, c. (2007). Gastro -intestinale geneesmiddelen. Antacida. In drugs tijdens zwangerschap en lactatie (tweede editie). Hersteld van Scientedirect.com.
- Rouquerol, f. et al. (1999). Eigenschappen van SOM nieuwe adsorbentia. In adsorptie door powerders en poreuze vaste stoffen. Hersteld van Scientedirect.com.
- « Notatie ontwikkeld wat is, voorbeelden en oefeningen
- Afro -colombia oorsprong, geschiedenis, kenmerken, belang »

