Foundation -elektroforese, techniek, waar is het voor, voorbeelden

- 987
- 32
- Kurt Aufderhar Jr.
De Elektroforese Het is een techniek die wordt gebruikt om moleculen in een elektrisch veld te scheiden. Het moet, met name, met de migratie van deeltjes geladen onder invloed van een elektrische stroom die wordt toegepast tussen twee polen, een positief en een ander negatief.
Elektroforese is momenteel een van de meest routinematige procedures die plaatsvinden tijdens de ontwikkeling van een experiment, vooral op gebieden die verband houden met analytische chemie, biochemie en biologische en medische wetenschappen in het algemeen.
 Elektroforese emmer. Bron: Melodygar/CC BY-SA (https: // creativeCommons.Org/licenties/by-sa/4.0)
Elektroforese emmer. Bron: Melodygar/CC BY-SA (https: // creativeCommons.Org/licenties/by-sa/4.0) Het wordt gebruikt om eiwitten, peptiden, DNA, RNA en anderen te scheiden volgens hun belasting, grootte, dichtheid en zuiverheid.
De verschillende commerciële huizen hebben verschillende formaten ontworpen, met verschillende toepassingen en geschikte winst voor specifieke doeleinden, maar alle procedures vereisen dezelfde basiselementen:
- Een energiebron om elektrische lading te genereren
- Een medium van steun voor scheiding
- Een bufferoplossing (buffer) Om de pH constant te houden
[TOC]
Basis
Elektroforese is niets meer dan de migratie (scheiding) van deeltjes of geladen moleculen (natuurlijk of kunstmatig) in een medium of ondersteuning onder invloed van een elektrisch veld.
De techniek is gebaseerd op een van de belangrijkste fysieke vergelijkingen van elektromagnetisme, volgens welke de kracht gelijk is aan de elektrische lading vermenigvuldigd met het elektrische veld dat op dat punt wordt toegepast (F (Force) = Q (elektrische lading) x E (elektrisch veld )).
Volgens deze vergelijking zullen twee deeltjes met dezelfde massa, maar van verschillende belasting, naar verschillende snelheden in hetzelfde elektrische veld gaan. Bovendien zal de bewegingssnelheid van deze deeltjes afhangen van de relatie tussen hun belasting en hun massa.
Wetenschappers hebben gebruik gemaakt van deze eigenschappen en vracht-/massaberelaties om de componenten van biomoleculen in hun kleinste delen te scheiden, en om verschillende moleculen in een mengsel te scheiden, onder andere toepassingen.
Het is belangrijk om te onthouden dat biologische moleculen zoals aminozuren, peptiden, eiwitten, sommige koolhydraten, nucleotiden en nucleïnezuren allemaal iets hebben dat we "ioniseerbare groepen" noemen, zodat ze kunnen bestaan als positieve of negatief geladen soorten onder bepaalde omstandigheden van pH.
Techniek
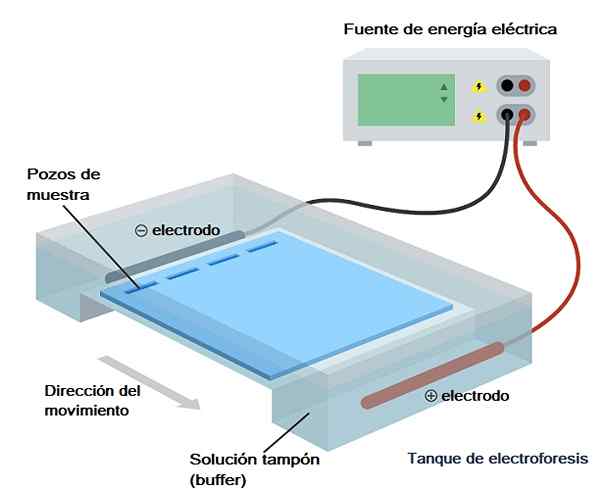
Hoewel er verschillende soorten elektroforese zijn, is gelelektroforese het meest gebruikt in biochemische analyse, moleculaire biologie en biotechnologie, dus het zal zijn waar we in technische termen kort over zullen praten.
Zoals de naam al aangeeft, impliceert gelelektroforese het gebruik van een vaste vaste stofhulpmedium, hetzij voor de analyse/scheiding van mengsels van eiwitten of nucleïnezuren (DNA en/of RNA) onder invloed van een elektrisch veld.
Het systeem of apparaat dat wordt gebruikt om een elektroforetische "run" uit te voeren, kan horizontaal zijn (meestal gebruikt voor nucleïnezuren) of verticaal (meestal gebruikt voor eiwitten).
- Voorbeeld van de techniek van nucleïnezuurelektroforese -techniek
Nucleïnezuren worden meestal gescheiden met behulp van agarosegels (galactosepolysacharide) die wordt bereid met een adequate bufferoplossing (Tris/Acetaat/EDTA of Tris/Borato/EDTA) en wiens concentratie de "resolutie" van fragmenten van verschillende afmetingen zal bepalen.
Kan u van dienst zijn: Earth's Food Chain: Links en voorbeeldMonsterbereiding
De eerste stap voor het uitvoeren van een elektroforetische run in een agarosegel is het verkrijgen van het monster. Dit hangt af van het experimentele uiteinde en de monsters kunnen het product zijn van een enzymatische spijsvertering, van een polymerasekettingreactie (PCR), een zuivering van nucleïnezuren, enz.
 Mix van het monster met de laadfanaat.Org/licenties/door/4.0) Via Wikimedia Commons)
Mix van het monster met de laadfanaat.Org/licenties/door/4.0) Via Wikimedia Commons) Na het verkrijgen wordt dit gemengd met een gekleurde oplossing (laadoplossing) die de snelle afzetting van het monster in een put mogelijk maakt, omdat het glycerol en een kleurstof heeft die de run visueel mogelijk maakt.
Gelbreiding
Deze stap bestaat uit het mengen van de noodzakelijke hoeveelheid geleersubstraat (de agarose) met de bufferoplossing, het smelten met warmte en het stollen van een ondersteuning die functioneert als "schimmel".
Tijdens de gelificatie worden sommige "kammen" geïntroduceerd in de gel geplaatst in de "mal" om de "putten" af te bakenen waar de monsters vóór de run worden geïntroduceerd.
Zodra de gel is afgekoeld en gestold, worden de "kammen" verwijderd en wordt deze geïntroduceerd in een container die bekend staat als "Bucket", die vol zit met lopende bufferoplossing (Tris/Acetate/EDTA of Tris/Borato/Borato/EDTA).
Deze emmer is op zijn beurt opgenomen in wat de "elektroforetische kamer" wordt genoemd, die niets meer is dan de container waardoor het elektrische veld wordt doorgegeven en die een ruimte heeft waar de gel wordt geïntroduceerd en twee secties waarmee ze zijn gevuld met buffer oplossing (buffer loop).
Deze camera heeft twee elektroden, één positief en één negatief, waaronder de ionenbeweging wordt geproduceerd na de toepassing van een elektrisch veld (deze is verbonden met een stroombron).
Laadmonsters
Zodra de monsters zijn gemengd met de respectieve belastingsoplossing, worden deze geïntroduceerd in de "putten" die eerder in de gel zijn gemaakt.
Omdat nucleïnezuren een negatieve netto belasting hebben, migreren ze van de negatieve pool naar het positieve, dus hier moet rekening mee worden gehouden wanneer de camera is aangesloten op de stroombron, zodat de negatieve pool overeenkomt met de meest plaats naast de plaats waar de monsters werden geladen.
Corrida -tijd wordt vastgesteld in strikte afhankelijkheid van de onderzoeker die verantwoordelijk is voor het experiment. De spanning wordt in het algemeen berekend in een 5 volt -verhouding per centimeter in de gel die de twee elektroden scheidt.
Weergave
Wanneer de gel loopt (wanneer de monsters de gel van het ene uiteinde naar het andere hebben gereisd), is deze ondergedompeld in een oplossing van ethide bromide (ETBR), een kleurstof die wordt afgewisseld tussen de stikstofbases en dat het "merk", dus Ze kunnen worden gevisualiseerd in een transilumenant met behulp van ultraviolet licht.
Waar is elektroforese voor?
Elektroforese is van oudsher gebruikt met meerdere doeleinden. Tegenwoordig hangt het nut ervan echter grotendeels af van de 'vraag' die de onderzoeker wordt gesteld in relatie tot een fenomeen of een bepaald systeem, evenals het type elektroforese dat hij wenst te gebruiken.
Kan u van dienst zijn: topoisomerase: wat zijn, kenmerken, functies, typenWe kunnen echter enkele van de belangrijkste functies inschakelen die deze techniek heeft, beginnend met de meest "zeldzame" en eindigend door de meest populaire en meestal uitgebuit in de wereld van de biologische wetenschappen. Elektroforese is nuttig:
- Voor de kwantitatieve analyse van complexe mengsels van macromoleculen en voor de berekening van de potentiële "zeta" (colloïdale eigenschap van een deeltje in een vloeibaar medium onder invloed van een statisch elektrisch veld).
- Voor de analyse van bloedsera voor diagnostische doeleinden.
- Voor de scheiding van glucoproteïnen, lipoproteïnen en bloedhemoglobine.
- Voor voedselanalyse, farmaceutische producten en milieuverontreinigende stoffen.
Elektroforese in agarosegels
- Voor de scheiding van DNA -fragmenten na spijsvertering met restrictie -enzymen.
- Voor de scheiding van nucleïnezuurmoleculen vóór overdracht naar membranen voor latere analyses.
- Voor de analyse van PCR -producten (polymerasekettingreactie) verifiëren of deze al dan niet heeft plaatsgevonden.
- Voor de schatting van de grootte van de moleculen in een mengsel van DNA of RNA.
- Voor de schatting van de hoeveelheid en/of de kwaliteit van gezuiverde nucleïnezuren.
Elektroforese in polyacrylamidegels onder denaturaliserende of inheemse omstandigheden
- Om de grootte van een eiwit te bepalen.
- Om eiwitten te identificeren.
- Om de zuiverheid van een monster te bepalen na verschillende zuiveringsstappen.
- Om de aanwezigheid van intramoleculaire disulfidekinks te identificeren.
- Om de interactie tussen eiwitten te bepalen.
- Om het iso -elektrische punt van een eiwit te bepalen.
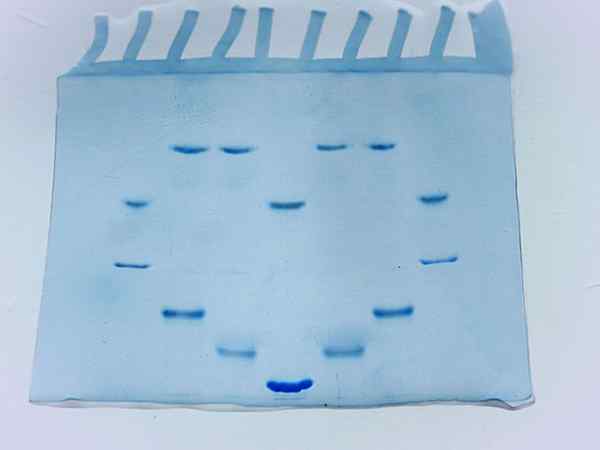 Fotografie van een acrylamidegel na de run van verschillende eiwitmonsters (Bron: Larionova.Marina/CC BY-SA (https: // creativeCommons.Org/licenties/by-sa/4.0) Via Wikimedia Commons)
Fotografie van een acrylamidegel na de run van verschillende eiwitmonsters (Bron: Larionova.Marina/CC BY-SA (https: // creativeCommons.Org/licenties/by-sa/4.0) Via Wikimedia Commons) Factoren die de elektroforese beïnvloeden
De migratie van een deeltje in een elektrisch veld hangt af van verschillende factoren, waaronder:
- Uw elektrische lading
- Zijn moleculaire grootte
- Zijn hydrofobiciteit en zijn vorm
- De grootte van het elektrische veld dat wordt toegepast
- De systeemtemperatuur en ionenkracht van de gebruikte bufferoplossing
- De aard van de omgeving waar het zich bevindt
In relatie tot het monster
Onder de parameters met betrekking tot deeltjes (monster) die onderworpen zijn aan een elektrisch veld, hebben de belangrijkste factoren die dit proces beïnvloeden te maken met hun belasting, hun grootte en vorm.
Hoe groter de netto belasting van een deeltje, hoe groter de migratiesnelheid en deze grootte zal afhangen van de pH. De relatie met de grootte is echter omgekeerd evenredig, wat betekent dat hoe meer "groot" het molecuul, hoe langzaam migreert.
Het kan u van dienst zijn: Lia Agar (Iron Lysine): wat is, fundering, voorbereiding, gebruikIn relatie tot het elektrische veld
Tot nu toe hebben we gesproken over het belang van het elektrische veld om de beweging van een deeltje door elektroforese te bereiken, maar we hebben niet gedefinieerd wat het is: elektrische kracht per eenheid van belasting of, in eenvoudiger termen, een gebied van ruimte waar er is waar er is een elektrische kracht.
De parameters met betrekking tot het elektrische veld dat de migratie kan beïnvloeden, zijn spanning, stroom en weerstand.
De spanning beïnvloedt de "vliegtijd" van de moleculen die zijn gescheiden na het aanbrengen van het elektrische veld. Hoe hoger het is, hoe sneller deze beweging.
De stroom (continue en uniforme elektronen die worden "geduwd" door de spanningsbron) wordt uitgevoerd tussen de elektroforetische systeemelektroden dankzij de ionen die aanwezig zijn in de bufferoplossing. Is direct gerelateerd aan spanning.
In relatie tot de bufferoplossing
De samenstelling, ionische kracht en pH van de bufferoplossing zijn de belangrijkste parameters die een elektroforetische "run" beïnvloeden, omdat ze direct een deel van de eigenschappen van de monsters beïnvloeden, met name de elektrische lading.
Omdat? De bufferoplossing stabiliseert de pH van het ondersteuningsmedium waar elektroforese optreedt. De samenstelling ervan kan de verplaatsing van de migratedeeltjes en de ionische concentratie ook beïnvloeden, omdat deze direct gerelateerd is aan de stroom.
Met betrekking tot het ondersteuningsmedium
De verschillende soorten en elektroforese -formaten presenteren ook verschillende media waarop migratie optreedt en waar het vervolgens kan worden "geregistreerd".
De migratiesnelheid van de aan elektroforese onderworpen moleculen hangt af van het type ondersteuningsmedium, dat meestal inert moet zijn.
De absorptie-eigenschappen ervan, elektro-endo-osmose zijn belangrijk (bewegingscapaciteit van een vloeistof door een membraan onder invloed van een elektrisch veld) en zijn moleculaire zeefcapaciteit.
Voorbeelden van het gebruik van elektroforese
Klassieke voorbeelden van elektroforetische technieken die in de biologie en biotechnologie worden gebruikt, zijn onder meer:
- Elektroforese in agarosegels (Engels Elektroforese gel))
- Elektroforese in acrylamidegels in denaturaliserende omstandigheden (SDS-PAGE, Engels Natriumdodecylsulfat polyacrylamidegelelektroforese))
- Elektroforese in acrylamidegels in inheemse omstandigheden (BN-PAGE, Engels Blauwe natieve polyacrylamidegelelektroforese))
- Elektroforese in twee dimensies (2D-pagina, uit het Engels Tweedimensionale polyacrylamidegelelektroforese))
- Capillaire elektroforese (uit het Engels Elektroforese capillair))
- Isolectroenfoque (Engels Isolectrophocusing))
- Gepulseerde veldelektroforese (Engels Gepulseerde veldelektroforese))
Referenties
- Beck, Kevin. (2020, 25 mei). De soorten elektroforese. Wetenschap.com. Opgehaald uit de wetenschap.com
- Essays, VK. (November 2018). Elektroforese typen en toepassingen. Opgehaald uit ukessays.com
- Nelson, D. L., Lehninger, een. L., & Cox, m. M. (2008). Lehninger -principes van biochemie. Macmillan.
- Parmar, p. (Augustus 2018). Elektroforese: betekenis, definitie en classificatie (met diagram). Bio -technologie. Opgehaald uit biotechnologie.com
- Perrett, D. (2010). 200 jaar elektroforese. Chromatog. Vandaag 4-7.
- Righetti, p. G. (2005). Elektroforese: The Mars of Pennies, The March of Dimes. Journal of Chromatography A, 1079 (1-2), 24-40.
- Rilbe, h. (negentienvijfennegentig). Som herinneringen van de geschiedenis van elektroforese. Elektroforese, 16 (1), 1354-1359.
- Vesterberg, of. (1993). Een korte geschiedenis van elektroforetische methoden. Elektroforese, 14 (1), 1243-1249.
- Vinayagam, m. (Geen datum). Factoren die de elektroforese beïnvloeden. Academie.Edu. Opgehaald uit de academische wereld.Edu
- « Chemical Balance -verklaring, factoren, typen, voorbeelden
- Toltec -cultuur oorsprong, locatie, kenmerken, organisatie »

