Onderdelen en voorbeelden van chemische vergelijking
- 2461
- 209
- Cecil Graham
De Reactievergelijking Het is een schematische weergave van sommige kenmerken van een chemische reactie. Er kan ook worden gezegd dat de chemische vergelijking de veranderingen beschrijft die worden ervaren door de verschillende stoffen die bij een reactie betrokken zijn.
In de chemische vergelijking worden de formules en symbolen van de verschillende deelnemende stoffen geplaatst, wat duidelijk wijst op het aantal atomen van elk element dat aanwezig is in de verbindingen, dat verschijnt als een subscript en niet kan worden gewijzigd bij het balanceren van de vergelijking.
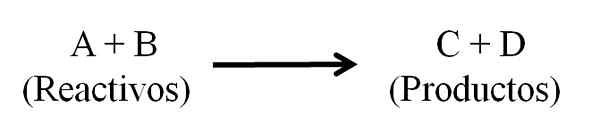
 Algemene chemische vergelijking voor een chemische reactie. Reagentia en producten. Bron: Gabriel Bolívar.
Algemene chemische vergelijking voor een chemische reactie. Reagentia en producten. Bron: Gabriel Bolívar. De chemische vergelijking moet in evenwicht lijken, dat wil zeggen dat het aantal atomen van zowel reagentia als producten hetzelfde moet zijn. Op deze manier wordt de wet van het behoud van materie gehoorzamen. Het is wenselijk dat de getallen die worden gebruikt om de vergelijkingen in evenwicht te brengen, hele getallen zijn.
Deze vergelijkingen onthullen geen opeenvolgende stappen, of waarom mechanismen reagentia worden omgezet in producten.
Dat is de reden waarom hoewel ze erg nuttig zijn om te begrijpen waar een chemische reactie naartoe gaat, het niet toestaat om de moleculaire aspecten ervan te begrijpen of hoe ze worden beïnvloed door bepaalde variabelen; zoals pH, viscositeit, reactietijd, agitatiesnelheid, onder andere.
[TOC]
Delen van een chemische vergelijking
In principe zijn er drie hoofdonderdelen in een chemische vergelijking: de reagentia, de producten en de pijl die de betekenis van de chemische reactie aangeeft.
Locatie van reagentia en producten
In de chemische vergelijking verschijnen alle stoffen die fungeren als reagentia en al diegenen die producten zijn. Deze middelengroepen worden gescheiden door een pijl die de betekenis van de reactie aangeeft. De reagentia bevinden zich links van de pijl en de producten aan de rechterkant.
De pijl betekent wat wordt geproduceerd en is georiënteerd van links naar rechts (→), hoewel er in de omkeerbare reacties twee equivalente en parallelle pijlen zijn; de ene naar rechts gericht, en een andere naar links. Het symbool (δ) wordt meestal op de pijl geplaatst, wat aangeeft dat warmte in de reactie werd gebruikt.
Kan u van dienst zijn: TerpenosBovendien wordt de identificatie van de katalysator meestal op de pijl geplaatst, indien mogelijk met zijn formule of symbool. De verschillende stoffen die als reagentia verschijnen, worden gescheiden door teken (+), wat aangeeft dat stoffen reageren of met elkaar combineren.
In het geval van stoffen die als producten verschijnen, heeft teken (+) niet de eerdere connotatie; Tenzij de reactie omkeerbaar is. Het is handig dat het teken (+) op gelijke afstand wordt geplaatst van de scheidende stoffen.
Evenwicht van chemische vergelijkingen
Het is een essentiële vereiste dat chemische vergelijkingen goed in evenwicht zijn. Hiervoor wordt een getal genaamd stoichiometrische coëfficiënt geplaatst. Indien nodig moet deze coëfficiënt voor de stoffen gaan die verschijnen als reagentia of producten.
Dit is zo om ervoor te zorgen dat het aantal atomen van de elementen die als reagentia verschijnen precies gelijk is aan het aantal dat in het product verschijnt. De eenvoudigste methode voor chemische vergelijkingen is die van Tanteo.
Fysieke toestanden van de componenten van de chemische vergelijking
In sommige chemische vergelijkingen wordt de fysische toestand van stoffen aangegeven met een subindustrie. Hiervoor worden de volgende afkortingen in het Spaans gebruikt: (s) voor de vaste toestand; (l) voor de vloeibare toestand; (g), gasvormige toestand; en (AC), waterige oplossing.
Voorbeeld: calciumcarbonaatreactie met zoutzuur.
Dief3 (s) + 2 HCl(AC) → CaCl2 (s) + H2OF(L) + CO2 g)
Veranderingen van de fysieke status
In sommige gevallen wordt het aangegeven in de chemische vergelijking als er een productie van een gas in de chemische reactie is of als er de neerslag is van een van de geproduceerde stoffen.
Kan u van dienst zijn: binaire zoutenDe aanwezigheid van een gas wordt aangegeven met een verticale pijl met zijn uiteinde naar boven gericht (↑), geplaatst aan de rechterkant van de gasvormige stof.
Voorbeeld: zinkreactie met zoutzuur.
Zn +2 HCl → ZnCl2 + H2↑
Als in de chemische reactie een van de stoffen een neerslag vormt, wordt dit gesymboliseerd door een verticale pijl te plaatsen met zijn uiteinde gericht (↓), geplaatst aan de rechterkant van de neergeslagen stof.
Voorbeeld: zoutzuurreactie met zilvernitraat.
HCl + Agno3 → hno3 + Agcl ↓
Voorbeeld van chemische vergelijkingen
- Fotosynthese
 Fotosynthese -vergelijking
Fotosynthese -vergelijking Fotosynthese is een proces waarbij planten lichte energie vastleggen en transformeren, van zonlicht, om de energie te genereren die nodig is voor hun bestaan. Fotosynthese wordt uitgevoerd door organellen die typisch zijn voor plantencellen die chloroplasten worden genoemd.
In het chloroplastmembraan zijn tilacoïden, plaatsen waar chlorofylen worden gevonden naar En B, die de belangrijkste pigmenten zijn die lichte energie vastleggen.
Hoewel fotosynthese een complex proces is, kan het worden gechematiseerd in de volgende chemische vergelijking:
6 CO2 + 6 H2O → C6H12OF6 + 6 o2↑ ΔGº = 2.870 kJ/mol
C6H12OF6 Het is de formule van glucose, gemetaboliseerde koolhydraat voor de productie van ATP; Verbinding dat is het belangrijkste energiereservoir in de meeste levende wezens. Bovendien wordt van glucose NADPH gegenereerd, co -enzym nodig voor talloze reacties.
- Cellulaire ademhaling
Cellen gebruiken zuurstof voor het metabolisme van talloze stoffen die aanwezig zijn in ingenomen voedingsmiddelen. Ondertussen wordt de ATP gebruikt als een energiebron van de activiteiten die worden uitgevoerd door levende wezens, die in deze processen dioxide -koolstof en water produceren.
Kan u van dienst zijn: aluminium acetaat (AL (CH3COO) 3): structuur, eigenschappen, gebruikAls glucose wordt gebruikt als een gemetaboliseerd middelenmodel, kan ademhaling worden gescheiden door de volgende chemische vergelijking:
C6H12OF6 + 6 o2 → 6 CO2 + 6 H2OF
- Veel voorkomende elementenreacties
Ontledingsreactie
Een verbinding of verbindingen dissocieert (n) die vormt met zijn atomen andere verschillende verbindingen:
2 KCLO3 (s) → 2 KCl(S) + 3 o2 g)
Verplaatsingsreactie
Een metaal reageert met een verbinding die hierin een aanwezige metaal vervangt:
Mg(S) + Cuso4 (AC) → Cu(S) + MGSO4 (AC)
Eliminatiereactie
In dit type reactie, het aantal atomen of groepen bevestigd aan een koolstofatoom:
Ch3-Ch2Br +NaOH → H2C = Ch2 + H2O +Nabr
Hydratatiereactie
Het is een reactie waarbij een verbinding een watermolecuul toevoegt. Deze reactie is belangrijk bij de bereiding van alcoholen:
H2C = Ch2 + H2O → H2C-CH2Oh
Neutralisatie-reactie
Een basis of alkali reageert met een zuur dat een zout en water produceert:
HCl(AC) + Nao(AC) → NaCl(AC) + H2OF(L)
Synthesiereactie
In dit type reactie worden twee of meer stoffen gecombineerd om een nieuwe verbinding te veroorzaken:
2 Li(S) + Klet2 g) → 2 licl(S)
Dubbele verplaatsingsreactie (metathese)
In dit type reactie is er uitwisseling van positieve en negatieve ionen om nieuwe verbindingen te vormen:
Agno3 (AC) + NaCl(AC) → Agcl(S) + Oudere broer3 (AC)
Referenties
- Bloemen, j. (2002). Scheikunde. Editie 1was. Santillana redactioneel
- Mathews, c. K., Van Holde, K. EN., En ahern, k. G. (2002). Biochemie. 3was Editie. Pearson Addison Wesley redactioneel
- Whitten, Davis, Peck & Stanley. (2008). Scheikunde. (8e ed.)). Cengage leren.
- Wikipedia. (2019). Reactievergelijking. Opgehaald uit: in.Wikipedia.borg
- Helmestine, Anne Marie, pH.D. (20 september 2019). Wat is een chemische vergelijking? Hersteld van: Thoughtco.com
- « Molair volume concept en formule, berekening en voorbeelden
- Challenger abyss geologische vorming, locatie, kenmerken »

