Molair volume concept en formule, berekening en voorbeelden
- 696
- 27
- Pete Heaney V
Hij Molair volume Het is een intensieve eigenschap die aangeeft hoeveel ruimte een mol van een bepaling of verbinding inneemt. Wordt weergegeven door symbool VM, en wordt uitgedrukt in DM -eenheden3/mol voor gassen en cm3/mol voor vloeistoffen en vaste stoffen, omdat de laatste meer beperkt zijn door hun grootste intermoleculaire krachten.
Deze eigenschap komt terug bij het bestuderen van thermodynamische systemen die gassen met zich meebrengen; sindsdien, voor vloeistoffen en vaste stoffen de vergelijkingen om V te bepalenM Ze worden ingewikkelder en onnauwkeuriger. Daarom, wat basiscursussen betreft, wordt molaire volume altijd geassocieerd met de ideale gassentheorie.
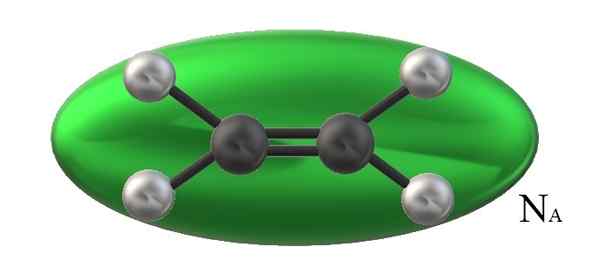
 Het volume van een ethyleenmolecuul wordt oppervlakkig beperkt door de groene ellipsoïde en het aantal Avogadro -tijden deze hoeveelheid. Bron: Gabriel Bolívar.
Het volume van een ethyleenmolecuul wordt oppervlakkig beperkt door de groene ellipsoïde en het aantal Avogadro -tijden deze hoeveelheid. Bron: Gabriel Bolívar. Dit komt omdat voor de ideale of perfecte gassen de structurele aspecten niet relevant zijn; Al zijn deeltjes worden gevisualiseerd als bollen die elastisch met elkaar botsen en zich op dezelfde manier gedragen, ongeacht wat hun massa of eigenschappen zijn.
Aldus zal één mol van elk ideaal gas bij een bepaalde druk en temperatuur hetzelfde volume V bezettenM. Er wordt gezegd dat onder normale omstandigheden van P en T, respectievelijk 1 atm en 0 ºC, één mol van een ideaal gas een volume van 22,4 liter zal bezetten. Deze waarde is nuttig en benaderen zelfs wanneer echte gassen worden geëvalueerd.
[TOC]
Concept en formule
Voor gassen
De onmiddellijke formule om het molaire volume van een soort te berekenen is:
VM = V/n
Waar v het volume is dat het bezet, en N De hoeveelheid van de soort in mollen. Het probleem is dat vM Het hangt af van de druk en temperatuur die wordt ervaren door moleculen, en een wiskundige uitdrukking is gewenst om rekening te houden met deze variabelen.
Kan u van dienst zijn: MolealityHet ethyleen van het beeld, h2C = Ch2, Het heeft een moleculair volume geassocieerd en beperkt door een groene ellipsoïde. Dit h2C = Ch2 Het kan op meerdere manieren roteren, wat is alsof het in de ruimte wordt bewogen die ellipsoïde is om te visualiseren hoeveel volume het zou bezetten (kennelijk verachtelijk).
Als het volume van zo'n groene ellipsoïde echter vermenigvuldigen, vermenigvuldigen we het met nNAAR, Het Avogadro -nummer zal dan een mol ethyleenmoleculen hebben; een mol ellipsoïde die met elkaar in wisselwerking staat. Bij een hogere temperatuur scheiden de moleculen van elkaar; Hoewel ze bij meer druk worden aangebracht en hun volume zullen verminderen.
Daarom vM is afhankelijk van P en T. Ethyleen is platte geometrie, dus het kan niet worden gedacht dat zijn VM Wees nauwkeurig en precies hetzelfde als die van methaan, cho4, van tetraëdrische geometrie en in staat om te worden weergegeven met een bol en niet een ellipsoïde.
Voor vloeistoffen en vaste stoffen
De moleculen of atomen van vloeistoffen en vaste stoffen hebben ook hun eigen VM, die kan worden gerelateerd aan uw dichtheid:
VM = m/(d · n)
De temperatuur beïnvloedt het molaire volume meer voor vloeistoffen en vaste stoffen dan de druk, zolang deze niet sterk of exorbitant varieert (in de volgorde van de GPA). Evenzo, zoals vermeld met ethyleen, hebben geometrieën en moleculaire structuren een grote invloed op de waarden van VM.
In normale omstandigheden wordt echter waargenomen dat dichtheden voor verschillende vloeistoffen of vaste stoffen niet te veel variëren in hun magnitudes; Hetzelfde geldt voor zijn molaire volumes. Merk op dat hoe dichtst ze zijn, hoe lagere VM.
Wat vaste stoffen betreft, hangt het molaire volume ook af van zijn kristallijne structuren (het volume van de eenheidscel).
Kan u van dienst zijn: kalium bifthalaat: structuur, nomenclatuur, gebruik, risico'sHoe molair volume te berekenen?
In tegenstelling tot vloeistoffen en vaste stoffen, is er voor ideale gassen een vergelijking waarmee u V kunt berekenenM Afhankelijk van P en T en zijn veranderingen; Dit is dat van ideale gassen:
P = NRT/V
Die meegaand is om v/n uit te drukken:
V/n = rt/p
VM = RT/P
Als we de gasconstante r = 0,082 l · atm · k gebruiken-1· Mol-1, Dan moeten de temperaturen worden uitgedrukt in Kelvin (K) en de druk in atmosferen. Merk op dat hier wordt waargenomen waarom VM Het is een intensieve eigenschap: T en P hebben niets te maken met de massa van het gas, maar met zijn volume.
Deze berekeningen zijn alleen geldig in omstandigheden waarbij gassen zich nauw gedragen voor idealiteit. De door experimenten verkregen waarden hebben echter een kleine marge ten opzichte van theoretici.
Molaire volumeberekening voorbeelden
voorbeeld 1
Je hebt een gas en wiens dichtheid 8,5 · 10 is-4 g/cm3. Als je 16 gram hebt die gelijkwaardig is aan 0,92 mol y, bereken dan je molaire volume.
Uit de dichtheidsformule kunnen we berekenen welk volume en dergelijke 16 gram bezetten:
V = 16 g/ (8,5 · 10-4 g/cm3))
= 18.823.52 cm3 of 18.82 l
Dus vM Het wordt direct berekend door dit volume te delen tussen de gegeven hoeveelheid mol:
VM = 18,82 l/0,92 mol
= 20,45 l/mol o l · mol-1 of DM3· Mol-1
Oefening 2
In het vorige voorbeeld van en werd op geen enkel moment gespecificeerd wat de temperatuur was die werd ervaren door de deeltjes van genoemde gas. Ervan uitgaande dat het werkte met en bij atmosferische druk, berekent u de temperatuur die nodig is om het te comprimeren tot het bepaalde molaire volume.
Kan u van dienst zijn: verpakkingsfactorDe trainingsverklaring is langer dan de resolutie. We gaan naar de vergelijking:
VM = RT/P
Maar we wissen T, en wetende dat atmosferische druk 1 atm is, lossen we op:
T = vMP/r
= (20,45 l/mol) (1 atm)/(0,082 l · atm/k · mol)
= 249.39 K
Dat wil zeggen, één mol en zal 20,45 liter bezetten bij een temperatuur dicht bij -23.76 ºC.
Oefening 3
Bepaal V na de bovenstaande resultaten VM bij 0 ºC, 25 ° C en bij absolute nul bij atmosferische druk.
De temperaturen transformeren naar Kelvin, hebben we eerste 273.17 K, 298.15 K en 0 K. We lossen rechtstreeks op door de eerste en tweede temperaturen te vervangen:
VM = RT/P
= (0,082 L · atm/ k · mol) (273,15 K)/ 1 atm
= 22.40 l/mol (0 ºC)
= (0,082 L · atm/ k · mol) (298,15 K)/ 1 atm
= 24,45 l/mol (25ºC)
De waarde van 22,4 liter werd in het begin genoemd. Merk op hoe vM Verhogen met de temperatuur. Als u dezelfde berekening met absolute nul wilt maken, struikelen we de derde wet van de thermodynamica:
(0,082 L · ATM/ K · mol) (0 K)/ 1 atm
= 0 l/mol (-273.15 ºC)
Het gas en kan geen niet -bestaand molaire volume hebben; Dat betekent dat het een vloeistof is geworden en de vorige vergelijking is niet langer geldig.
Aan de andere kant is de onmogelijkheid om V te berekenenM In absolute nul gehoorzaamt de derde wet van de thermodynamica, die zegt dat het onmogelijk is om elke stof bij de temperatuur van absolute nul te koelen.
Referenties
- Iran. Levine. (2014). Principes van fysicochemie. Zesde editie. MC Graw Hill.
- Glasstone. (1970). Fysisch chemie verdrag. Tweede druk. Machtig.
- Wikipedia. (2019). Molair volume. Opgehaald uit: in.Wikipedia.borg
- Helmestine, Anne Marie, pH.D. (8 augustus 2019). Molaire volumedefinitie in de chemie. Hersteld van: Thoughtco.com
- Byju's. (2019). Molaire volumeformule. Hersteld van: byjus.com
- González Mónica. (28 oktober 2010). Molair volume. Hersteld van: chemie.Laguia2000.com

