Chemische concentratie

- 3143
- 406
- Kurt Aufderhar Jr.
 Chemische concentratie is wat het aandeel van een opgeloste stof en een oplosmiddel in een chemische oplossing bepaalt
Chemische concentratie is wat het aandeel van een opgeloste stof en een oplosmiddel in een chemische oplossing bepaalt Wat is chemische concentratie?
De Chemische concentratie Het is een eigenschap van de oplossingen die de hoeveelheid opgeloste stof vertegenwoordigt voor elke eenheid van oplossing. Met andere woorden, het is een getal dat aangeeft het aandeel waarin de opgeloste stof en het oplosmiddel zich bevinden.
Bedenk dat een oplossing een homogeen mengsel is gevormd door een oplosmiddel (in het algemeen vloeistof) en een of meer stoffen opgelost in het oplosmiddel dat we opgeloste stoffen noemen. De oplossingen worden gekenmerkt door het oplosmiddel, de opgeloste stof en de concentratie.
De concentratie is een zeer nuttige eigenschap, omdat het ons in staat stelt ze te beschrijven. Als we bijvoorbeeld weten dat de concentratie van zout in zeewater 35 gram is voor elke liter, weten we dat we in ons huis 35 gram zout in een liter oplossing oplossen, we een gelijke oplossing van zout zullen verkrijgen dat zeewater.
Kenmerken van chemische concentratie
Het is een intensief eigendom
Dit is het belangrijkste kenmerk van concentratie. Intensief betekent dat het niet afhangt van de hoeveelheid oplossing die we hebben. Als voorbeeld betekent dit dat de concentratie hetzelfde is in een druppel zeewater dan in 100 liter hetzelfde.
Kan variëren met temperatuur
Over het algemeen breiden vloeistoffen hun volume uit of verhogen. Dit geldt ook voor oplossingen. Om deze reden kunnen de uitgedrukte concentraties afhankelijk van het volume enigszins veranderen bij het verwarmen of koelen van de oplossing.
Het kan zeer brede bereikbereiken dekken
Ongeacht de eenheden waarin een chemische concentratie wordt uitgedrukt, kan deze hebben van relatief grote waarden tot extreem kleine waarden.
De concentratie van een in het percentage uitgedrukte oplossing kan bijvoorbeeld waarden hebben van 0% tot 100%, waardoor vele ordes van grootte worden bestrijkt. We kunnen een oplossing van 90%voorbereiden, omdat we ook één om 10 kunnen voorbereiden-12%, dat is bijna 14 orden van kleine omvang.
Wat is chemische concentratie voor?
Als we de concentratie van een oplossing kennen, kunnen we deze beschrijven. Er zijn veel eigenschappen van oplossingen die afhankelijk zijn van hun concentratie. Het smelt- en kookpunt is bijvoorbeeld afhankelijk van de concentratie, dus wetende dat het ons in staat stelt deze twee eigenschappen te berekenen.
Kan u van dienst zijn: glasachtige staatAan de andere kant stelt concentratie ons in staat om een oplossing gemakkelijk te vergelijken met een andere. Als we twee wateroplossingen met suiker hebben, kunnen we weten dat hun concentraties kunnen weten welke van de twee zoeter is.
Bovendien hangen alle chemische reacties die het leven mogelijk maken sterk af van de concentratie van eindeloze opgeloste opgeloste stoffen in cellen en de omgeving van levende wezens.
De concentratie van zuurstof in de lucht bepaalt bijvoorbeeld of een persoon zal stikken of niet; De pH van een oplossing (wat een manier is om de concentratie van H -ionen te meten+) Bepaal of een bacteriën zullen leven en zich voortplanten of dat deze daarentegen zal sterven; en de concentratie van een gif zal bepalen of het dodelijk zal zijn of niet.
Soorten concentratie -eenheden
De concentratie van een oplossing is er één, dus het is niet correct om te praten over soorten concentratie. Dezelfde concentratie kan echter worden uitgedrukt in verschillende soorten concentratie -eenheden. Dit zijn:
- Fysieke concentratie -eenheden
- Chemische concentratie -eenheden
Fysieke concentratie -eenheden
Deze worden gekenmerkt door de hoeveelheden van de opgeloste stof en het oplosmiddel uit te drukken, hetzij in eenheden van massa of volume. Ze worden fysieke eenheden genoemd, omdat ze worden geassocieerd met massa's en volumes in plaats van mol en equivalent.
Wanneer we twee oplossingen vergelijken met dezelfde fysieke concentratie, kunnen we niet ervoor zorgen dat ze gelijke hoeveelheden atomen en moleculen hebben. Dit is wat hen onderscheidt van chemische concentratie -eenheden.
De meest voorkomende fysieke concentratie -eenheden zijn:
- Eenvoudige titel (TS)
- %gewicht/gewicht (%P/P) of massa/massa (%m/m)
- %gewicht/volume (%p/v) of massa/volume (%m/v)
- % volume/volume (% v/v)
- Delen per miljoen gewicht/gewicht (PPMp/p) of massa/massa (ppmm/m))
- Delen per miljoen gewicht/volume (ppmp/v) of massa/volume (ppmm/v))
- Onderdelen per miljoen volume/volume (PPMV/v))
Chemische concentratie -eenheden
In het geval van chemische eenheden worden de hoeveelheid opgeloste stof en in sommige gevallen die van het oplosmiddel of de oplossing uitgedrukt in termen van het aantal deeltjes of mol of equivalenten die aanwezig zijn in de oplossing.
Ze worden chemische eenheden genoemd, omdat twee oplossingen die dezelfde chemische concentratie hebben, equivalente hoeveelheden atomen, moleculen of opgeloste ionen per eenheid van oplossing hebben, zoals het geval kan zijn.
Kan u van dienst zijn: Oplosbaarheidsregels: algemene aspecten en regelsDe meest voorkomende chemische eenheden zijn:
- Molariteit (M)
- Molaliteit (M)
- Molaire fractie (x)
- Normaliteit (N)
Formule van fysische concentratie -eenheden
Eenvoudige titel (TS)
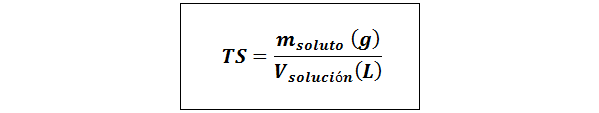
Waar mopgeloste stof vertegenwoordigt de massa van de opgeloste stof in gram en voplossing Het is het volume van de oplossing in liters.
%gewicht/gewicht (%P/P) of massa/massa (%m/m)
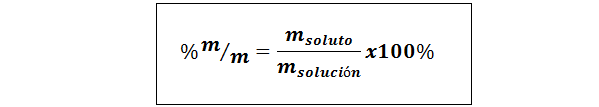
Waar mopgeloste stof en Moplossing vertegenwoordigen respectievelijk de massa van de opgeloste stof en de oplossing. Elke massa -eenheid kan worden gebruikt (G, MG, KG, enz.), zolang beide massa's in dezelfde eenheid worden uitgedrukt.
%gewicht/volume (%p/v) of massa/volume (%m/v)
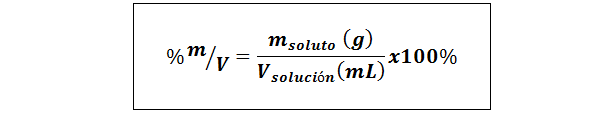
Waar mopgeloste stof Het is de massa van de oplossing in gram en voplossing Het is het volume van de oplossing, in dit geval in milliliter.
% volume/volume (% v/v)

Waar vopgeloste stof en voplossing vertegenwoordigen respectievelijk het volume van de opgeloste stof en de oplossing. In dit geval kan elke eenheid worden gebruikt om deze volumes uit te drukken, zolang het voor beide hetzelfde is.
Delen per miljoen gewicht/gewicht (PPMp/p) of massa/massa (ppmm/m))
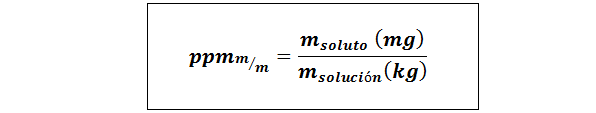
Waar mopgeloste stof en Moplossing Ze vertegenwoordigen de massa van de opgeloste stof en de oplossing in respectievelijk milligram en kilogrammen.
Delen per miljoen gewicht/volume (ppmp/v) of massa/volume (ppmm/v))
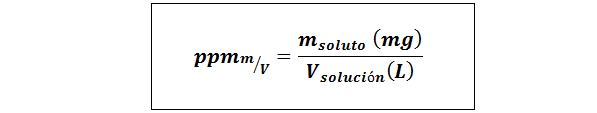
Waar mopgeloste stof Het is de massa van de oplossing in milligram en voplossing Het is het volume van de oplossing, in dit geval in liters.
Onderdelen per miljoen volume/volume (PPMV/v))
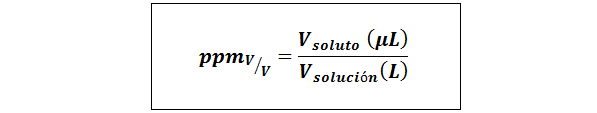
Waar vopgeloste stof en voplossing Ze zijn respectievelijk het volume van de opgeloste stof en de oplossing in microliter en liters.
Formules van de chemische concentratie -eenheden
In het geval van chemische concentratie -eenheden wordt de hoeveelheid van de componenten van de oplossing, met name van de opgeloste stof, uitgedrukt in het aantal mol of in het aantal equivalenten. Deze hoeveelheden hebben het reële aantal deeltjes (atomen, moleculen of ionen, naargelang het geval).
Deze hoeveelheden kunnen niet eenvoudig bekend zijn door het wegen of meten van het volume van stoffen, maar het is noodzakelijk om de samenstelling of chemische formule van de verbindingen te kennen om de concentratie te bepalen. Dit is de belangrijkste reden waarom ze chemische concentraties worden genoemd.
Vervolgens worden de verschillende formules gepresenteerd om de vier meest gebruikte chemische concentraties te berekenen:
Molariteit (M)
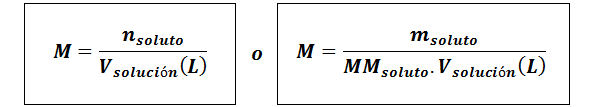
Waaropgeloste stof Ze zijn de mol opgeloste stof, mopgeloste stof vertegenwoordigt de massa van de opgeloste stof in gram, mmopgeloste stof is zijn molaire massa en voplossing Het is het volume van de oplossing in liters.
Molaliteit (M)
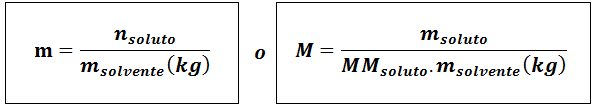
Waaropgeloste stof Ze zijn de mol opgeloste stof, mopgeloste stof vertegenwoordigt de massa van de opgeloste stof in gram, mmopgeloste stof Het is zijn molaire massa en moplosmiddel Het is de massa van het oplosmiddel in kilogram.
Kan u van dienst zijn: solvatieMolaire fractie (x)
De molaire fractie kan worden berekend voor zowel de opgeloste stof als het oplosmiddel. De molaire fractie van de opgeloste stof is:
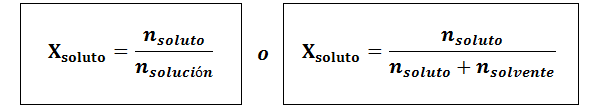
Het oplosmiddel is:
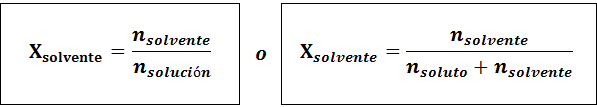
De relatie tussen beide molaire fracties is:
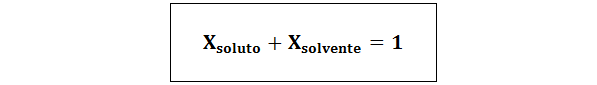
In alle gevallen nopgeloste stof, Noplossing en Noplosmiddel zijn respectievelijk de mol opgeloste stof, oplossing en oplosmiddel.
Normaliteit (N)
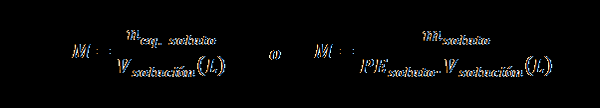
Hier neq. opgeloste stof vertegenwoordigt het aantal equivalent van de opgeloste stof, mopgeloste stof vertegenwoordigt de massa van de opgeloste stof, PEopgeloste stof Het is het equivalente gewicht van de opgeloste stof en Voplossing Het is het volume van de oplossing in liters.
Voorbeelden van chemische concentratie
- De concentratie van zout in marien water is 35 g/l, wat overeenkomt met een molariteit van 0,60 mol/l.
- De gemiddelde bloedsuikerconcentratie ligt tussen 82 mg/dl en 110 mg/dl. Deze concentraties zijn gelijk aan een eenvoudige titel bij 0,82 g/l en 1,10 g/l, en in molariteit op 4,4.10-3 mol/l en 6.1.10-3 mol/l, respectievelijk.
- De lucht kan worden beschouwd als een gasvormige oplossing die voornamelijk wordt gevormd door stikstof en zuurstof, het oplosmiddel is stikstof, omdat deze in een groter verhouding is. Deze gasoplossing bevat een 0,22 zuurstof- en stikstoffractie van ongeveer 0,78.
- Staal is een legering tussen ijzer en koolstof. Hoewel het geen strikt oplossingen zijn, zijn dit homogene vaste mengsels die meestal een koolstofconcentratie bevatten in de volgorde van 0,03% en 1.075% in massa.
- Ondanks de verwoestende effecten voor het milieu en voor de gezondheid van mensen, zijn concentraties van veel verontreinigende stoffen meestal aanzienlijk laag. Een voorbeeld is de maximale concentratie van arseen giftig metaal in water. De Wereldgezondheidsorganisatie (WHO) heeft vastgesteld dat drinkwater geen arseenconcentratie mag bevatten groter dan 10ppb M/V (delen per miljard of nanogram per liter). Deze concentratie is gelijk aan 0.010 PPM M/V.
Referenties
- BBC (s. F.)). Concentratie van oplossingen - Berekeningen in chemie - AQA - GCSE Chemistry (Single Science) Review - AQA. BBC genomen.co.Uk.
- Dit is wat concentratie betekent in de chemie (2020). Take van Thoughtco.com.
- LiBhethexts (2022). 4.5: Concentratie van oplossingen. Genomen uit chem.Librhetxts.borg.
- Mandal, a., MD. (2021). Normale bloedsuikerwaarden. Ontleend aan nieuws-medisch.netto.
- Chemicaliën.Netto (s. F.)). Chemische concentraties. Uit chemici genomen.netto.

