Verdampingswarmte

- 2001
- 276
- James Dach
 De verdampingswarmte of verdamping is degene die een chemische stof lijdt om de vloeibare toestand in de gasvormige te veranderen
De verdampingswarmte of verdamping is degene die een chemische stof lijdt om de vloeibare toestand in de gasvormige te veranderen Wat is verdampingswarmte?
Hij Verdampingswarmte, Ook wel verdampingswarmte genoemd, wordt het gedefinieerd als de hoeveelheid warmte die een pure chemie absorbeert om te verdampen, dat wil zeggen een verandering van toestand van de vloeibare toestand in de gastoestand.
Dat wil zeggen, het is de warmte die is geassocieerd met het volgende faseveranderingsproces:
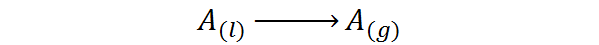
Het is een soort warmte die geen temperatuurstijging genereert, maar de krachten breekt die de vloeibare moleculen bij elkaar houden. Op deze manier is het mogelijk om de moleculen van elkaar te scheiden, ze te bevrijden van de gasfase.
Formule en eenheden
De verdampingswarmte of verdamping kan worden weergegeven door middel van het symbool QDapper. Het is een uitgebreide hoeveelheid, dat wil zeggen, het hangt af van de hoeveelheid substantie.
In die zin kan het worden berekend uit de hoeveelheid substantie en een intensieve maat voor verdampingswarmte.
Wanneer de hoeveelheid stof tot expressie wordt gebracht in de vorm van een massa, moet de latente verdampingswarmte of verdamping worden gebruikt, lDapper, in welk geval de verdampingswarmte wordt uitgedrukt als:
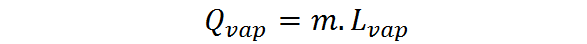
De latente verdampingswarmte is een intensieve en karakteristieke hoeveelheid van elke stof. Het is een min of meer directe maat voor hoe sterk de intermoleculaire interacties zijn tussen de deeltjes die een vloeistof vormen.
Aan de andere kant kan de verdampingswarmte ook worden berekend op basis van het aantal mol, in welk geval de molaire verdampingswarmte nodig is, ook wel verdampingsthalpie genoemd:
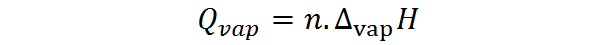
Waar N vertegenwoordigt het aantal mol en ∆DapperH is de enthalpie van verdamping van de stof. Vaporisatie -enthalpie vertegenwoordigt de hoeveelheid constante druk die nodig is om een mol van een stof te verdampen.
Het kan u van dienst zijn: propaanzuurVerdampingswarmte -eenheden
Als een soort warmte, wat een vorm van energie is, wordt verdampingswarmte uitgedrukt in energie -eenheden. De meest gebruikte eenheden zijn:
- Calorieën (kalk)
- Kilocalorieën (kcal of limoen)
- Jouls of Joules (J)
- Kilojouls of kilojulios (kj), etc.
Aan de andere kant, de latente verdampingswarmte (lDapper) Het wordt uitgedrukt in massa -energie -eenheden. Bijvoorbeeld:
- limoen/g
- Kcal/g
- Kcal/kg
- KJ/G
- kj/kg, etc.
Ten slotte, verdamping enthalpie (∆DapperH) Het wordt uitgedrukt in energie -eenheden op eenheden van hoeveelheid materie, meestal mol. Enkele voorbeelden zijn:
- limoen/mol
- Kcal/mol
- J/mol
- kj/mol, etc.
Hoe wordt verdampingswarmte berekend?
Zoals we een moment geleden zagen, kan verdampingswarmte worden berekend uit de massa of het aantal mol en de latente verdampingswarmte of de verdampingsthalpie, respectievelijk.
Deze hoeveelheden worden echter meestal bepaald, experimenteel meten van de hoeveelheid warmte die nodig is om een bepaalde massa van een stof te verdampen en vervolgens een van de twee eerdere vergelijkingen op te ruimen.
Vanwege het bovenstaande is het algemene ding niet dat de verdampingswarmte wordt berekend, maar dat deze experimenteel wordt gemeten, in het laboratorium.
Aan de andere kant, aangezien enthalpie als de thermodynamische eigenschap van een systeem een statusfunctie is, kan dit worden berekend uit andere enthalpieën die betrekking hebben op een stof in een vloeibare toestand met dezelfde stof in een gasvormige toestand.
Vaporisatie -enthalpie kan bijvoorbeeld worden berekend door de sublimatie -enthalpie af te trekken, behalve de fusion -enthalpie van een stof. Vervolgens worden deze enthalpie en het aantal mol gebruikt om de verdampingswarmte van het monster te bepalen.
Kan u van dienst zijn: aluminium polychloride: structuur, eigenschappen, verkrijgen, gebruikVerdampingswarmtoepassingen
Er zijn veel velden waarin verdampingswarmte wordt gebruikt. In feite, in elk proces dat een chemische stof inhoudt die ooit in een vloeibare toestand is en in een ander in een gasvormige toestand, zal de verdampingswarmte ingrijpen.
Verdampingswarmte is altijd positief, omdat het altijd nodig is om warmte te absorberen om de unie te breken tussen de moleculen die een vloeistof vormen. De stof absorbeert deze warmte uit de onmiddellijke omgeving, zodat ze warmte verliezen wanneer een vloeistof verdampt.
Verdampingswarmte en lichaamstemperatuurregulering
Dit is het werkingsprincipe van zweten als een lichaamstemperatuurregulatiesysteem.
Als we zweten, verdampt zweetwater op het oppervlak van onze huid. Omdat de huid in direct contact is met zweet, is dat waar het water de verdampingswarmte verkrijgt.
Dan, wanneer het verdampt, draagt het zweetwater een hoeveelheid warmte van de huid, die afkoelen, ook het bloed koelen dat door de haarvaten van de huid stroomt en uiteindelijk het interieur van het lichaam.
Verdampingswarmte in de industrie
Energie is een van de grootste kosten voor veel industrieën, en velen van hen moeten energie uitgeven om verschillende stoffen te verdampen. Om deze reden is het noodzakelijk om de hoeveelheid warmte te berekenen die nodig is om verschillende vloeistoffen te verdampen, om de bedrijfskosten te berekenen.
Als een farmaceutisch bedrijf bijvoorbeeld een medicijn in een alcoholische oplossing synthetiseert, zal het waarschijnlijk moeten verdampen en het product drogen om alle alcohol te elimineren. Verdampingswarmte stelt ons in staat om te bepalen hoeveel energie nodig is om dit uit te voeren.
Het kan u van dienst zijn: periódiczuur (HIO4): wat is, structuur, eigenschappen, gebruikIJsproductie op een trein
Vóór het bestaan van elektriciteit gebruikten treinen verdampingswarmte om water te bevriezen en zo ijs te maken tijdens de reis. Het proces is vergelijkbaar met zweten en werkt op dezelfde manier.
Op het station haakt de trein een lederen zak met vloeibaar water. De tas is niet perfect hermetisch, dus de buitenkant is bevochtigd. Tijdens de reis verdampt de lucht snel het water van het oppervlak van de zak, absorbeert warmte van vloeibaar water en afkoelt, tot het punt van het bevriezen.
Voorbeelden van verdampingsverwarming
De volgende tabel bevat latent verdampingswarmtes of verdamping voor sommige gemeenschappelijke chemicaliën.
| Substantie | Latente warmte van verdamping (LDapper/kj.G-1)) | Verdamping enthalpie (∆DapperH/kj.mol-1)) |
| Water (h2OF) | 2.260 | 40,657 |
| Ethanol (ch3Ch2OH) | 0,837 | 38.56 |
| Waterstofsulfide (h2S) | 0.6422 | 21.90 |
Referenties
- Ehu.Het is s. F.)). Latente warmte van waterdamping. Uitgevoerd van SC.Ehu.is.
- Luz, G. (S. F.)). Verdampingswarmte. Uit materialen genomen.Gelsonluz.com.
- Soler & Palau (2019). Latente warmte: fusie en verdamping. Uit Solerpalau genomen.com.
- Spiegato (2021). Wat is de verdampingswarmte? Uit Spiegato genomen.com.

