Evenwicht van materie wat is, algemene vergelijking, typen
- 3893
- 1162
- Ernesto McKenzie
Hij materiële balans Het is de telling van de componenten die tot een systeem of proces worden bestudeerd. Deze balans kan bijna op elk type systeem worden toegepast, omdat wordt aangenomen dat de som van de massa's van dergelijke elementen constant moet blijven voor verschillende metingen van metingen.
U kunt door onderdeel van knikkers, bacteriën, dieren, hout, ingrediënten voor een cake begrijpen; en in het geval van chemie, moleculen of ionen, of meer specifiek, verbindingen of stoffen. Vervolgens moet de totale massa van de moleculen die een systeem binnenkomen, met of zonder chemische reactie constant blijven; Zolang er geen lekverliezen zijn.
In de praktijk worden ontelbare problemen gepresenteerd die de balans van materie kunnen beïnvloeden, naast rekening houdend met verschillende fenomenen van materie en het effect van veel variabelen (temperatuur, druk, stroming, agitatie, reactormrootte, enz.)).
Op papier moeten de berekeningen van het evenwicht echter samenvallen; dat wil zeggen, de massa chemische verbindingen zou op geen enkel moment moeten verdwijnen. Dit evenwicht maken is analoog om een stapel rotsen in evenwicht te brengen. Als een van de massa's niet op zijn plaats komt, valt alles uit elkaar; In dit geval zou dit betekenen dat de berekeningen verkeerd zijn.
Algemene vergelijking van het vakgebied
In elk systeem of proces moet eerst worden gedefinieerd wat hun grenzen zijn. Van hen zal bekend zijn welke verbindingen binnenkomen of vertrekken. Het is handig om dit te doen, vooral als er meerdere proceseenheden zijn om te overwegen. Wanneer alle eenheden of subsystemen worden overwogen, is er sprake van een balans van algemene materie.
Dit saldo heeft een vergelijking, die kan worden toegepast op elk systeem dat de wet van massabeservatie gehoorzaamt. De vergelijking is als volgt:
Kan u van dienst zijn: loodchloride: eigenschappen, structuur, gebruikE + G - S - C = A
Waar e de hoeveelheid materie is binnenkomen Naar het systeem; G is wat ik weet genereren Als een chemische reactie optreedt in het proces (zoals in een reactor); S is wat komt uit van het systeem; C is wat ik weet consumeren, Nogmaals, als er een reactie is; En ten slotte is het wat ik weet zich ophopen.
Vereenvoudiging
Als in het bestudeerde systeem of proces geen chemische reactie is, zijn G en C nul waard. De vergelijking blijft dus:
E - S = A
Als het systeem ook wordt overwogen in de stationaire toestand, zonder aanzienlijke veranderingen in de variabelen of stromen van de componenten, wordt gezegd dat er niets van binnen gaat. Daarom is het nul waard en de vergelijking vereenvoudigt nog meer:
E = s
Dat wil zeggen, de hoeveelheid materie die binnenkomt is gelijk aan degene die uitkomt. Niets kan verloren gaan of verdwijnen.
Aan de andere kant, als er een chemische reactie is, maar het systeem zich in de stationaire toestand bevindt, zal G en C waarden hebben en zullen ze nul blijven:
E + G - S - C = 0
E + G = S + C
Wat betekent dat in een reactor de massa van de reagentia die binnenkomen en van de producten die erin genereren, gelijk is aan de massa van de producten en reagentia die uitkomen, en van de geconsumeerde reagentia.
Voorbeeld van het gebruik ervan: vis in de rivier
Neem aan dat het aantal vissen in een rivier wordt bestudeerd, wiens oevers de grens van het systeem vertegenwoordigen. Het is bekend dat gemiddeld 568 vissen per jaar binnenkomen, 424 worden geboren (genereren), 353 sterven (consumeren) en 236 emigreren of vertrekken.
Het toepassen van de algemene vergelijking dan heb je:
568 + 424 - 353 - 236 = 403
Dit betekent dat ze door 403 vissen zich ophopen in de rivier; dat wil zeggen, per jaar verrijkt de rivier meer vissen. Als ik een negatieve waarde had, zou dit betekenen dat het aantal vissen afneemt, misschien tot negatieve milieueffecten.
Het kan u van dienst zijn: Ionische kracht: eenheden, hoe u het kunt berekenen, voorbeeldenJongens
Uit de algemene vergelijking kunt u denken dat er vier vergelijkingen zijn voor verschillende soorten chemische processen. Het evenwicht is echter in twee soorten onderverdeeld volgens een ander criterium: tijd.
Differentiaal evenwicht
In de balans tussen differentiële materie is er op een bepaalde tijd of tijd het bedrag van de componenten binnen een systeem. Deze massale hoeveelheden worden uitgedrukt met eenheden van tijd en vertegenwoordigen daarom snelheden; Bijvoorbeeld kg/h, die aangeeft hoeveel kilometer binnenkomen, verlaten, accumuleren, genereren of consumeren in een uur.
Zodat er massa (of volumetrische stromen zijn, met de dichtheid bij de hand), moet het systeem over het algemeen open zijn.
Integrale balans
Wanneer het systeem wordt gesloten, zoals bij de reacties die worden uitgevoerd in intermitterende reactoren (batchtype), interesseren de massa's van zijn componenten meestal voor en na het proces; dat wil zeggen, een van de eerste en laatste T -tijden.
Daarom worden de hoeveelheden uitgedrukt als louter massa's en geen snelheden. Dit type evenwicht wordt mentaal gemaakt wanneer een blender wordt gebruikt: de massa van de ingrediënten die binnenkomen moet gelijk zijn aan de overgelaten na de motor.
Voorbeeldoefening
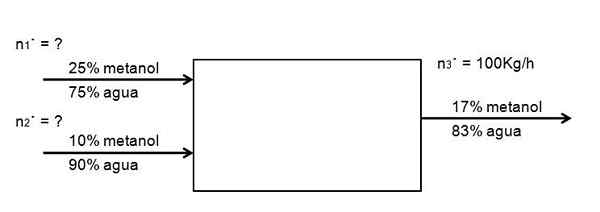
Het is gewenst om een stroom van een 25% methanoloplossing in water te verdunnen, met een andere concentratie van 10%, meer verdund, op een zodanige manier dat 100 kg/u wordt gegenereerd uit een 17% methanoloplossing. Hoeveel van beide methanoloplossingen, met 25 en 10%, moeten het systeem per uur invoeren om dit te bereiken? Neem aan dat het systeem zich in stationaire staat bevindt
Kan u van dienst zijn: verzepingHet volgende diagram is een voorbeeld van de verklaring:
 Stroomdiagram voor de verdunning van de verdunning van de methanoloplossing. Bron: Gabriel Bolívar.
Stroomdiagram voor de verdunning van de verdunning van de methanoloplossing. Bron: Gabriel Bolívar. Er is geen chemische reactie, dus de hoeveelheid methanol die binnenkomt, moet gelijk zijn aan degene die uitkomt:
ENMethanol = SMethanol
0,25 n1· + 0,10 n2· = 0,17 n3·
Alleen de waarde van N is bekend3·. De rest zijn onbekenden. Om deze vergelijking van twee onbekenden op te lossen, is een ander evenwicht nodig: die van het water. Dan is het maken van dezelfde balans voor water:
0,75 n1· + 0,90 n2· = 0,83 n3·
De waarde van N wordt gewist voor water1· (Het kan ook n zijn2·):
N1· = (83 kg/h - 0,90n2·)/ (0,75)
Vervangen dan n1· In de materie -balansvergelijking voor methanol, en het oplossen van n2· Je hebt:
0,25 [(83 kg/h - 0,90n2·)/ (0,75)] + 0,10 n2· = 0,17 (100 kg/h)
N2· = 53,33 kg/h
En om n te verkrijgen1· gewoon aftrekken:
N1· = (100-53,33) kg/h
= 46,67 kg/h
Daarom moet u per uur het systeem van 46,67 kg invoeren van 25%methanoloplossing en 53,33 kg van de 10%oplossing.
Referenties
- Felder en Rousseau. (2000). Elementaire principes van chemische processen. (Tweede druk.)). Addison Wesley.
- Fernández Germán. (20 oktober 2012). Definitie van materie -balans. Hersteld van: industrie.netto

