Thermische alcoholstructuur, eigenschappen, risico's en gebruik
- 1801
- 180
- Lonnie Rohan
Hij Thermische alcohol Het is een organische verbinding waarvan de formule is (ch3))3Coh of t-buoh. Dit is de eenvoudigste tertiaire alcohol van allemaal. Afhankelijk van de omgevingstemperatuur wordt het gepresenteerd als een vaste of vloeibare kleurloos. In de onderste afbeelding tonen ze bijvoorbeeld hun kleurloze kristallen.
Deze alcohol is geen substraat voor het enzymcoholische dehydrogenase, of voor de peroxidasische activiteit van catalase, dus wordt het geclassificeerd als een niet -metaboliseerbare alcohol. Vanwege zijn biochemische eigenschappen wordt gedacht dat het nuttig zou kunnen zijn bij de detectie van hydroxillen in vivo in intacte cellen.

Het is een van de vier isomeren van isobutilische alcohol, die de minder gevoelige isomeer voor oxidatie is en de minst reactief. In de natuur wordt het gevonden in de kikkererwten en in cassave of cassave, wortel die wordt gefermenteerd om alcoholische dranken te produceren.
Thermische alcohol is zeer oplosbaar in water en organische oplosmiddelen. Het belangrijkste gebruik ervan is als een oplosmiddel, die die rol vervult in de uitwerking van kunststoffen, parfums, remversies van schilderen, enz.
Zoals veel organische verbindingen, is het een beetje giftig, maar in hoge doses heeft het een verdovend effect, gekenmerkt door hoofdpijn, vahidos, duizeligheid, duizeligheid en verval.
[TOC]
Thermische alcoholstructuur
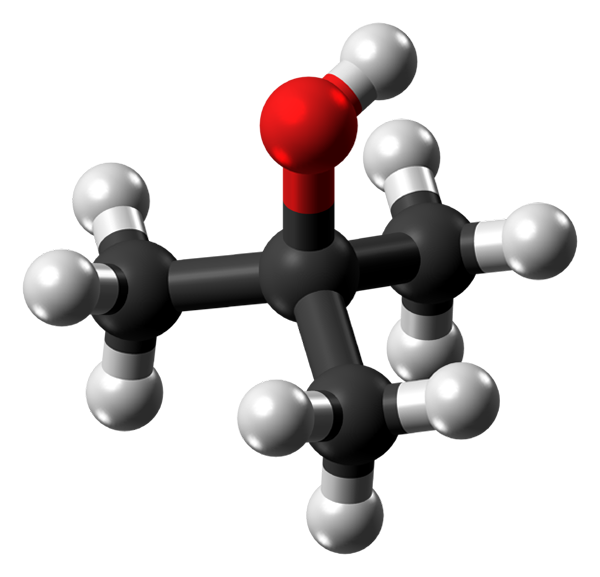
 Thermische alcoholmolecuul. Bron: Jynto via Wikipedia.
Thermische alcoholmolecuul. Bron: Jynto via Wikipedia. In het bovenste beeld heb je de moleculaire structuur van thermische alcohol met een model van bollen en staven. Het hele molecuul heeft een wereldwijde tetraëdrische geometrie, met de 3e koolstof in het midden en de groepen3 En oh in zijn hoekpunten.
Als u deze structuur waarneemt, wordt het wel begrepen waarom deze alcohol tertiair is: de koolstof van het centrum is gekoppeld aan drie andere koolstofatomen. Doorgaan met de tetraëder, kan het onderste deel ervan worden beschouwd als apolar, terwijl het bovenste hoekpunt, polar.
Het kan u van dienst zijn: fehling -reactie: voorbereidingen, actieve agenten, voorbeelden, gebruikIn dit hoekpunt is de OH-groep, die een permanente dipool creëert en ook T-BuOH-moleculen mogelijk maakt om te interageren via waterstofbruggen; Op dezelfde manier als bij watermoleculen en andere polaire stoffen.
In T-Buah-kristallen zijn deze waterstofbruggen een sleutelfactor voor de moleculen om samen te blijven; Hoewel er niet te veel informatie is over wat de kristallijne structuur van deze alcohol is.
Wanneer de OH -groep zo dichtbij is en omgeven door de Apolar Groups Cho3, Watermoleculen slagen erin om bijna alle alcohol te hydrateren terwijl ze interactie hebben met OH. Dit zou zijn grote oplosbaarheid in water verklaren.
Eigenschappen
Chemische namen
-Thermische alcohol
-Ter-butanol
-2- Methyl-2-propanol
-2-methylpropan-2-ol.
Moleculaire formule
C4H10O O (Cho3))3Coh.
Molecuulgewicht
74,123 g/mol.
Fysieke beschrijving
Kleurloze vaste of kleurloze vloeistof, afhankelijk van de omgevingstemperatuur, omdat het smeltpunt 77,9 ºF (25,4 ºC) is. Boven 77,9 ºF is een vloeistof.
Geur
Vergelijkbaar met de kamfer.
Kookpunt
82.4 ºC.
Smeltpunt
77,9 ºF (25,4 ºC).
ontstekingspunt
52 ºF (11 ºC). GESLOTEN BEKER.
Oplosbaarheid in water
Erg oplosbaar. In feite, ongeacht de verhoudingen, is deze alcohol altijd mengbaar met water.
Oplosbaarheid in biologische oplosmiddelen
Mengbaar met ethanol, ethylether en oplosbaar in chloroform.
Dikte
0,78 g/cm3.
Stoomdichtheid
2,55 (met luchtrelatie = 1).
Dampdruk
4.1 kPa bij 20 ºC.
Octanol/waterpartitiecoëfficiënt
Log p = 0,35.
Thermostabiliteit
Onstabiel in warmte
Zelfsturingstemperatuur
896 ºF (470 ºC).
Kan u van dienst zijn: aliquot (chemie)Ontleding
Wanneer verwarmd kan koolstof- en isobutileenmonoxidedampen afgeven.
Verdampingswarmte
39.07 kJ/mol.
Calorische capaciteit
215,37 JK-1mol-1.
Training Enthalpy
-360.04 tot -358.36 kjmol-1.
Bewaar temperatuur
2-8 ºC.
Stabiliteit
Het is stabiel, maar onverenigbaar met sterke oxiderende middelen, koper, koperlegeringen, alkalische en aluminiummetalen.
Ionisatiepotentieel
9.70 eV.
Geurdrempel
219 mg/m3 (lage geur).
Brekingsindex
1.382 tot 25 ° C.
Dissociatie constant
PKA = 19.20.
Maximale stoomconcentratie
5,53 % bij 25 ºC.
Reacties
-Het is onaangenaam door een sterke basis om een alcoxide -anion te veroorzaken; In het bijzonder een terbutoxide, (ch3))3CO-.
-Thermische alcohol reageert met waterstofchloride om het terbutylchloride te vormen.
(Ch3))3Coh +hcl => (ch3))3CCL +H2OF
Tertiaire alcoholen hebben een grotere reactiviteit met waterstofhalogeniden dan secundaire en primaire alcoholen.
Risico's
Thermische alcohol per contact met de huid produceert milde laesies, zoals erytheem en niet -serieuze hyperemie. Bovendien kruist het niet de huid. Integendeel, in de ogen produceert het ernstige irritatie.
Wanneer het wordt ingeademd, produceert het irritatie in de neus, keel en bronchi. In het geval van hoge blootstelling, verdovende effecten, kunnen een toestand van slaperigheid, evenals fades, vahidos en hoofdpijn optreden.
Deze alcohol is een experimenteel teratogeen middel, dus het is waargenomen bij dieren die het uiterlijk van aangeboren aandoeningen kunnen beïnvloeden.
Wat betreft de opslag, zijn de vloeistof en dampen ontvlambaar, en daarom kan het in bepaalde omstandigheden branden en explosies genereren.
OSHA heeft een concentratielimiet van 100 ppm vastgesteld (300 mg/m3) Voor een dag van 8 uur.
Kan u van dienst zijn: percentageoplossingenToepassingen
-Thermische alcohol wordt gebruikt voor de opname van de thermische groep in organische verbindingen, om oplosbare oliën in oliën te bereiden, en trinitro-tter-butletolueen, een kunstmatige musk. Bovendien vormt het een eerste materiaal voor de bereiding van peroxiden.
-Het is goedgekeurd door de FDA als een splijtermiddel om te gebruiken in componenten en plastic materialen die in contact zijn met voedsel. Het is gebruikt bij de uitwerking van fruit, kunststoffen en lacas essenties.
-Het is een intermediair voor de productie van terbutyl- en tributilfenolchloride. Het fungeert als een denatureringsagent van ethanol.
-Dienen voor de vervaardiging van flotatie -middelen, als een organisch oplosmiddel om schilderijen te verwijderen, en om essenties op te lossen die in parfums worden gebruikt.
-Het wordt gebruikt als een octaanversterker in benzine; brandstof- en brandstofadditief; Oplosmiddel om te gebruiken bij het reinigen en als een ellendig.
-Thermische alcohol is een intermediair middel bij de productie van de terbutylmetylether (MTBE) en tributilethylether (ETBE), die respectievelijk reageren met methanol en ethanol.
-Het werkt ook op dezelfde manier bij de productie van tributylhydroperoxide (TBHP) door reactie met waterstofperoxide.
-Het wordt gebruikt als een reagens in het proces dat bekend staat als Curtius Reareglo.
Referenties
- Graham Solomons T.W., Craig B. Friteuse. (2011). Organische chemie. Amines. (10e Editie.)). Wiley Plus.
- Wikipedia. (2019). Tert-butylalcohol. Opgehaald uit: in.Wikipedia.borg
- CommonorganicChemistry. (S.F.)). T-butanol. Hersteld van: CommonorganicChemistry.com
- Nationaal centrum voor biotechnologie -informatie. (2019). Tert Butanol. PubChem -database. Hersteld van: pubchem.NCBI.NLM.NIH.Gov
- Carey F. NAAR. (2008). Organische chemie. (Zesde editie). MC Graw Hill.
- « Attitudinale inhoud kenmerken en voorbeelden
- Wat moeten kinderen en jongeren uit de 21ste eeuw leren handelen in de wereld van vandaag? »

