Arseentrioxide (As2O3)
- 2420
- 251
- Aaron Okuneva
Hij arseentrioxide Het is een anorganische verbinding waarvan de chemische formule zo is2OF3. Arseen in zijn metalen toestand wordt snel omgezet in dit oxide, dat een zeer giftig gif is dat acute en chronische manifestaties kan hebben.
Omdat het arseen- en zuurstofelementen van blok P is, met een relatief laag elektronegativiteitsverschil, wordt de aas verwacht2OF3 samengesteld zijn uit covalente aard; dat wil zeggen dat de AS-O-bindingen overheersen in hun vaste stof, over elektrostatische interacties tussen de ACE-ionen3+ I2-.
Acute vergiftiging met arseentrioxide wordt geproduceerd door inname of inhalatie, die de belangrijkste manifestaties hiervan zijn: sterke gastro -intestinale aandoeningen, krampen, ineenstorting van de bloedsomloop en longoedeem.
Ondanks zijn toxiciteit is het echter industrieel gebruikt; Bijvoorbeeld in het behoud van hout, in de uitwerking van pigmenten, halfgeleiders, enz. Evenzo werd het eerder gebruikt bij de behandeling van talloze ziekten.
Arseentrioxide is een amfoterische verbinding, oplosbaar in zuren en verdunde alkalis, onoplosbaar in organische oplosmiddelen, en relatief oplosbaar in water. Het wordt gepresenteerd als een solide (superieure afbeelding), met twee kristallijne vormen: kubiek en monoklinisch.
Arseentrioxidestructuur
Claudetita
Bij kamertemperatuur, de aas2OF3 Kristalliseert in twee monokliene polymorfen, beide gevonden in het Claudetita -mineraal. In hen zijn er trigonale piramide -eenheden aso3, die binden door hun zuurstofatomen om alleen de elektronische tekort aan de eenheid te compenseren.
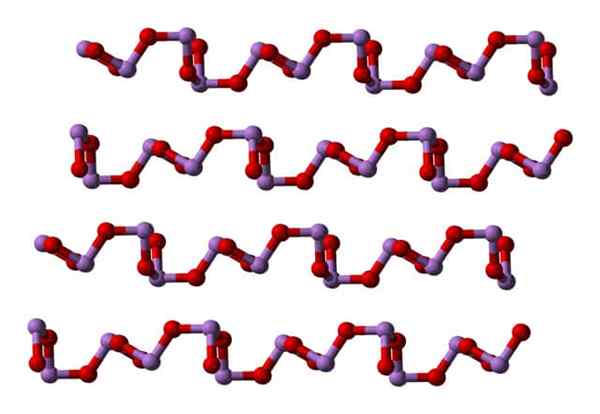
In een polymorph de ASO -eenheden3 Ze zijn gekoppelde vormige rijen (Claudetita I), en in de andere zijn ze gekoppeld alsof ze een netwerk weven (Claudetita II):
Kan u van dienst zijn: agglomerante materialen Claudetita polymorfo structuur i. Bron: Ben Mills [Public Domain].
Claudetita polymorfo structuur i. Bron: Ben Mills [Public Domain].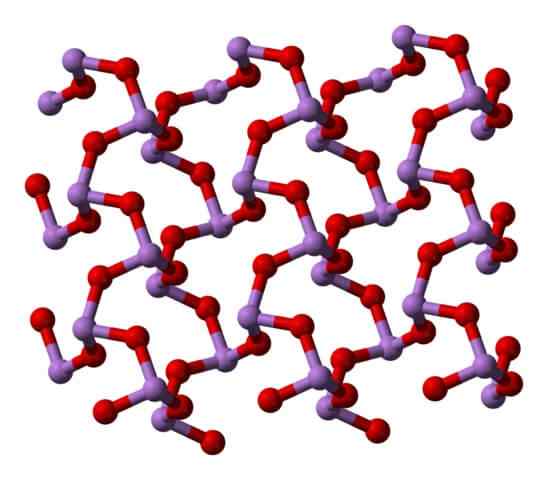 Claudetita polymorfo structuur II. Bron: Ben Mills [Public Domain].
Claudetita polymorfo structuur II. Bron: Ben Mills [Public Domain].
Vloeistof en gasvormig
Wanneer al die structuren die monokliene kristallen definiëren, worden verwarmd, zijn de trillingen zodanig dat verschillende AS-O-links worden verbroken en uiteindelijk een kleiner molecuul heerst:4OF6. In het onderste beeld wordt de structuur weergegeven.
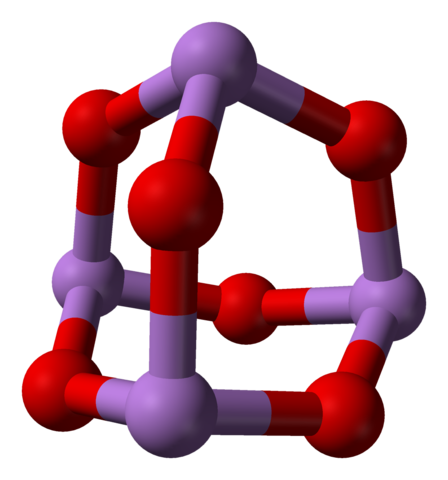 AS4O6 Molecuul. Bron: Ben Mills [Public Domain]
AS4O6 Molecuul. Bron: Ben Mills [Public Domain] Men zou kunnen zeggen dat het bestaat uit een dag van As2OF3. De stabiliteit is zodanig dat het 800 ° C ondersteunt in een gasfase; Maar boven deze temperatuur is het gefragmenteerd als moleculen2OF3.
Arsenoliet
Hetzelfde als4OF6 kan met elkaar communiceren om te kristalliseren in een kubieke vaste stof, waarvan de structuur wordt gevonden in het arsenolietmineraal.
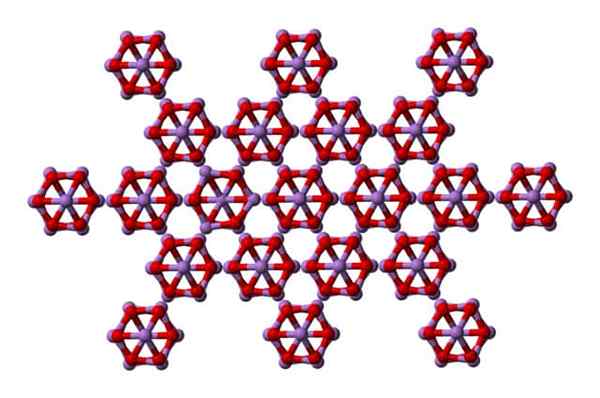 As4O6 -moleculen in de arsenoliet -vaste stof. Bron: Ben Mills [Public Domain]
As4O6 -moleculen in de arsenoliet -vaste stof. Bron: Ben Mills [Public Domain] Merk op dat in de afbeelding de structuur wordt getoond uit een hoger vlak. In vergelijking met Claudetita is het structurele verschil met arsenoliet duidelijk. Hier zijn het discrete moleculen4OF6 dat eenheden worden gehandhaafd door van der Waals Forces.
Eigenschappen
Ruilnamen
-Arsenoliet
-Arsodent
-Trisenox
-Claudetita
Molecuulgewicht
197.84 g/mol.
Fysiek uiterlijk
-Witte kubieke kristallen (arsenoliet).
-Monoklinische kleurloze kristallen (Claudetita).
-Wit of transparante vaste, glasachtige, amorfe knobbels of kristallijn stof.
Geur
Toilet.
Smaak
Smaakloos.
Kookpunt
460 ºC.
Smeltpunt
-313 ºC (Claudetita).
-274 ºC (arsenoliet).
ontstekingspunt
485 º C (sublima).
Oplosbaarheid in water
17 g/l A 18 ºC (20 g/L A 25 ºC).
Oplosbaarheid
Oplosbaar zuur (vooral in zoutzuur) en alkalie. Praktisch onoplosbaar in chloroform en ether.
Kan u van dienst zijn: centrifugatieDikte
-3,85 g/cm3 (kubieke kristallen);
-4.15 g/cm3 (rhombische kristallen).
Dampdruk
2,47 · 10-4 mmHg bij 25 ºC.
Ontleding
Het is geen brandstof, maar vanwege de opwarming kan het een giftige rook veroorzaken die Arsina kan omvatten.
Corrosiviteit
In aanwezigheid van vocht kan het corrosief zijn voor metalen.
Verdampingswarmte
77 kJ/mol.
Dissociatieconstante (ka)
1.1 · 10-4 bij 25 ºC.
Brekingsindex
-1.755 (arsenoliet)
-1.92-2.01 (Claudetita).
Reactiviteit
-Arseentrioxide is een amfoterische verbinding, maar het werkt bij voorkeur als zuur.
-Het kan reageren met zoutzuur of met fluorhorisch zuur, waardoor arseen triflouride of arseen triflouur wordt gevormd.
-Het reageert ook met sterke oxidanten, zoals salpeterzuur, die arseenzuur en stikstofoxide veroorzaken.
-Arseentrioxide kan reageren met salpeterzuur, waardoor arsine- of arseenelement wordt geproduceerd, afhankelijk van de reactieomstandigheden.
Ace2OF3 + 6 Zn +12 HNO3 => 2 as3 + 6 Zn (nee3))2 + 3 H2OF.
Deze reactie diende als basis voor het creëren van de moerastest, gebruikt voor de detectie van arseenvergiftiging.
Nomenclatuur
Bij2OF3 Het kan worden aangesteld volgens de volgende nomenclatures, wetende dat Arseen werkt met Valencia +3:
-Arsenioso -oxide (traditionele nomenclatuur).
-Arseenoxide (III) (voorraadnomenclatuur).
-Diarseentrioxide (systematische nomenclatuur).
Toepassingen
Industriëlen
-Het wordt gebruikt bij de productie van glas, met name als een vervagingsmiddel. Het wordt ook gebruikt bij de uitwerking van keramiek, elektronische producten en vuurwerk.
-Het wordt toegevoegd als een kleine component aan op koper gebaseerde legeringen, om de corrosieweerstand van legeringsmetalen te vergroten.
-De As2OF3 Het is het uitgangsmateriaal voor de bereiding van elementair arseen, om elektrische gewrichten te verbeteren en voor de uitwerking van semiconductors van Arsenuros
Het kan u van dienst zijn: Nucleaire chemie: geschiedenis, studiegebied, gebieden, toepassingen-De As2OF3, Naast koperarseniato worden ze gebruikt als houten conserveermiddelen. Het werd gebruikt in combinatie met koperacetaat voor de uitwerking van het groene pigment van Parijs, gebruikt bij de uitwerking van schilderijen en raticides.
Artsen
-Arseentrioxide is een verbinding die al eeuwenlang wordt gebruikt bij de behandeling van talloze ziekten. Het werd gebruikt als tonic bij de behandeling van voedingsstoornissen, neuralgie, reuma, artritis, astma, Korea, malaria, syfilis en tuberculose.
-Evenzo is het gebruikt bij de lokale behandeling van huidziekten, die worden gebruikt om enkele oppervlakkige epitheliomen te vernietigen.
-Fowler's oplossing werd gebruikt bij de behandeling van huidziekten en leukemie. Het gebruik van dit medicijn wordt stopgezet.
-In de jaren zeventig ontwikkelde de Chinese onderzoeker Zhang Tingdong een onderzoek naar het gebruik van arseentrioxide bij de behandeling van acute promielocytische leukemie (APL). Die leidde tot de productie van het Trisenox -medicijn, dat werd goedgekeurd door de FDA van de Verenigde Staten.
-Trisenox is gebruikt bij PLA -patiënten die niet reageren op de behandeling van "eerste lijn", bestaande uit alle transzuurzuur (ATTRA). Het is aangetoond dat arseentrioxide kankercellen induceert om apoptose te lijden.
-Trisenox wordt gebruikt als een cytostatisch bij de behandeling van refractaire promiselocytische subtype (m3) van app.
Referenties
- Arseentrioxide. De Sevier. Opgehaald uit: Scientedirect.com
- Arseen (iii) oxide. Hersteld van: pubchem.NCBI.NLM.NIH.Gov

