Tiocyanaatvorming, structuur, typen, gebruik
- 2539
- 808
- Dr. Rickey Hudson
Hij Tiocianato Het is een anorganisch anion waarvan de formule SCN is-. Dit is wat bekend is bij pseudohalogenuro, omdat het chemische gedrag ervan lijkt op dat van halogenuros, dat wil zeggen fluoride, chloride, enz. Het is ook bekend onder de naam Rodanida, hoewel dit momenteel minder vaak wordt gebruikt.
Tiocianaat is een merkwaardige soort, omdat het aan de grens tussen organische en anorganische chemie is geplaatst. Perfect maakt het deel uit van zowel organische als anorganische verbindingen, die alleen variërend van de manier waarop het is gekoppeld of interactie. Deze pseudohalogenuro heeft een sterke biochemische link met cyanide -ionen en hun metabolisme.
 Tiocyanaatanion vertegenwoordigd door een full space -model. Bron: Benjah-BMM27 / Public Domain.
Tiocyanaatanion vertegenwoordigd door een full space -model. Bron: Benjah-BMM27 / Public Domain. In het superieure beeld is er een weergave van de SCN- met behulp van een full space -model. De gele bol komt overeen met het zwavelatoom, terwijl de zwarte en blauwachtige respectievelijk koolstof- en stikstofatomen zijn. Tiocianaat heeft een geoxygeneerde broer: Cyanato, OCN-, waarin het zwavelatoom wordt vervangen door een zuurstof.
Kalium Tiocianaat, KSCN, is een van de meest representatieve voorbeelden voor deze pseudohalogenuro. Aan de andere kant zijn er in organische chemie Tiociaanse wiens algemene formules RSCN zijn, zoals methyl tiocianaat, cho3SCN.
[TOC]
Opleiding
Reactie tussen cyanide en zwavel
De SCN -formule- Hiermee kunt u een glimp opvangen dat de synthese ervan is gebaseerd op de cyanidereactie, CN-, Met een soort die zwavelatomen doneert. Inderdaad, cyanide kan goed reageren met elementaire zwavel, s8, of met de tiosulfate anionen, s2OF32- Om tiocyanaat te produceren:
8 CN- + S8 → 8 SCN-
CN- + S2OF32- → SCN- + S2OF32-
Kan u van dienst zijn: CO2 LinktypeDe tweede reactie wordt echter gekatalyseerd door een enzymsysteem bestaande uit zwavel -thiosulfaat. Ons lichaam heeft deze enzymen, en daarom zijn we in staat om cyaniden te metaboliseren die afkomstig zijn van cyanoglucosiden (koolhydraten die de CN -groep hebben). Op deze manier verwijdert het lichaam de schadelijke CN-, die interfereren met cellulaire ademhalingsprocessen.
Tiocianaten worden opgelost in speeksel en, in mindere mate, in plasma. Hun concentratieniveaus onthullen hoe blootgesteld zijn aan cyaniden, hetzij vanwege een overmatige inname van voedingsmiddelen die het in hun natuurlijke vorm bevatten (noten, amandelen, peulvruchten, linaza's, enz.), of door langdurige inademing van de rook van sigaretten en tabak.
Tiocische zuurneutralisatie
De SCN- Het kan worden verkregen door neutralisatie van zijn zure vorm: tiocianinezuur, HSCN of isotiocyanic, HNCS. Afhankelijk van de gebruikte basis zal ook een Tiociaanse zout worden verkregen.
Structuur
Links
 Tiociaanse resonantiestructuren. Bron: Ben Mills via Wikipedia.
Tiociaanse resonantiestructuren. Bron: Ben Mills via Wikipedia. Het superieure beeld laat zien hoe de negatieve belasting van de SCN wordt verdeeld-. Merk op dat alle atomen SP -hybridisatie hebben2, Dus ze bevinden zich in dezelfde lijn.
Het elektronenpaar kan goed gelegen zijn op het stikstofatoom, of op het zwavelatoom. Dit feit verklaart een belangrijk kenmerk van Tiocianaat: het is een bident ligand, dat wil zeggen in staat om op twee verschillende manieren te koppelen.
Isomería
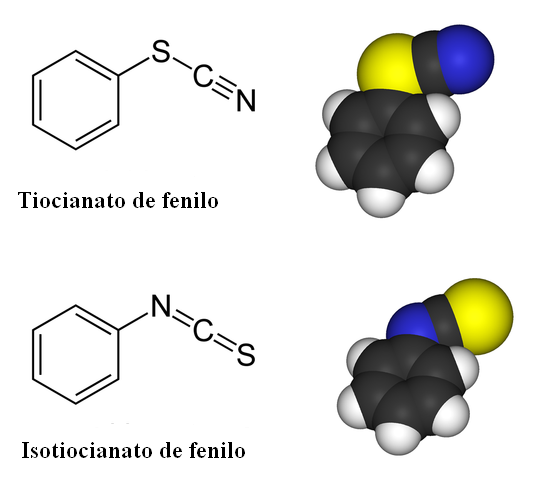
 Liaison -isomerie voor fenyltiocyanaat. Bron: Benjah-BMM27 / Public Domain
Liaison -isomerie voor fenyltiocyanaat. Bron: Benjah-BMM27 / Public Domain In Tiocianaatverbindingen is de link -isomeer aanwezig. Zoals te zien is in het superieure beeld, de SCN- Het kan worden gekoppeld aan een benzene ring of fenylgroep door zijn zwavelatoom of stikstofatoom. Wanneer gekoppeld aan de S, wordt het Tiociaanaat genoemd; Terwijl wanneer gekoppeld aan de n, wordt het isotiocianaat genoemd.
Kan u van dienst zijn: Stanislao CannizzaroMerk op hoe -scn of -ncs eruit zien als lineaire fragmenten. Deze lineaire geometrie blijft ongewijzigd in zowel organische als anorganische tiociaanaten.
De -cs -binding is sterker dan -Scn, omdat stikstof, omdat deze kleiner is, de negatieve belasting van het elektronpaar waarmee de covalente binding zal vormen.
Interacties
SCN anionen- Ze kunnen niet met elkaar communiceren vanwege elektrostatische afstotingen. Daarom hebben ze kationen nodig zodat ze elektrostatisch kunnen communiceren en dus een kristal kunnen "bouwen". Anorganische tiociaan zijn verbindingen in ionische essentie.
Ondertussen zijn hun interacties voor organische Tiocianen gebaseerd op de krachten van van der Waals; Vooral die van een dipool-dipolo-type. De SCN -groep is, zoals gekoppeld, polair en draagt daarom bij aan een toename van de polariteit van de verbinding. Het is duidelijk dat dipool-dipolo-interacties zwakker zijn dan ionische attracties, bijvoorbeeld aanwezig bij de KSCN+SCN-)).
Organische Tiociaanse
Organische tiocianen worden weergegeven met de RSCN -formule. Aan de andere kant hebben we, met contact isomeria, ook de isoocianaten, RNC's.
Het is dus voldoende om R te vervangen door alkyl- of aromatische moleculaire fragmenten om verschillende verbindingen te verkrijgen. Bijvoorbeeld cho3Ch2SCN is ethyl tiocianaat. In de vorige sectie r6H5SCN of φ-scn.
Anorganische tiociaanjes
Anorganische tiocyanaten worden beschouwd als zouten van tiocianinezuur, HSCN, en kunnen worden weergegeven als MSCN, waarbij M een metaalkation of ammoniumkation is. We hebben dus bijvoorbeeld:
-NASCN, natriumtiocyanaat
-NH4SCN, ammonium tiocianaat
Het kan u van dienst zijn: verschillen tussen organische en anorganische verbindingen-Faith (SCN)3, Ferrisch tiocyanaat
Veel anorganische tiocianen zijn kleurloze vaste zouten.
Aan de andere kant hebben we ook de Tiocianaatcomplexen in oplossing. Bijvoorbeeld een waterige oplossing die geloofsionen bevat3+ zal worden voltooid met SCN -ionen- Om [geloof (ncs) (h te vormen2OF)5]2+, dat is bloedrood.
Evenzo, de SCN- Het is in staat om te complexen met andere metalen kationen, zoals CO2+, Cu2+ jij ook4+, Elk uit een kleurrijk complex.
Toepassingen
Het SCN -anion- Het wordt gebruikt voor fotometrische metaalbepalingen in waterige oplossingen. Deze methode is precies gebaseerd op de meting van de absorptie van de kleurrijke complexen van tiociaanjes met metalen.
Uit dit specifieke gebruik zijn anderen net zo gevarieerd als de Tiociaanse die bestaan.
Organische tiociaan zijn meer dan wat dan ook bestemd als structurele blokken voor de synthese van zwavelverbindingen die in de geneeskunde worden gebruikt.
Aan de andere kant worden anorganische tiociaanse die kleuringen hebben gebruikt voor de textielindustrie of als additieven voor bootschilderijen. Ook omdat het goede SCN -iondonoren zijn-, Ze zijn vereist voor de productie van insecticiden en fungiciden.
Van de Tiociaanse zijn de meest populaire de NASCN en KSCN, beide zeer gevraagd in de geneesmiddelen, constructies, elektronische en agrochemische industrie.
Referenties
- Morrison, r. T. en Boyd, R, n. (1987). Organische chemie. 5e editie. Redactionele addison-wesley inter-Amerikaan.
- Carey F. (2008). Organische chemie. (Zesde editie). MC Graw Hill.
- Graham Solomons T.W., Craig B. Friteuse. (2011). Organische chemie. (10e editie.)). Wiley Plus.
- Shiver & Atkins. (2008). Anorganische scheikunde. (Vierde druk). MC Graw Hill.
- Wikipedia. (2020). Thiocyanaat. Opgehaald uit: in.Wikipedia.borg
- Nationaal centrum voor biotechnologie -informatie. (2020). Thiocyanaat. PubChem -database., CID = 9322. Hersteld van: pubchem.NCBI.NLM.NIH.Gov
- Elsevier B.V. (2020). Thiocyanaat. Wetenschappelijk. Opgehaald uit: Scientedirect.com
- Nouryon. (2020). Thiocyanaat. Opgehaald uit: zwavelurderivaten.Nouryon.com
- Riedel, K., Hagundan, h.W. En Scherer, G. (2013). Thiocyanaat in plasma en speeksel [Biomonitoring Methods, 2013]. In de Mak - Collection for Occupational Health and Safety (eds and). Doi: 10.1002/3527600418.BI5712Sale0013
- « Journalistische teksten kenmerken, structuur, typen, voorbeelden
- Gespecialiseerde tekstenkenmerken, structuur, typen, voorbeelden »

