Osmoseproces, typen, verschillen met diffusie en voorbeelden
- 814
- 18
- Glen Armstrong
De osmose Het is een passief fenomeen van waterverplaatsing door een membraan. Dit kan een celmembraan, een epitheel of een kunstmatig membraan zijn. Het water wordt gemobiliseerd uit een laag osmotisch drukgebied (of waar het water overvloediger is) naar het gebied met grotere osmotische druk (of waar het water minder overvloedig is).
Dit proces is van biologische relevantie en orkest een reeks fysiologische processen, zowel bij dieren als bij planten.
 Bron: OpenTax [CC door 4.0 (https: // creativeCommons.Org/licenties/door/4.0)]
Bron: OpenTax [CC door 4.0 (https: // creativeCommons.Org/licenties/door/4.0)] De eerste onderzoeker bij het melden van het osmotische fenomeen was Abbé Jean Antoine Nollet. In 1748 werkte Nollet met membranen van dierencellen en merkte op dat wanneer zuiver water aan de ene kant van het membraan werd geplaatst en aan de andere kant een oplossing met verdunde elektrolyten, het water naar het gebied bewoog met opgeloste stof naar het gebied.
Aldus werd de doorgang van water ten gunste van de concentratiegradiënt beschreven en werd osmose genoemd. De term komt van Griekse wortels Osmos, Wat betekent het duw.
In 1877 voerde Wilhelm Pfeller de eerste studies uit naar osmotische druk. Het experimentele ontwerp omvatte het gebruik van een "membraan" van koperferrocyanide op het oppervlak van een poreus kleiplas, wat aanleiding gaf tot een membraan dat de doorgang van watermoleculen mogelijk maakte.
De kunstmatige membranen van Pfeller waren sterk genoeg om significante osmotische druk te weerstaan en niet in te storten. Deze onderzoeker zou kunnen concluderen dat de osmotische druk evenredig is met de opgeloste concentratie.
[TOC]
Proces
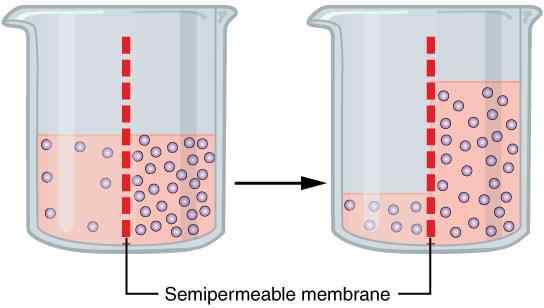
De beweging van water door een membraan van een lage concentratiezone naar een hoge concentratiezone wordt osmose genoemd. Dit proces treedt op uit een gebied met de laagste osmotische druk naar de hoogste osmotische druk.
In het begin kan deze verklaring verwarrend zijn - en zelfs tegenstrijdig. We zijn gewend aan de passieve beweging van "Alto to Bajo". Warmte kan bijvoorbeeld van hoge tot lage temperaturen zijn, glucose diffundeert van gebieden met hoge concentratie naar minder geconcentreerde gebieden, enzovoort,.
Zoals we al zeiden, beweegt het water dat wordt ervaren door het fenomeen van osmose van lage druk naar hoge drukken. Dit gebeurt omdat water overvloediger is per volume -eenheid waar de opgeloste stof minder overvloedig is.
Dat wil zeggen, tijdens de osmose wordt het water gemobiliseerd waar zij (water) is overvloediger wanneer het minder overvloedig is. Daarom moet het fenomeen worden begrepen vanuit het perspectief van water.
Het is belangrijk om te onthouden dat osmose de beweging van water door de membranen en heeft geen invloed op de beweging van opgeloste stoffen rechtstreeks. Wanneer opgeloste stoffen zich verspreiden, doen ze dit na de gradiënten van hun eigen chemische concentratie. Alleen het water volgt de gradiënt van de osmotische drukconcentratie.
Kan u van dienst zijn: Biuret: foundation, reagentia, procedure, gebruikOsmotische druk
Druk?
Een van de meest verwarde aspecten bij het begrijpen van het osmoseproces is het gebruik van het woord Druk. Om verbijster te voorkomen.
Een concentratieglucoseoplossing van 1 m heeft bijvoorbeeld een osmotische druk van 22 atm. De oplossing "exploiteert" echter geen glazen flessen en kan op dezelfde manier worden opgeslagen als zuiver water omdat een geïsoleerde oplossing zich niet vertaalt in hydrostatische druk.
De term druk wordt alleen gebruikt door een historisch ongeval, omdat de eerste wetenschappers die deze fenomenen bestudeerden fysiek en chemisch waren.
Dus als twee oplossingen die verschillen in hun osmotische druk worden gescheiden door een membraan, wordt er hydrostatische druk gemaakt.
Osmotische en hydrostatische druk
Het osmoseproces leidt tot de vorming van hydrostatische druk. Het drukverschil leidt tot het niveau van de meest geconcentreerde oplossing, terwijl het water zich hiernaar verspreidt. De toename van het continue waterniveau totdat de netto snelheid van de waterbeweging gelijk is aan nul.
Een netto stroom wordt bereikt wanneer de hydrostatische druk in compartiment II voldoende is om de watermoleculen te dwingen terug te gaan naar gedrag I, met dezelfde snelheid dat osmose ervoor zorgt dat de moleculen van compartiment I naar de II naar de II naar.
Naar de waterdruk veroorzaakt door de deeltjes (van compartiment I tot II) wordt osmotische druk van de oplossing genoemd in compartiment II.
Hoe regelen water in cellen regelen?
Dankzij het osmotische fenomeen kan water passief door celmembranen bewegen. Historisch gezien is het bekend dat dieren een actief watertransportsysteem missen om de stroom van deze stof te regelen.
Actieve opgeloste transportsystemen kunnen echter de richting van waterverplaatsing in een gunstige richting wijzigen. Op deze manier is actief opgeloste transport een manier waarop dieren hun metabole energie gebruiken om watertransport te regelen.
Kwantificering
Er zijn wiskundige formules die het meten van de snelheid waarmee het water de membranen zal oversteken door osmose mogelijk maken. De vergelijking om te berekenen is als volgt:
Het kan u van dienst zijn: Parapatric Speciation: wat is en voorbeeldenWater osmotisch transportsnelheid = k (π1-Π2 / X). Waar π1 en π2 Ze zijn de osmotische druk van de oplossingen aan beide zijden van het membraan en X is de afstand die ze scheidt.
De relatie (π1-Π2 / X) staat bekend als osmotische druk of osmotische drukgradiënt.
De laatste term van de vergelijking is K is de evenredigheidscoëfficiënt die afhankelijk is van de temperatuur- en membraanpermeabiliteit.
Diffusieverschillen
Wat is diffusie?
Diffusie vindt plaats door de willekeurige thermische beweging van opgeloste of gesuspendeerde moleculen, die de dispersie ervan veroorzaakt door de tot de laagste concentraties van concentraties veroorzaakt. De diffusiesnelheid kan worden berekend door de vergelijking van Fick.
Het is een exergonisch proces vanwege de toename van entropie die wordt weergegeven door de willekeurige verdeling van moleculen.
In het geval dat de stof een elektrolytisch is, moet rekening worden gehouden - naast de concentraties - het totale belastingverschil tussen de twee compartimenten.
Osmose is een bepaald geval van verspreiding
Diffusie en osmose zijn geen tegengestelde termen, veel minder wederzijds exclusieve concepten.
Watermoleculen hebben het vermogen om snel door celmembranen te bewegen. Zoals we uitleggen, verspreiden ze zich van een lage concentratiegebied naar een hoge concentratie in een proces dat osmose wordt genoemd.
We lijken vreemd om te praten over "waterconcentratie", maar deze stof gedraagt zich als elke andere stof. Dat wil zeggen, verspreid ten gunste van zijn concentratiegradiënt.
Sommige auteurs gebruiken echter de term "waterverspreiding" als synoniem met osmose. Pas het letterlijk toe op biologische systemen kan verkeerd zijn, omdat is aangetoond dat de osmosesnelheid door biologische membranen groter is dan wat zou worden verwacht door een eenvoudig diffusieproces.
In sommige biologische systemen gaat water door eenvoudige diffusie door het celmembraan. Sommige cellen hebben echter speciale kanalen voor waterpassage. De belangrijkste worden aquaporines genoemd, waardoor de watersnelheid door het membraan wordt verhoogd.
Voorbeelden
Binnen biologische systemen is de beweging van water door celmembranen cruciaal om tientallen fysiologische processen te begrijpen. Enkele voorbeelden zijn:
Osmotische uitwisseling in zoetwatervissen
Een interessant voorbeeld van de rol van dieren osmose is de uitwisseling van water dat optreedt bij vissen die in verse wateren leven.
Kan u van dienst zijn: takken van biochemieDe dieren die zoetwaterlichamen bewonen bevinden zich in een constant wateruitlaat van de rivier of vijver waar ze in hun lichaam leven, omdat de concentratie van bloedplasma en andere lichaamsvloeistoffen een veel hogere concentratie hebben dan die van water.
De vissoorten Carassius auratus Leven in zoetwateromgevingen. Een persoon met een massa van 100 gram kan ongeveer 30 gram water per dag krijgen dankzij de verplaatsing van water in zijn lichaam. De vis heeft systemen - energetisch duur - om continu overtollig water af te komen.
Vloeistofresorptie
In het gastro -intestinale systeem van dieren moet het fenomeen van osmose optreden, zodat het correct werkt. Het geheime spijsverteringskanaal een aanzienlijke hoeveelheid vloeistof (in de orderliters) die door osmose moet worden geresorbeerd door de cellen die de darmen bekleden.
In het geval dat dit systeem zijn werk niet uitvoert, kunnen intense diarree -gebeurtenissen worden gepresenteerd. De verlenging van deze storing kan zich vertalen in de uitdroging van de patiënt.
Turgentie in planten
Het volume water in de cellen hangt af van de concentratie van zowel de binnen- als de externe omgeving, en de stroom wordt georkestreerd door de diffusiefenomenen en osmose.
Als een dierlijke cel (zoals een erytrocyt) wordt geplaatst in een medium dat de watering van de water bevordert, kan deze barsten. Plantencellen hebben daarentegen een wand die hen beschermt tegen osmotische stress.
In feite profiteren niet -houtachtige planten van deze druk die wordt gegenereerd door passieve waterinvoer. Deze druk helpt om turgide te houden tot verschillende plantenorganen, zoals bladeren. Op het moment dat het water uit de cellen begint te komen, verliest de cell.
Referenties
- Cooper, G. M., Hausman, r. EN., & Hausman, r. EN. (2000). De cel: een naderingsmoleculair. ASM Press.
- Eckert, r., Randall, r., & Augustine, g. (1988). Fysiologiedier: mechanismen en aanpassingen. WH Freeman & Co.
- Hill, r. W., Wyse, g. NAAR., Anderson, m., & Anderson, m. (2004). Fysiologiedier. Sinauer Associates.
- Karp, g. (2009). Cel- en moleculaire biologie: concepten en experimenten. John Wiley & Sons.
- Pollard, T. D., Earnshaw, W. C., Lippincott-Schwartz, J., & Johnson, g. (2016). Celbiologie e-boek. Elsevier Health Sciences.
- Schmidt-Nielsen, K. (1997). Fysiologisch dier: aanpassing en omgeving. Cambridge University Press.

