Serine -kenmerken, functies, metabolisme, voedsel
- 4909
- 1599
- James Dach
De Serine Het is een van de 22 basisaminozuren, hoewel dit niet wordt geclassificeerd als een essentieel aminozuur voor mens en andere dieren, omdat het wordt gesynthetiseerd door het menselijk lichaam.
Volgens de nomenclatuur met drie brieven wordt de serine in de literatuur beschreven als zijnde (s in de enkele lettercode). Dit aminozuur neemt deel aan een groot aantal metabole routes en heeft polaire kenmerken, maar heeft geen belasting op neutrale pH.
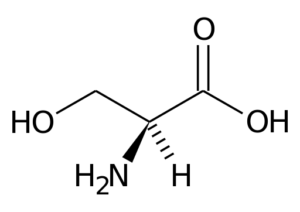 Weergave van de serie van het serinaminozuur (bron: PageZero erop.Wikipedia [Public Domain] via Wikimedia Commons)
Weergave van de serie van het serinaminozuur (bron: PageZero erop.Wikipedia [Public Domain] via Wikimedia Commons) Veel belangrijke enzymen voor cellen hebben genoeg.
De serine, onder veel van zijn functies, neemt deel als een voorloper en steigermolecuul in de biosynthese van andere aminozuren zoals glycine en cysteïne en maakt deel uit van de structuur van de sfingolipiden die aanwezig zijn in celmembranen in celmembranen.
De serine -synthesesnelheid varieert in elk orgaan en verandert bovendien volgens het stadium van ontwikkeling waarin het individu is.
Wetenschappers hebben voorgesteld dat L-serineconcentraties in hersenweefsel toenemen met de leeftijd, omdat de permeabiliteit van de bloedcelbarrière afneemt in de hersenen van de volwassen.
Het is bekend dat L-serine van vitaal belang is voor de biosynthese van neurotransmitters, fosfolipiden en andere complexe macromoleculen, omdat het de voorlopers biedt voor deze meerdere metabole routes.
Verschillende studies hebben aangetoond dat het aanbod van supplementen of concentraten van L-serine aan bepaalde soorten patiënten glucosehomeostase, mitochondriale functie verbeteren en de neuronale dood verminderen.
[TOC]
Kenmerken en structuur
Alle aminozuren hebben als basisstructuur een carboxylgroep en een aminogroep bevestigd aan hetzelfde koolstofatoom; Deze verschillen echter van elkaar door hun zijketens, bekend als R -groepen, die kunnen variëren in hun grootte, structuur en zelfs in hun elektrische lading
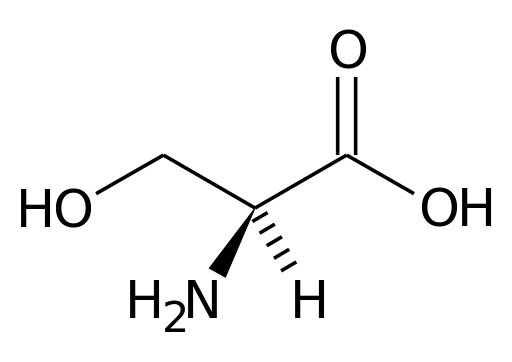
De serine bevat drie koolstofatomen: een verenigde centrale koolstof enerzijds, naar een carboxylgroep (COOH) en anderzijds een aminogroep (NH3+). De andere twee centrale koolstofbindingen worden bezet door een waterstofatoom en een CH2OH (groep R) -groep, kenmerkend voor de serine.
De centrale koolstof waaraan de amino- en carboxylgroepen van de aminozuren bekend staan als de α -koolstof. De andere koolstofatomen van R -groepen worden aangeduid met de letters van het Griekse alfabet.
In het geval van de serine, bijvoorbeeld, staat het enige koolstofatoom in zijn R -groep, die is gekoppeld aan de OH -groep, bekend als koolstof γ.
Kan u van dienst zijn: fosfatidilserine: structuur, synthese, functies, locatieClassificatie
De serine wordt geclassificeerd binnen de groep polaire aminozuren zonder belasting. De leden van deze groep zijn zeer oplosbare aminozuren in water, dat wil zeggen dat het hydrofiele verbindingen zijn. In de serine en het tronine is hydrofiliciteit te wijten aan het vermogen om waterstofbruggen te vormen met water door zijn hydroxylgroepen (OH).
Binnen de groep polaire aminozuren zonder belasting worden cysteïne, asparagine en glutamine ook gegroepeerd. Al deze hebben een polaire groep in hun R -keten, maar deze groep is niet ioniseerbaar en pH dicht bij neutraliteit annuleren hun kosten die een verbinding produceren in de vorm van "Zwitterion".
Stereochemie
De algemene asymmetrie van aminozuren maakt de stereochemie van deze verbindingen van vitaal belang in de metabole routes waaraan ze deelnemen. In het geval van de serine kan dit worden gevonden als d-o l-serine, die de laatste is die uitsluitend wordt gesynthetiseerd door de cellen van het zenuwstelsel dat bekend staat als astrocyten.
De α -koolstofatomen van de aminozuren zijn chirale koolstofatomen, omdat ze vier verschillende verenigde substituenten hebben, wat genereert dat er ten minste twee onderscheidbare stereoisomeren zijn voor elk aminozuur.
Een stereoisomeer is een spiegelafbeelding van een molecuul, dat wil zeggen dat je de ene kunt overlappen aan de andere. De oplossingen van deze aminozuren roteren het gepolariseerde lichtvlak in tegengestelde richtingen in tegengestelde richtingen worden aangeduid met de letter d o die experimenteel.
De L-serine die wordt gesynthetiseerd in cellen van het zenuwstelsel dient als een substraat om glycine of D-serine te synthetiseren. De D-Serin is een van de belangrijkste elementen voor de uitwisseling van blaasjes tussen neuronen, dus sommige auteurs stellen voor dat beide serine-isovormen in werkelijkheid essentiële aminozuren zijn voor neuronen voor neuronen.
Functie
De OH -groep van de serine in zijn R -keten R maakt het een goede nucleofiel, dus het is de sleutel tot de activiteit van veel enzymen met serine op zijn actieve plaatsen. Serine is een van de benodigde substraten voor NADPH en glutathionische nucleotidesynthese.
L-serie is onmisbaar voor de ontwikkeling en de juiste werking van het centrale zenuwstelsel. Studies hebben aangetoond dat de exogene toevoer van L-serine in lage doses naar hippocampus neuronen en Purkinje-cellen In vitro, Verbetert je overleving.
Verschillende studies van kankercellen en lymfocyten hebben aangetoond dat serineafhankelijke koolstofeenheden nodig zijn voor de overmatige productie van nucleotide, evenals de daaropvolgende proliferatie van kankercellen.
Kan u van dienst zijn: microbiota: samenstelling, functies en waar is hetSelenocysteïne maakt deel uit van de 22 basale aminozuren en wordt alleen verkregen als een afgeleide van de serine. Dit aminozuur is alleen in sommige eiwitten waargenomen, bevat selenium in plaats van zwavel bevestigd aan de cysteïne en wordt gesynthetiseerd op basis van een gesterifieerde serine.
Biosynthese
De serine is een niet -essentieel aminozuur, omdat het wordt gesynthetiseerd door het menselijk lichaam. Dit kan echter worden geassimileerd uit het dieet van verschillende bronnen zoals eiwitten en fosfolipiden, vooral.
De serine wordt in zijn vorm gesynthetiseerd door de omzetting van een glycinemolecuul, een reactie gemedieerd door een hydroxymethyltransferase-enzym.
Het is bekend dat de belangrijkste plaats van synthese van L-serine zich in astrocyten bevindt en niet in neuronen. Het zijn deze cellen, synthese treedt op door een fosforylatieroute waarin de 3-fosfoglyceraat deelneemt, een glycolytische tussenpersoon.
Drie enzymen werken op deze route: de 3-fosfoglycerate dehydrogenase, fosfoserine-transferase en fosfoserine-fosfatase.
Andere belangrijke organen met betrekking tot serine -synthese zijn de lever, nieren, testikels en milt. De enzymen die serine synthetiseren.
Een van de eerste syntheseroutes van de bekend serine was de katabole route die betrokken was bij gluconeogenese, waarbij L-serine wordt verkregen als een secundaire metaboliet. De bijdrage van deze route aan de productie van lichaamsserine is echter laag.
Metabolisme
Het is momenteel bekend dat de serine kan worden verkregen uit koolhydraatmetabolisme in de lever, waar D-glycerisch zuur, 3-fosfoglycerisch zuur en 3-fosfohydroxipirúvinezuur wordt geproduceerd. Dankzij een transaminatieproces tussen 3-hydroxi pyruvinezuur en alanine wordt serine geproduceerd.
Experimenten met ratten die radioactief koolstof 4 van glucose markeren, hebben geconcludeerd dat deze koolstof effectief wordt opgenomen in de koolstofskeletten van de serine, wat suggereert dat dit aminozuur een voorloper van drie koolstofatomen heeft, waarschijnlijk van pyruvaat.
In bacteriën is het L-serine-desaminase-enzym het belangrijkste enzym dat de leiding heeft voor het metaboliseren van de serine: het omzet L-serine in een pyruvaat. Het is bekend dat dit enzym aanwezig is en actief is in gewassen van EN. coli Toekennen in minimale media met glucose.
Het is niet zeker weet wat de echte functie is van het L-serine-desaminase in deze micro-organismen, omdat de expressie ervan wordt geïnduceerd door mutatie-effectoren die DNA beschadigen door ultraviolette straling, vanwege de aanwezigheid van nalidíxicico, mythomicine en anderen, mythomicine en mythomicine en anderen, dus volgt dat het belangrijke fysiologische implicaties moet hebben.
Kan u van dienst zijn: Dryopithecus: ontdekking, kenmerken, schedel, voedselSerine Rich Foods
Alle voedingsmiddelen met hoge eiwitconcentraties zijn rijk aan serine, voornamelijk eieren, vlees en vis. Dit is echter een niet -essentieel aminozuur, dus het is niet strikt noodzakelijk om het in te nemen, gezien het feit dat het lichaam het zelf kan synthetiseren.
Sommige mensen lijden aan een ongebruikelijke aandoening, omdat ze een tekortfenotype hebben met betrekking tot de synthesemechanismen van serine en glycine, daarom moeten ze geconcentreerde voedselsupplementen voor beide aminozuren innemen.
Bovendien bieden commerciële merken die gespecialiseerd zijn in de verkoop van vitaminesupplementen (Lamberts, Now Sport en Holomega) fosfatidylserine- en L-serineconcentraten om de productie van spiermassa in hoge competitie-atleten en gewichtheffers te verhogen.
Gerelateerde ziekten
De storing van de enzymen die betrokken zijn bij de biosynthese van de serine kan ernstige pathologieën veroorzaken. Door de serineconcentratie in bloedplasma en cerebrospinale vloeistof te verminderen, kan het hypertonie, psychomotorische vertraging, microcefalie, epilepsie en complexe aandoeningen van het centrale zenuwstelsel veroorzaken.
Momenteel is ontdekt dat serinedeficiëntie betrokken is bij de ontwikkeling van diabetes mellitus, omdat L-serine noodzakelijk is voor de synthese van insuline en die van zijn receptoren.
Baby's die defecten presenteren in serinebiosynthese zijn neurologisch abnormaal bij de geboorte, hebben vertragingen in intra -uteriene groei, aangeboren microcefalie, staar, aanvallen, aanvallen en een ernstige vertraging in neurologische ontwikkeling.
Referenties
- Elsila, J. EN., Dworkin, J. P., Bernstein, m. P., Martin, m. P., & Sandford, s. NAAR. (2007). Mechanismen van aminozuurvorming in interstellair ijsanalogen. The Astrophysical Journal, 660 (1), 911.
- Ichord, r. N., & Bearden, D. R. (2017). Perinatale metabole encefalopathieën. In de pediatrische neurologie van Swaiman (pp. 171-177). Elsevier.
- Mothet, J. P., Ouder, een. T., Wolosker, h., Brady, r. OF., Linden, D. J., Ferris, c. D.,… & Snyder, s. H. (2000). D-serine is een endogeen ligand voor de glycine-plaats van de N-methyl-D-apartediende. Proceedings of the National Academy of Sciences, 97 (9), 4926-4931
- Nelson, D. L., Lehninger, een. L., & Cox, m. M. (2008). Lehninger -principes van biochemie. Macmillan.
- Rodríguez, een. EN., Ducker, g. S., Billingham, l. K., Martinez, C. NAAR., Mainolfi, n., Suri, V.,… & Chandel, n. S. (2019). Serine-metabolisme ondersteunt de productie van macrofaag IL-1β. Celmetabolisme, 29 (4), 1003-1011.
- Tabatabaie, l., Klomp, l. W., Berger, r., & Koning, T. J. (2010). L-serine-synthese in het centrale zenuwstelsel: een overzicht van de aandoeningen van serine-deficiëntie. Moleculaire genetica en metabolisme, 99 (3), 256-262.
- « Glyceraldehydestructuur, kenmerken, functies
- Zinkgeschiedenis, eigenschappen, structuur, risico's, gebruik »

