Renio Discovery, eigenschappen, structuur, gebruik

- 2689
- 222
- Alton D'Amore
Hij Renio Het is een metalen element waarvan het chemisch symbool is RE en zich bevindt in groep 7 van de periodiek systeem, twee posities onder het mangaan. Deel met dit en technecio -eigendom van meerdere nummers of oxidatietoestanden, van +1 tot +7. Vormt ook een anion genaamd perrenato, gevangene4-, Analoog aan permanganaat, mno4-.
Dit metaal is een van de meest zeldzame en schaars van aard, dus de prijs is hoog. Het wordt geëxtraheerd als een bijproduct van molybdeen- en koperen mijnbouw. Een van de meest relevante eigenschappen van Renio is het hoge smeltpunt, nauwelijks overwonnen door koolstof en wolfraam, en de grote dichtheid, het dubbele van die van lood.
 Renio Metal Sphere. Bron: Hi-Res Images ofChemical Elements/CC door (https: // creativeCommons.Org/licenties/door/3.0)
Renio Metal Sphere. Bron: Hi-Res Images ofChemical Elements/CC door (https: // creativeCommons.Org/licenties/door/3.0) Zijn ontdekking heeft controversiële en ongelukkige nuances. De naam van 'Renio' komt voort uit het Latijnse woord 'rhenus', wat Rin betekent, de beroemde Duitse rivier in de buurt van de site waar de Duitse chemici die dit nieuwe element hebben geïsoleerd en geïdentificeerd, werk.
Renio heeft talloze toepassingen, waaronder de verfijning van het octaan van benzine -stands.
[TOC]
Ontdekking
Het bestaan van twee zware elementen met chemische kenmerken die vergelijkbaar zijn met die van het mangaan al voorspelden sinds de 1869, door het periodiek systeem van de Russische chemicus Dmitri Mendeleev. Het was in die tijd echter niet bekend wat hun atoomnummers zouden moeten zijn; En het was hier in 1913 toen de voorspelling van de Engelse natuurkundige Henry Moseley werd geïntroduceerd.
Volgens Moseley moeten deze twee elementen die tot de mangaangroep behoren, atomaire nummers 43 en 75 hebben.
Een paar jaar eerder had de Japanse chemicus Masataka Ogawa echter het vermeende element 43 ontdekt in een steekproef van Mineral Torianita. Nadat hij de resultaten in 1908 had aangekondigd, wilde hij dit element dopen met de naam 'Niponio'. Helaas toonden de chemici op dat moment aan dat Ogawa geen element 43 had ontdekt.
Het kan u van dienst zijn: cycloalques: chemische structuur, eigenschappen, nomenclatuurEn dus verstreken andere jaren toen in 1925 drie Duitse chemici: Walter Noddack, Ida Noddack en Otto Berg, element 75 gevonden in columbita, gadoliniet en molybdeniet minerale monsters. Deze gaven hem de naam Renio, ter ere van de Rin Rin van Duitsland ('Rhenus', in het Latijn).
De fout van Masataka Ogawa was om afgesproken te zijn in de identificatie van het element: hij had Renio ontdekt, niet element 43, vandaag TecNecio genoemd.
Renio -eigenschappen
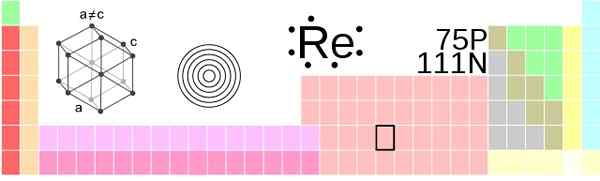 Renio -situatie in het periodiek systeem. !Origineel: ahoteseiervector: sushant savla/cc by-s (https: // creativeCommons.Org/licenties/by-sa/3.0)
Renio -situatie in het periodiek systeem. !Origineel: ahoteseiervector: sushant savla/cc by-s (https: // creativeCommons.Org/licenties/by-sa/3.0) Fysiek uiterlijk
Renio wordt meestal op de markt gebracht in de vorm van grijsachtig stof. De metalen stukken, meestal bolvormige druppels, zijn zilvergrijs, die ook zeer helder zijn.
Molaire massa
186,207 g/mol
Atoomnummer
75
Smeltpunt
3186 ºC
Kookpunt
5630 ºC
Dikte
-Bij kamertemperatuur: 21,02 g/cm3
-Precies op het smeltpunt: 18,9 g/cm3
Renio is een metaal dat bijna twee keer zo dicht is dan dezelfde voorsprong. Aldus kan een Renio -bol die 1 gram weegt, worden gelijkgesteld met een robuust loodkristal van dezelfde massa.
Elektronegativiteit
1.9 Op de Pauling -schaal
Ionisatie -energieën
Eerst: 760 kJ/mol
Ten tweede: 1260 kJ/mol
Derde: 2510 kJ/mol
Molaire warmtecapaciteit
25.48 J/(mol · k)
Warmtegeleiding
48.0 w/(m · k)
Elektrische weerstand
193 nω · m
Mohs hardheid
7
Isotopen
Renio -atomen worden in de natuur gepresenteerd als twee isotopen: 185Re, met een overvloed van 37,4%; En 187Re, met een overvloed van 62,6%. Renio is een van die elementen waarvan de meest voorkomende isotoop radioactief is; De tijd van het halfwaardetijd van echter 187Re is erg groot (4.12 · 1010 jaren), dus het wordt praktisch als stabiel beschouwd.
Kan u van dienst zijn: Nikkel: Geschiedenis, eigenschappen, structuur, gebruik, risico'sReactiviteit
Metallic Renio is een materiaal dat resistent is tegen oxideren. Wanneer hij dat doet, zijn oxide, Re2OF7, Het wordt vervluchtigd bij hoge temperaturen en brandt met een geelachtige groene vlam. Renio's stukken weerstaan de aanval van Hno3 geconcentreerd; Maar heet, lost op om reninezuur en stikstofdioxide te genereren, die de oplossing kleurt:
Re + 7hno3 → hreo4 + 7 Nee2 + 3H2OF
De chemie van Renio is enorm, omdat het in staat is om verbindingen te vormen met een breed spectrum van oxidatienummers, en een quadrupolo-binding tussen twee Renio-atomen tot stand brengt (vier re-covalente bindingen).
Elektronische structuur en configuratie
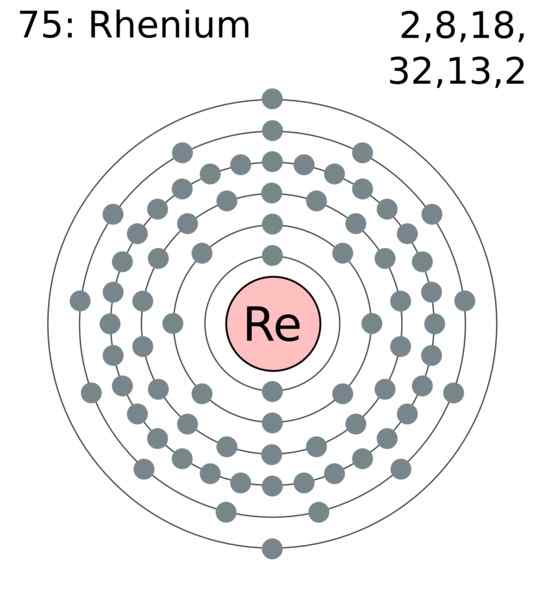 Renio Electron Layer. Auteur: Gebruiker: Gregrobson (Greg Robson). Wikimedia Commons
Renio Electron Layer. Auteur: Gebruiker: Gregrobson (Greg Robson). Wikimedia Commons Renio -atomen zijn gegroepeerd in hun kristallen om een compacte hexagonale structuur te veroorzaken, HCP, die wordt gekenmerkt door erg dicht. Dit komt overeen met het feit dat het een metaal van grote dichtheid is. De metalen link, product van de overlapping van zijn externe orbitalen, houdt de atomen sterk samenhangend.
In deze metalen link, ReRE, nemen de elektronen van Valencia deel, die volgens de elektronische configuratie zijn:
[XE] 4F14 5 D5 6s2
In principe zijn het 5D- en 6s -orbitalen die elkaar overlappen om de RE -atomen in de HCP -structuur te compacteren. Merk op dat uw elektronen in totaal 7 toevoegen, overeenkomend met het nummer van uw groep in het periodieke tabel.
Oxidatienummers
De Renio Electronic Configuration eenmaal een glimp van een glimp van zijn atoom in staat is om maximaal 7 elektronen te verliezen, om de hypothetische kation te worden7+. Wanneer het bestaan van de RE wordt aangenomen7+ In elke Renio -verbinding bijvoorbeeld in de RE2OF7 (Met betrekking tot27+OF72-), Er wordt gezegd dat het een oxidatienummer van +7, Re (vii) heeft.
Andere positieve oxidatienummers voor Renio zijn: +1 (Re+), +2 (Re2+), +3 (Re3+), Enzovoort tot +7. Evenzo kan Renio opwekken dat elektronen een anion worden. In deze gevallen wordt gezegd dat het een negatief oxidatienummer heeft: -3 (Re3-), -2 (Re2-) en -1 (Re-)).
Het kan u van dienst zijn: Hydrolyse: wat is het en voorbeelden van reactiesToepassingen
Benzine
Renio wordt samen met platina gebruikt om katalysatoren te creëren die de mate van octaan van benzine vergroten, terwijl het loodgehalte wordt verminderd. Aan de andere kant zijn renio -katalysatoren bestemd voor meerdere hydrogeneringsreacties, dit vanwege hun weerstand tegen vergiftiging van stikstof, fosfor en zwavel.
Refractaire superlaties
Renio is een vuurvast metaalproduct van zijn hoge smeltpunt. Dat is de reden waarom nikkellegeringen worden toegevoegd om ze ongevoelig te maken en bestand tegen grote drukken en temperaturen. Deze superlaties worden meestal gebruikt voor het ontwerp van turbines en motoren voor ruimtevaartschepen.
Wolfraamfilamenten
Renio kan ook legeringen vormen met wolfraam, die zijn ductiliteit verbetert en daarom de vervaardiging van filamenten vergemakkelijkt. Deze Renio-Tungsten-filamenten worden gebruikt als röntgenbronnen, en voor het ontwerp van thermocuplaes die in staat zijn temperaturen tot 2200 ° C te meten.
Evenzo werden deze Renio -filamenten ooit gebruikt voor archaïsche camera's flitsen, en momenteel voor geavanceerde apparatuurlampen; zoals massaspectrofotometer.
Referenties
- Shiver & Atkins. (2008). Anorganische scheikunde. (Vierde druk). MC Graw Hill.
- Sarah Pierce. (2020). Rhenium: gebruik, geschiedenis, feiten en isotopen. Studie. Hersteld van: studie.com
- Nationaal centrum voor biotechnologie -informatie. (2020). Rhenium. PubChem -database., CID = 23947. Hersteld van: pubchem.NCBI.NLM.NIH.Gov
- Wikipedia. (2020). Rhenium. Opgehaald uit: in.Wikipedia.borg
- Dr. Doug Stewart. (2020). Rhenium -elementen Feiten. Hersteld van: chemicool.com
- Eric Scerri. (18 november 2008). Rhenium. Chemie in zijn elementen. Hersteld van: chemieworld.com
- « Geen karakteristieke elektrolyten en voorbeelden
- Alfa-cootogl De eigenschappen, functies en toepassingen »

