Neerslag

- 4103
- 264
- Ernesto McKenzie
We leggen uit wat een neerslag is, de neerslagreactie, de typen die bestaan en geven verschillende voorbeelden
 Gele neerslagvorming bij het mengen van een oplossing met een neerslagmiddel
Gele neerslagvorming bij het mengen van een oplossing met een neerslagmiddel Wat is een neerslag?
A neerslag Het is een vaste stof die wordt gevormd uit een oplossing, hetzij door de kristallisatie van een opgeloste stof of door de vorming van een onoplosbare stof door een chemische reactie.
Het eerste geval treedt op wanneer een vaste stof, die aanvankelijk werd opgelost in een oplosmiddel zoals water, minder oplosbaar wordt. Dit kan gebeuren wanneer:
- De temperatuur van de oplossing is verlaagd.
- Er wordt een neerslagmiddel toegevoegd.
- Een ander oplosmiddel wordt toegevoegd waarin de vaste stof minder oplosbaar is.
Wanneer de oplosbaarheid ervan kleiner wordt dan zijn concentratie, raakt de oplossing oververzadigd en treedt een neerslagreactie op.
Het tweede geval treedt op na een chemische reactie die een onoplosbaar of zeer weinig oplosbaar product in het oplosmiddel genereert. Zodra dit product zich begint te vormen, is de oplossing snel verzadigd en begint de vaste stof neer te slaan.
Chemische neerslagreactie
De neerslagreactie is het chemische proces dat leidt tot de vorming van een neerslag. Afhankelijk van hoe het neerslag wordt gevormd, kan de reactie op twee verschillende manieren worden geschreven:
- Als de neerslag optreedt omdat de oplosbaarheid van de vaste stof in het oplosmiddel werd verminderd (bijvoorbeeld koelen of een ander oplosmiddel toevoegen), dan omvat de neerslagreactie alleen de opgeloste stof en zou er zo uitzien:

Bijvoorbeeld, Als natriumacetaat oplost (CH-3Zak) In heet water en vervolgens toegestaan om te koelen, zal natriumacetaat neerslaan volgens de volgende vergelijking:

- Als de neerslag optreedt omdat een neerslagmiddel is toegevoegd, zal de neerslagreactie zowel de opgeloste stof als het neerslagmiddel inhouden.
Bijvoorbeeld, Zilverionen (Ag+) Ze kunnen neerslaan uit een zilvernitraatoplossing (agno3) Een oplossing van natriumchloride of NaCl (neerslagmiddel) toevoegen. De neerslagreactie wordt in dit geval gegeven door:
Het kan u van dienst zijn: nikkelchloride (NICL2): structuur, eigenschappen, verkrijgen, gebruik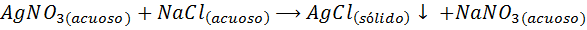
Neerslagmechanisme
Ongeacht de neerslagreactie komt de vorming van het neerslag altijd voor in twee stadia die nucleatie en groei worden genoemd:
-
Nucleatie
Aan het begin van de neerslagreactie worden kleine neerslagdeeltjes gevormd die kernen worden genoemd, dus dit stadium wordt nucleatie genoemd.
-
Groei
Na nucleatie worden nieuwe deeltjes niet langer gevormd, maar de al gevormde kernen beginnen te groeien totdat de neerslag stopt.
Soorten neerslag
De snelheid waarmee de neerslag wordt gevormd, beïnvloedt de grootte van de vaste deeltjes en de eigenschappen van dezelfde. Afhankelijk van de grootte van de deeltjes en de aard van de verbinding die neerslaat, kunnen drie soorten neerslag worden onderscheiden:
Kristallijne neerslag
Het is het eenvoudigste type neerslag. In dit geval bestaat het neerslag uit grote vaste deeltjes met een diameter groter dan 0,1 micrometer.
 Kristallijn neerslag van kopersulfaat (II) pentahydraat
Kristallijn neerslag van kopersulfaat (II) pentahydraat Kristallijne neerslag wordt gevormd wanneer de neerslagreactie langzaam optreedt. Hierdoor kunnen er weinig vaste deeltjes zich vormen tijdens nucleatie, en elk van deze deeltjes heeft voldoende tijd om te groeien en grote en zware kristallen te vormen die op de bodem van de oplossing vallen.
Deze deeltjes zijn bijna altijd kristallijne vaste stoffen met platte en heldere gezichten, vergelijkbaar met de facetten van een diamant, en kunnen bijna altijd worden onderscheiden met het blote oog.
Casusous neerslachten
Ze worden neergeslagen voor veel kleinere deeltjes, tussen 0,01 en 0,1 micrometer in diameter. Dit type neerslag wordt gevormd wanneer de neerslagreactie zeer snel optreedt, waardoor veel deeltjes worden gegenereerd tijdens nucleatie die geen tijd hebben om te groeien.
Vanwege hun grootte zijn deze deeltjes zeer licht en worden ze gesuspendeerd in de oplossing die een stabiele colloïde vormt. Om deze reden vestigen ze zich niet onderaan de oplossing en ziet het er bewolkt uit in plaats van transparant.
Kan u van dienst zijn: dihydroxyaceton: structuur, eigenschappen, verkrijgen, gebruik Drie caseosos van verschillende kleuren. De drie oplossingen zijn troebel na de vorming van de neerslag
Drie caseosos van verschillende kleuren. De drie oplossingen zijn troebel na de vorming van de neerslag Daarnaast zijn de deeltjes zo klein dat ze erin slagen om de meeste filters over te steken die worden gebruikt om de neerslag van de oplossingen te scheiden.
Jellyry Hacords
Wanneer de deeltjes nog kleiner zijn dan die van de caseous neerslag, dat wil zeggen met diameters van minder dan 0,01 micrometer, worden de neerslagen gelei genoemd. De reden is omdat de vaste stof een uiterlijk verwerft vergelijkbaar met de gelatine of een jam.
Deze neerslag wordt ook beschouwd als colloïden. In feite is de gelatine een typisch voorbeeld van een colloïde, en deze neerslagen halen hun naam uit hetzelfde.
Karakteristieke voorbeelden van steile jelly steile zijn de gehydrateerde oxiden van sommige metalen. Deze oxiden absorberen een grote hoeveelheid water op hun oppervlak waardoor het grotere deeltjes vormt die kristalliseren.
Voorbeelden
Natriumacetaat (ch3Zak)
Zoals hierboven vermeld, kan natriumacetaat worden neergeslagen uit een hete verzadigde oplossing die kan afkoelen. Als het langzaam kan afkoelen, wordt een kristallijn neerslag gevormd waarin lange witte naaldkristallen worden waargenomen.
Cadmium sulfide (II) (cd's)
Cadmiumsulfide is een zeer onoplosbaar zout dat onmiddellijk wordt gemengd in een cadmiumion (II) -oplossing met een andere die sulfide -ionen bevat.
Kopersulfaat (ii) pentahydraat (cuo4.5h2OF)
Bij het oplossen van het in water vormt kopersulfaat (II) gehydrateerde ionen van intens blauw. Als het water langzaam verdampt, neerslaat dan prachtige blauwe kristallen van Cuso4.5h2OF. Deze kristallen lijken edelstenen.
Silver Bromide (AGBR)
Dit is een voorbeeld van een verbinding die zeer snel neerslaat en een neerslag vormt met zeer dunne deeltjes die moeilijk te filteren zijn.
Kan u van dienst zijn: equivalent gewichtAluminium gehydrateerd oxide (III) (tot2OF3.NH2OF)
Dit is een klassiek voorbeeld van de vorming van een gelatineus neerslag. Het wordt gevormd wanneer een aluminium nitraatoplossing (nee (nee3))3)).
Mangaansulfide (II) (MNS)
Veel sulfiden zijn onoplosbaar in water en mangaansulfide is geen uitzondering. Dit neerslaat in de vorm van een zeer fijn stof.
Silver Chloride (AGCL)
Zilverionen (i) vormen zeer weinig oplosbare zouten met alle halogenen. Het geval van zilveren chloride is een klassiek voorbeeld van neergeslagen vorming in het laboratorium.
Calciumcarbonaat (caco3))
Calcium is een van de ionen die verantwoordelijk zijn voor de hardheid van water. Wanneer water dat calcium bevat, wordt verwarmd, reageert het en het vormen van calciumcarbonaat dat neerslaat in de vorm van een witte laag genaamd wijnsteen, die zelfs de leidingen kan belemmeren.
IJzer gehydrateerd oxide (III) (geloof2OF3.NH2OF)
Dit is een ander voorbeeld van een gelatineus neerslag dat wordt gevormd door de reactie van een oplossing die ijzerionen (III) bevat met natrium- of kaliumhydroxide.
Magnesiumhydroxide (Mg (OH)2))
Magnesium is het andere kation dat verantwoordelijk is voor waterhardheid, omdat het kan neerslaan in de vorm van magnesiumhydroxide in leidingen en andere waterverwarmingssystemen.
Referenties
- Bancoft, W. D. (1918). Overzicht van colloïde chemie.-III. Journal of the Franklin Institute, 185(3), 373-387. https: // doi.org/10.1016/S0016-0032 (18) 90710-6
- Civan, f. (2007). Kristalgroei en schaalvorming in poreuze media. Reservoirvormingsschade, 235-255. https: // doi.org/10.1016/B978-075067738-7/50010-5
- Skoog, D. NAAR., West, D. M., Holler, f. J., & Crouch, s. R. (2013). Fundamentals of Analytical Chemistry. New York City, New York: Cengage Learning.
- Wikipedia -bijdragers. (2021, 10 januari). Neerslag (chemie). Opgehaald van.Wikipedia.borg

