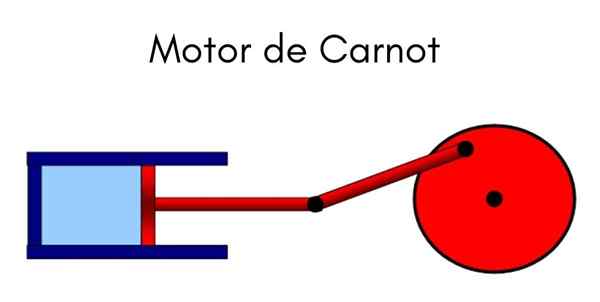
Carnot Machine
- 3486
- 1126
- Cecil Graham
Wat is de Carnot -machine?
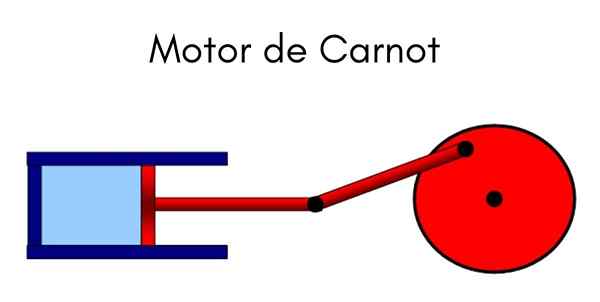
De Carnot Machine Het is een ideaal cyclisch model waarin warmte wordt gebruikt om een werk te doen. Het systeem kan worden opgevat als een zuiger die in een cilinder beweegt die een gas comprimeert. De uitgeoefende cyclus is die van Carnot, vermeld door de vader van de thermodynamica, de Franse natuurkundige en ingenieur Nicolas Leonard Sadi Carnot.
Carnot verklaarde deze cyclus in de vroege negentiende eeuw. De machine wordt onderworpen aan vier toestandsvariaties, afwisselende omstandigheden zoals constante temperatuur en druk, waarbij een variatie van het volume wordt aangetoond bij het comprimeren en uitbreiden van gas.
Formules
Volgens Carnot is het mogelijk om de ideale machine te onderwerpen aan temperatuur- en drukvariaties, het mogelijk om de verkregen prestaties te maximaliseren.
De carnotcyclus moet in elk van de vier fasen afzonderlijk worden geanalyseerd: isotherm expansie, adiabatische expansie, isotherme compressie en adiabatische compressie.
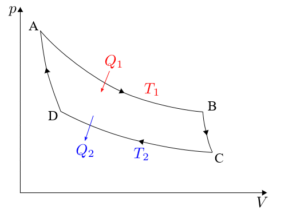
De formules die zijn geassocieerd met elk van de fasen van de cyclus die op de Carnot -machine wordt uitgeoefend, worden hieronder gedetailleerd beschreven.
Isotherme expansie (A → B)
De gebouwen van deze fase zijn de volgende:
- Gasvolume: Het gaat van het minimale volume naar een gemiddeld volume.
- Machinetemperatuur: constante temperatuur T1, hoge waarde (t1> t2).
- Machinedruk: Daal af van P1 naar P2.
Het isothermische proces houdt in dat temperatuur T1 niet varieert tijdens deze fase. Warmteoverdracht induceert gasuitbreiding, die beweging op de zuiger induceert en mechanisch werk produceert.
Bij het uitbreiden vormt het gas een bepaalde neiging om te koelen. Het absorbeert echter de warmte die wordt uitgezonden door de temperatuurbron en tijdens zijn expansie handhaaft het de constante temperatuur.
Kan u van dienst zijn: wat is de lineaire snelheid? (Met opgeloste oefeningen)Omdat de temperatuur tijdens dit proces constant blijft, verandert de interne energie van het gas niet en wordt alle warmte die door het gas wordt geabsorbeerd effectief omgezet in werk. Dus:
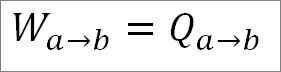
Aan de andere kant is het aan het einde van deze fase van de cyclus ook mogelijk om de drukwaarde te verkrijgen met behulp van de ideale gasvergelijking ervoor. Op deze manier heb je het volgende:
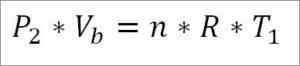
In deze uitdrukking:
- P2: Druk aan het einde van de fase.
- VB: Volume op punt B.
- N: aantal mol gas.
- A: Universele constante van ideale gassen. R = 0,082 (atm*liter)/(mol*k).
- T1: absolute begintemperatuur, Kelvin -graden.
Adiabatische expansie (B → C)
Tijdens deze fase van het proces wordt gasuitbreiding uitgevoerd zonder de noodzaak om warmte uit te wisselen. Op deze manier worden het pand hieronder gedetailleerd gedetailleerd:
- Gasvolume: Het gaat van het gemiddelde volume naar een maximaal volume.
- Machinetemperatuur: Daal af van T1 naar T2.
- Machinedruk: constante P2 -druk.
Het adiabatische proces houdt in dat de P2 -druk niet varieert tijdens deze fase. De temperatuur daalt en het gas blijft uitzetten totdat het het maximum van zijn volume bereikt; dat wil zeggen, de zuiger bereikt de top.
In dit geval komt het gedaan werk van de interne energie van het gas en is de waarde ervan negatief omdat de energie tijdens dit proces afneemt.
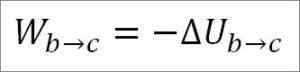
Ervan uitgaande dat het een ideaal gas is, wordt de theorie gehandhaafd dat gasmoleculen alleen kinetische energie hebben. Volgens de principes van de thermodynamica kan dit worden afgeleid door de volgende formule:
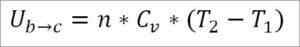
In deze formule:
- ∆UB → C: Interne energievariatie van het ideale gas tussen punten B en C.
- N: aantal mol gas.
- CV: Gasmolaire warmtecapaciteit.
- T1: absolute begintemperatuur, Kelvin -graden.
- T2: Absolute eindtemperatuur, Kelvin -graden.
Isotermische compressie (C → D)
In deze fase begint de compressie van gas; dat wil zeggen, de zuiger wordt gemobiliseerd in de cilinder, waarmee het gas zijn volume contracteert.
De voorwaarden die inherent zijn aan dit proces zijn hieronder gedetailleerd:
- Gasvolume: Het gaat van het maximale volume naar een tussenliggende volume.
- Machinetemperatuur: constante temperatuur T2, verminderde waarde (T2 < T1).
- Machinedruk: Verhoging van P2 tot P1.
Hier neemt de druk op het gas toe, dus het begint te comprimeren. De temperatuur blijft echter constant en daarom is de interne energievariatie van het gas nul.
Analoog aan de isotherme expansie, het werk is gelijk aan de hitte van het systeem. Dus:
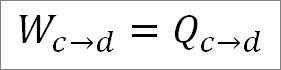
Het is ook mogelijk om de druk op dit punt te vinden met behulp van de ideale gasvergelijking.
Adiabatische compressie (D → A)
Dit is de laatste fase van het proces, waarbij het systeem terugkeert naar zijn beginvoorwaarden. Om dit te doen, worden de volgende voorwaarden beschouwd:
- Gasvolume: Het gaat van een tussenliggend volume naar een minimumvolume.
- Machinetemperatuur: Verhoging van T2 tot T1.
- Machinedruk: constante druk p1.
De warmtebron opgenomen in het systeem in de vorige fase wordt verwijderd, zodat het ideale gas zijn temperatuur ondertussen zal verhogen, blijft de druk constant.
Het gas keert terug naar de initiële temperatuuromstandigheden (T1) en bij het volume (minimum). Nogmaals, het gedaan werk komt van de interne energie van het gas, dus je moet:
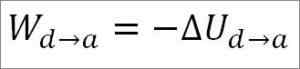
Vergelijkbaar met het geval van adiabatische expansie, is het haalbaar om de variatie van gasergie te verkrijgen door de volgende wiskundige expressie:
Kan u bedienen: calciumfluoride (CAF2): structuur, eigenschappen, gebruik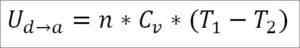
Hoe werkt de Carnot -machine?
De Carnot -machine werkt als een motor waarin prestaties worden gemaximaliseerd door variatie van isothermische en adiabatische processen, waarbij de fasen van expansie en begrip van een ideaal gas worden afwisselend een ideaal gas.
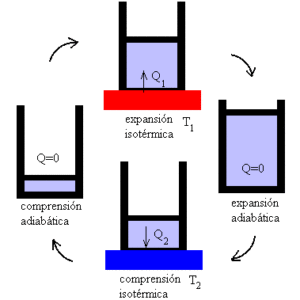
Het mechanisme kan worden opgevat als een ideaal apparaat dat een taak uitoefent die wordt onderworpen aan warmtevariaties, gezien het bestaan van twee temperatuurspotlights.
In de eerste focus wordt het systeem blootgesteld aan een T1 -temperatuur. Het is een hoge temperatuur die het systeem onderwerpt om te benadrukken en gasuitbreiding produceert.
Op zijn beurt vertaalt dit zich in de uitvoering van een mechanisch werk dat de mobilisatie van de zuiger uit de cilinder mogelijk maakt, en waarvan de limiet alleen mogelijk is door adiabatische expansie.
Dan komt de tweede focus, waarin het systeem wordt blootgesteld aan een T2 -temperatuur, minder dan T1; dat wil zeggen, het mechanisme is onderhevig aan koeling.
Dit induceert warmte -extractie en gasverzekering, dat zijn initiële volume bereikt na adiabatische compressie.
Toepassingen
De Carnot -machine is veel gebruikt dankzij de bijdrage in het begrip van de belangrijkste aspecten van de thermodynamica.
Met dit model kunt u de variaties van ideale gassen die onderhevig zijn aan temperatuur- en drukveranderingen duidelijk begrijpen, wat een referentiemethode is bij het ontwerpen van echte motoren.