Glyceraldehyde 3-fosfaat (G3P) structuur, functies
- 1801
- 136
- Dr. Rickey Hudson
Hij glyceraldehyde 3-fosfaat (kloof) Het is een metaboliet van glycolyse (de naam komt van het Griek )).
In cellen verbindt glyceraldehyde 3-fosfaat glycolyse met gluconeogenese en het pentosefosfaatpad. In fotosynthetische organismen wordt glyceraldehyde 3-fosfaat, van koolstofdioxidefixering, gebruikt voor suikerbiosynthese. In de lever produceert fructose -metabolisme Gap, die is opgenomen in glycolyse.
 Bron: Benjah-bmm27 [Public Domain]
Bron: Benjah-bmm27 [Public Domain] [TOC]
Structuur
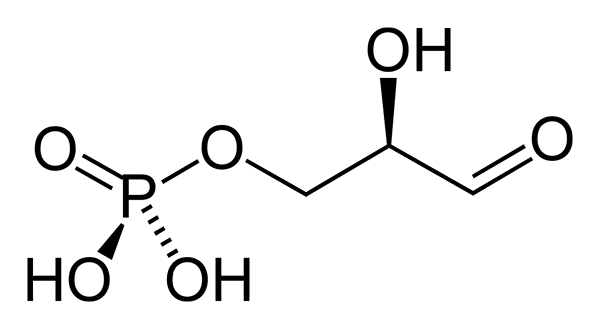
Het 3-fosfaatglyceraldehyde is een gefosforyleerde suiker met drie koolstofatomen. Zijn empirische formule is c3H7OF6P. De aldehyde-groep (-cho) is koolstof 1 (C-1), de hydroxymethyleengroep (-chah) is koolstof 2 (C-2) en de hydroxymetylgroep (-CH2Oh) is koolstof 3 (c3). Deze laatste vormt een link met de fosfaatgroep (Fosfoester Link).
De 3-fosfaat glyceraldehyde configuratie in de C-2 quiral is d. Volgens het Verdrag, met betrekking tot de quirale koolstof, wordt de aldehyde groep in de projectie van Fischer naar boven weergegeven, de hydroxymethyl-fosfaatgroep naar beneden, de hydroxylgroep rechts en het waterstofatoom links.
Kenmerken
Het 3-fosfaatglyceraldehyde heeft een moleculaire massa 170,06 g/mol. Standaard Gibbs vrije energieverandering (ΔGº) voor elke reactie moet worden berekend door de variatie van de vrije energie van de producten toe te voegen en de som van de variatie van de vrije energie van de reactanten af te trekken.
Het kan u van dienst zijn: Metazoa: kenmerken, typen, habitat en ziektenOp deze manier wordt vrije energievariatie (ΔGº) bepaald van glyceraldehyde 3 -fosfaat, dat is -1,285 kJ x mol is-1. Volgens het Verdrag is de vrije energie van de zuivere elementen in de standaardstatus 25 ºC en 1 atm, nul.
Functie
Glycolyse en gluconeogenese
Glycolyse is aanwezig in alle cellen. Het is verdeeld in twee fasen: 1) Energie-investeringsfase en metabolietensynthese met hoog fosfaatgroepoverdrachtspotentieel, zoals glyceraldehyde 3-fosfaat (GAP); 2) ATP -synthese -stadium van moleculen met een hoog overdrachtspotentieel voor fosfaatgroep.
Het 3-fosfaat glyceraldehyde en dihydroxyacetonfosfaat. Het 3-fosfaatglyceraldehyde wordt omgezet in 1,3-bifosfoglyceraat (1,3 bpg), door middel van een reactie gekatalyseerd door de enzym gap dehydrogenase.
De dehydrogenase -kloof katalyseert de oxidatie van het aldehyde koolstofatoom en draagt een fosfaatgroep over. Aldus wordt een gemengd anhydride (1,3 bpg) gevormd waarin de zure groep en het fosforatoom vatbaar zijn voor de nucleofiele aanvalsreactie.
Vervolgens, in een reactie gekatalyseerd door het 3-fosfoglyceraatkinase, brengt de 1,3 bpg de fosfaatgroep over van koolstof 1 naar ADP, waardoor ATP wordt gevormd.
Omdat de reacties gekatalyseerd door de aldolase, zijn de dehydrogenase-opening en het 3-fosfoglyceraatkinase in het evenwicht (ΔGº ~ 0), omkeerbaar en zijn daarom onderdeel van het pad van gluconeogenese (of van de nieuwe synthese van glucose).
Vía de la Pentosa fosfaat en Calvin -cyclus
In de pentose-fosfaatweg worden de 3-fosfaat (GAP) glyceraldehyde en de 6-fosfaatfructose (F6P) gevormd door snij- en vormingsreacties van C-C-bindingen, van het pentose, xylulose 5-fosfaat en ribose 5-fosfaat.
Kan u dienen: Hyracotherium: kenmerken, voeding, soort, reproductie3-fosfaatglyceraldehyde kan het pad van gluconeogenese volgen en 6-fosfaatglucose vormen, die het pad van het pentosefosfaat voortzetten. Glucose kan volledig worden geoxideerd door zes co -moleculen te produceren2 Door het oxidatieve stadium van de pontosa fosfaatweg.
In de Calvin -cyclus, de CO2 Het wordt vastgesteld als 3-fosfoglyceraat, in een reactie gekatalyseerd door het ribulous bifosfaatcarboxylase. Vervolgens wordt 3-fosfoglyceraat door NADH verminderd door werking van een enzym genaamd Gap dehydrogenase.
2 Gap -moleculen voor biosynthese van een hexose, zoals glucose, die dient voor zetmeel- of cellulosebiosynthese in planten in planten zijn nodig.
Fructose metabolisme
Fructochinase-enzym katalyseert de fosforylering van fructose door de ATP in C-1, waardoor 1-fosfaatfructose wordt gevormd. Aldolase A, die in de spier wordt gevonden, is specifiek voor fructose 1,6-bifosfaat als een substraat. Aldolase B wordt gevonden in de lever en is specifiek voor 1-fosfaatfructose als een substraat.
De B-aldolase katalyseert de aldolische breuk van fructose 1-fosfaat en produceert dihydroxyacetonfosfaat en glyceraldehyde. Het glyceraldehyde-kinase katalyseert de fosforylering van glyceraldehyde door ATP, waardoor een glycolytische tussenpersoon wordt gevormd, de 3-fosfaat glyceraldehyde (GAP).
In een andere route wordt glyceraldehyde omgezet in glycerol door een alcoholdehydrogenase die NADH gebruikt als een elektronendonorsubstraat. Vervolgens fosforyleren glycerol kinaseglycerol door ATP, waardoor glycerolfosfaat wordt gevormd. Deze laatste metaboliet is reoxy, die dihydroxyacetonfosfaat (DHAP) en NADH vormt.
De DHAP wordt omgezet in GAP door het drie isomease -fosfaat -enzym. Op deze manier wordt fructose omgezet in glycolysemetabolieten. Fructose die intraveneus wordt geleverd, kan echter ernstige schade veroorzaken, die bestaan uit de drastische afname van intracellulair fosfaat en ATP. Er treedt zelfs melkzuiger aan.
Het kan je van dienst zijn: Chihuahua Flora en Fauna: uitstekende soortenFructose -schade is te wijten aan het feit dat het niet de reguleringspunten heeft die glucosekatabolisme normaal gesproken heeft. Ten eerste komt fructose de spieren binnen via GLUT5, die onafhankelijk is van insuline.
Ten tweede wordt fructose direct omgezet in Gap en op deze manier doorloopt het niet de regulatie van het fosfofuto -kinase (PFK) enzym aan het begin van de glycolyse.
Via Entner-Doudoroff
Glycolyse is de universele route voor glucosekatabolisme. Sommige bacteriën gebruiken echter afwisselend de Entner-Doudoroff-weg. Deze route impliceert zes stappen die worden gekatalyseerd door enzymen, waarin glucose wordt omgezet in Gap en Pyruvato, die twee eindproducten van deze weg zijn.
Gap en pyruvaat worden omgezet in ethanol door alcoholische fermentatiereacties.
Referenties
- Berg, J. M., Tymoczco, J. L., Stryer, l. 2015. Biochemie. Tot korte koers. W. H. Freeman, New York.
- Miesfeld, r. L., McEvoy, m. M. 2017. Biochemie. W. W. Norton, New York.
- Nelson, D. L., Cox, m. M. 2017. Lehninger -principes van biochemie. W. H. Freeman, New York.
- Saway J. G. 2004. Metabolisme in één oogopslag. Blackwell, Malden.
- VOET, D., VOET, J. G., Pratt, c. W. 2008. Fundamentals of Biochemistry: Life op moleculair niveau. Wiley, Hoboken.

