Structurele formule (met voorbeelden)
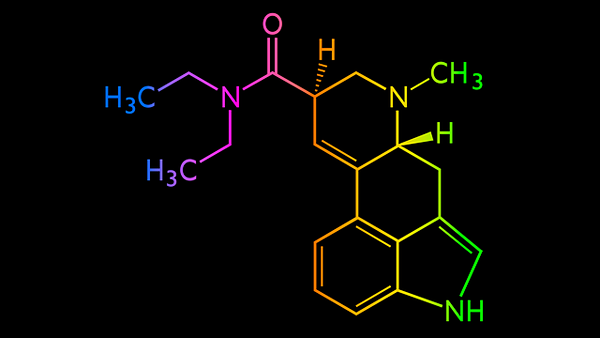
- 2841
- 912
- Kurt Aufderhar Jr.
De Structurele Formule Het is een grafische weergave van een molecuulverbindingen, waardoor licht op zijn structuur wordt werpt, eenmaal bepaald door spectroscopische methoden. Het is de meest concrete manier bij het verwijzen naar een specifieke verbinding, en niet verschillende isomeren die overeenkomen met dezelfde moleculaire formule.
Bijvoorbeeld Butane, c4H10, Het heeft twee isomeren: N-Butano (lineair) en 2-methyl-propaan (vertakt). De moleculaire formule discrimineert ook niet tussen; Terwijl als we ons tot structurele formules wenden, zal het precies worden gezien dat de ene lineair is en de andere vertakt.
 Structurele formules maken het mogelijk om de moleculaire structuren van de verbindingen te onderzoeken. Bron: Pixabay.
Structurele formules maken het mogelijk om de moleculaire structuren van de verbindingen te onderzoeken. Bron: Pixabay. Gebruik structurele formules vergemakkelijkt het begrip van de veranderingen die door een molecuul worden geleden tijdens een chemische reactie; Welke van hun links zijn verbroken, hoe de structuur ervan wordt gewijzigd in het proces en aan het einde ervan. Leren om deze formules te lezen is gelijk aan oppervlakkig voorspellende de eigenschappen van moleculen.
Structurele formules zijn 2D -representaties, hoewel ongeveer drie -dimensionale en geometrische aspecten daarin kunnen worden aangegeven. Hoe meer de structuur van een verbinding, hoe verfijnder en trouwer het uiteindelijk zijn structurele formule wordt. Laat anders essentiële aspecten opzij om de aard van de molecuul te begrijpen.
[TOC]
Voorbeelden van structurele formule
Elke verbinding heeft zijn respectieve structurele formule, die kan variëren, afhankelijk van het type projectie of perspectief dat wordt gebruikt. Gecondenseerde en skeletformules, Lewis -structuren en stereochemische projecties zijn bijvoorbeeld allemaal structurele formules, gewijd aan het in kaart brengen van de maximaal mogelijke informatie over de moleculaire structuur.
Er zijn er zoveel dat enkele eenvoudige voorbeelden zullen worden aangepakt.
Glucose
 Verschillende representaties van de structuur van de alfa-glucose. Bron: Yikrazuul via Wikipedia.
Verschillende representaties van de structuur van de alfa-glucose. Bron: Yikrazuul via Wikipedia. In het bovenste beeld worden vier representaties van het glucosemolecuul getoond. Elk is een geldige structurele formule; Maar de 2 (Haworth -projectie) en de 3 (voorzitterprojectie) zijn meestal het meest gebruikt in academische teksten en publicaties.
Het kan u van dienst zijn: wat zijn de negatieve effecten die we hebben met oplosbaarheid in water?De 4 heeft het voordeel dat het direct wordt aangegeven welke OH -groepen boven (dikke wiggen) of lager zijn (gestippelde wiggen) van de zeshoekige ring; dat wil zeggen, het vergemakkelijkt het begrip van zijn stereochemie. Aan de andere kant toont de 1 (Tollens-Fisher-projectie) het lineaire karakter van glucose voordat hij zijn cyclische vorm wordt.
Methaan
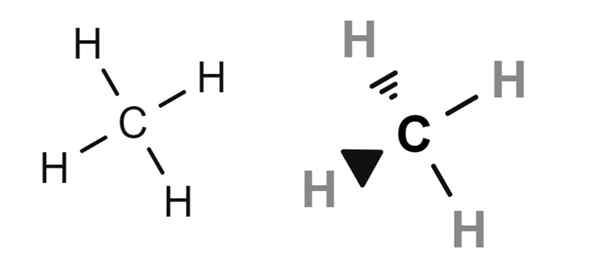 Structurele formule van methaan. Bron: Gabriel Bolívar via Molview.
Structurele formule van methaan. Bron: Gabriel Bolívar via Molview. Hierboven zijn er twee structurele formules van methaan, waarvan de moleculaire en condensaatformule cho is4. Voor degenen die geen chemie -kennis missen, kunnen ze de CHO -formule interpreteren4 Alsof het een molecuul is met een waterstofatoom in het midden.
Maar in werkelijkheid (en noodzakelijkerwijs) verduidelijken structurele formules dat koolstof het centrale atoom is. Daarom hebben we vier C-H-links. Merk op dat de formule links de valse indruk genereert dat het molecuul plat is, terwijl het in werkelijkheid tetraëdrisch is (rechter formule).
Dat is de reden waarom in de structurele formule van het recht de bindingen worden weergegeven door wiggen, wat de relatieve ruimtelijke posities van elk waterstofatoom (hoekpunten van de tetrahedron) aangeeft.
Methanol
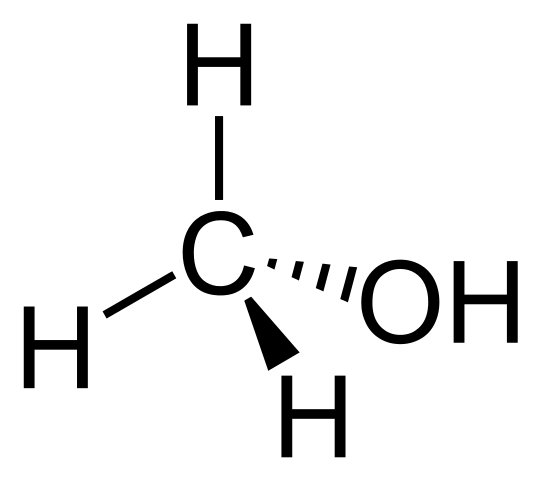 Structurele formule van methanol. Bron: Neurotoger [Public Domain]
Structurele formule van methanol. Bron: Neurotoger [Public Domain] De structurele formule van methanol is praktisch hetzelfde als die van methaan, met het verschil dat het een H presenteert die wordt vervangen door een OH. De formule van gecondenseerde of chemie is cho3Oh, en de moleculaire cho4OF. Opgemerkt wordt dat het ook bestaat uit een tetraëder.
Ethanol
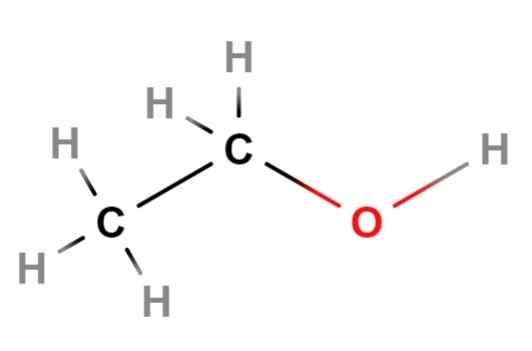 Ethanol structurele formule. Bron: Gabriel Bolívar via Molview.
Ethanol structurele formule. Bron: Gabriel Bolívar via Molview. Nu gaan we verder met ethanol, de volgende alcohol op de lijst. De chemische of gecondenseerde formule is cho3Ch2Oh, dat alleen al zijn lineaire structuur toont. Om uit twijfel te komen, toont de structurele formule van het superieure beeld effectief aan dat ethanol een lineaire ketting of skelet is.
Het kan u van dienst zijn: metoxietano: structuur, eigenschappen, verkrijgen, gebruik, risico'sIndien zorgvuldig waargenomen, zijn de omgevingen van elk koolstofatoom tetraëdralen.
Fructose
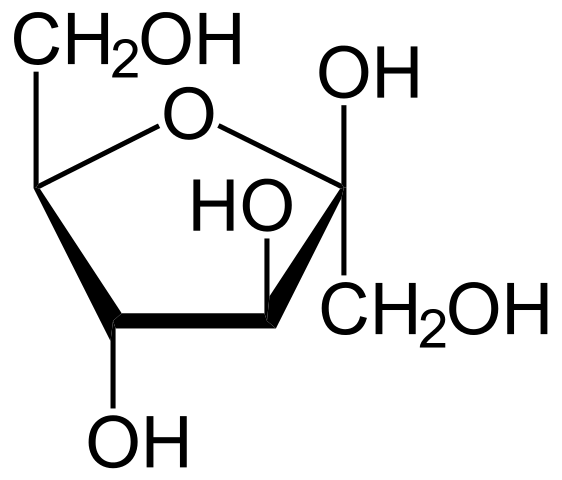 Structurele formule van beta-d-fructofuranosa. Bron: Neurotoger (Talk • Contribs) [Public Domain]
Structurele formule van beta-d-fructofuranosa. Bron: Neurotoger (Talk • Contribs) [Public Domain] We hebben de structurele formule van fructose, meer precies de Haworth -projectie van zijn furaneuze ring (vijf leden). Merk op hoeveel de structurele formule onthult in tegenstelling tot moleculaire, c6H12OF6, die samenvalt met die van glucose, beide zijn verschillende suikers.
Water
 Structurele waterformule. Bron: Benjah-bmm27 via Wikipedia.
Structurele waterformule. Bron: Benjah-bmm27 via Wikipedia. De chemische formule van water is h2Of, ook overeenkomend met gecondenseerde en moleculaire formules. Net als bij methaan, die het watermolecuul niet kent (en geen idee van chemische bindingen hebben) kan geloven dat hun structuur O-H-H is; Maar de structurele formule van het superieure beeld verduidelijkt de ware structuur.
Hoewel het niet wordt gewaardeerd, trekken de paren van elektronen vrij van zuurstof en waterstofatomen een tetraëder rond zuurstof; Dit is, elektronische watergeometrie: tetraëdral. Ondertussen vestigen de twee waterstofatomen een vlak dat vergelijkbaar is met een boemerang; Dit is, de moleculaire geometrie van water: hoekig.
Hoewel de structurele waterformule verreweg de eenvoudigste van de aangepakt voorbeelden is, verbergt meer geheimen en afwijkingen dan alleen.
Aspirine
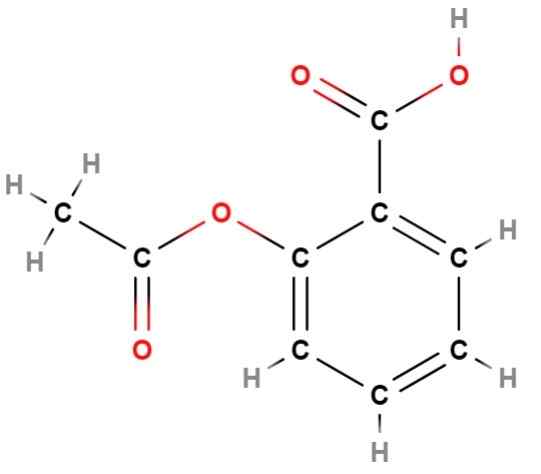 Structurele formule van aspirine. Bron: Gabriel Bolívar via Molview.
Structurele formule van aspirine. Bron: Gabriel Bolívar via Molview. We hebben een van de eerste "mislukkingen" van structurele formules: het onvermogen om het aromatische karakter van een structuur weer te geven; Dat het in dit geval overeenkomt met de aromaticiteit van de benzeen (zeshoekige) ring van aspirine (hierboven).
Kan u van dienst zijn: geconcentreerde oplossingAls deze formule zorgvuldig wordt waargenomen, wordt geconcludeerd dat het een molecuul is in platte essentie; Dat wil zeggen, bijna al zijn atomen "rusten" in hetzelfde vlak, behalve de methil3, Links, waar de tetraëdrische koolstofomgeving wordt gevisualiseerd.
Nogmaals, de structurele formule biedt veel meer informatie dan zijn gewone moleculaire formule, c9H8OF4; die overeenkomt met talloze structurele isomeren, totaal anders dan aspirine.
Benzeen
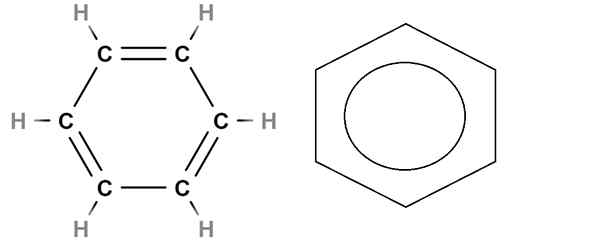 Benzeen structurele formule. Bron: Gabriel Bolívar via Molview.
Benzeen structurele formule. Bron: Gabriel Bolívar via Molview. Ten slotte hebben we de structurele benzeenformule hierboven. De moleculaire formule is c6H6, wat aangeeft dat het effectief zes koolstofatomen en zes waterstofatomen bevat. Maar hij zegt niets over de ware structuur van benzeen.
De dubbele bindingen C = C zijn niet statisch, als een paar elektronen, met name die in de orbitalen P van koolstof, het verhuist in de ring. Bijgevolg heeft benzeen verschillende resonantiestructuren, elk met een eigen structurele formule.
Deze verhuizing maakt deel uit van het aromatische karakter van benzeen, niet trouw weergegeven in de structurele formule van links. Het dichtst in de buurt is om de dubbele bindingen te vervangen door een cirkel (dona genoemd door sommigen) om de aromaticiteit van de ring aan te geven (rechts van de afbeelding).
En hoe zit het met de skeletformule? Dit lijkt erg op het structurele, dat alleen onderscheid maakt, omdat het geen waterstofatomen vertegenwoordigt; En daarom is het vereenvoudigder en is het comfortabeler om te grafiek. De benzeenring aan de rechterkant zou de skeletformule zijn.
Referenties
- Whitten, Davis, Peck & Stanley. (2008). Scheikunde. (8e ed.)). Cengage leren.
- Wikipedia. (2020). Structurele Formule. Opgehaald uit: in.Wikipedia.borg
- Nissa Garcia. (2020). Structurele formule: definitie en voorbeeld. Studie. Hersteld van: studie.com
- Clark Jim. (2012). Organische moleculen trekken. Hersteld van: chemguide.co.Uk
- William Reusch. (5 mei 2013). De vorm van moleculen. Hersteld van: 2.Scheikunde.MSU.Edu

