Verdunningsfactor
- 1422
- 78
- Kurt Aufderhar Jr.
 Seriële verdunning
Seriële verdunning Wat is de verdunningsfactor?
Hij Verdunningsfactor (FD) is een getal dat de tijden aangeeft dat een oplossing moet worden verdund om een lagere concentratie te verkrijgen. De oplossing kan een vaste, vloeibare of gasvormige opgeloste stof hebben opgelost.
Daarom hangt de concentratie ervan af van het aantal deeltjes van de opgeloste stof en het totale volume V.
Op het gebied van chemie worden veel uitingen van concentratie gebruikt: percentage, molair (m), normaal (n), onder andere. Elk van hen hangt af van een eindige hoeveelheid opgeloste stof; Van gram, kilogrammen of mol, tot equivalent.
Bij het verlagen van dergelijke concentraties is de FD echter van toepassing op al deze uitdrukkingen.
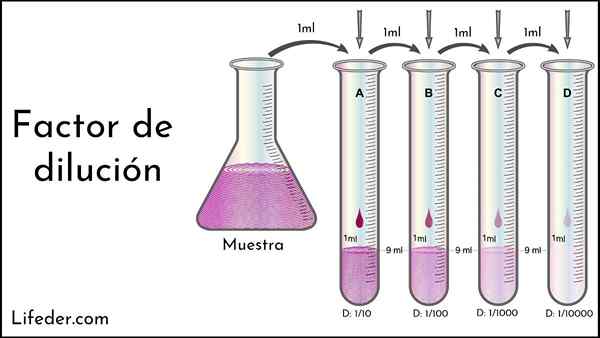
In het superieure beeld is er een voorbeeld van een opeenvolgende verdunning. Merk op dat van links naar rechts de violette kleur duidelijker wordt; die gelijk is aan een lagere concentratie van het monster.
De verdunningsfactor maakt het mogelijk om te bepalen hoe verdund het laatste vaartuig bevindt ten opzichte van de eerste. Dus in plaats van eenvoudige organoleptische eigenschappen, kan het experiment worden herhaald uit dezelfde FD uit dezelfde fles moederoplossing of monster, zodat er ervoor wordt gezorgd dat de concentraties van de nieuwe vaten gelijk zijn.
De concentratie kan in elke eenheid worden uitgedrukt; Het volume van de vaten is echter constant en om de berekeningen te vergemakkelijken, wordt het eenvoudig gebruikt voor de volumes van het monster opgelost in water. De som hiervan is gelijk aan V: het volume van totale vloeistof in het glas.
Net als bij het voorbeeldmonster gebeurt het in het laboratorium met een ander reagens. Geconcentreerde moedersoplossingen worden bereid, waarvan aliquots worden genomen en verdund om meer verdunde oplossingen te verkrijgen. Dit wil laboratoriumrisico's en reagensverliezen verminderen.
Wat is de verdunningsfactor?
Verdunning
Verdunning is een procedure die de concentratie van een oplossing of de dichtheid mogelijk maakt. De actie om de kleurintensiteit in een kleurstofoplossing te verminderen, kan ook als een verdunning worden beschouwd.
Om een oplossing met een bepaalde concentratie met succes te verdunnen, is het eerste dat moet worden gedaan om te weten hoe vaak de concentratie van de moederoplossing groter is in relatie tot de concentratie van de verdunde oplossing.
Het kan u van dienst zijn: kaliumdichromaat: formule, eigenschappen, risico's en gebruikAldus moeten de tijden dat de initiële oplossing wordt verdund om een oplossing te verkrijgen met de gewenste concentratie. Het aantal keren is wat bekend staat als de verdunningsfactor. En dit bestaat uit een dimensieloze fractie, die een verdunning aangeeft.
Factoren
Het is gebruikelijk om een verdunning te vinden, bijvoorbeeld als volgt: 1/5, 1/10, 1/100, enz. Dit geeft aan dat om een oplossing met de gewenste concentratie te verkrijgen, de moederoplossing die de noemer van de fractie noemde.
Als bijvoorbeeld 1/5 verdunning wordt gebruikt, moet de initiële oplossing worden verdund om een oplossing te verkrijgen met deze concentratie 5 keer. Daarom is nummer 5 de verdunningsfactor. Dit vertaalt zich als volgt: de 1/5 oplossing is vijf keer meer verdund dan de moeder.
Hoe u deze oplossing kunt voorbereiden? Als 1 ml van de moederoplossing wordt ingenomen, moet dit volume quintuped zijn, zodat de concentratie van de opgeloste stof wordt verdund door een 1/5 factor. Dus als het met water wordt verdund (zoals in het voorbeeld), moet 1 ml van deze oplossing 4 ml water worden toegevoegd (1+4 = 5 ml eindvolume VF)).
Vervolgens wordt opgemerkt hoe u de FD kunt afleiden en berekenen.
Hoe krijg je de verdunningsfactor?
Aftrek
Om een verdunning te bereiden, wordt een eerste oplossing of moeder naar een verergerde kolf gebracht, waar water wordt toegevoegd aan het voltooien van de maatregel van de bovengenoemde kolf.
In dit geval, wanneer water wordt toegevoegd aan de geaggoreerde kolf, wordt de massa van de opgeloste stof niet toegevoegd. Vervolgens blijft de massa opgeloste stof of de oplossing constant:
MJe = mF (1)
MJe = massa van de initiële opgeloste stof (in de geconcentreerde oplossing).
En MF = massa van de uiteindelijke opgeloste stof (in de verdunde oplossing).
Maar m = v x c. In vergelijking (1) vervangen u:
VJe X CJe = VF X CF (2)
VJe = Volume van de moeder of initiële oplossing die naar verdunning is gebracht.
CJe = concentratie van de moeder of initiële oplossing.
VF = volume van de verdunde oplossing die werd voorbereid.
CF = concentratie van de verdunde oplossing.
Vergelijking 2 kan als volgt worden geschreven:
CJe / CF = VF / VJe (3)
Twee geldige uitdrukkingen voor FD
Maar cJe / CF Per definitie is de Verdunningsfactor, Omdat het de tijden aangeeft dat de concentratie van de moeder of initiële oplossing groter is in relatie tot de concentratie van de verdunde oplossing.
Daarom geeft de verdunning aan die moet worden uitgevoerd om de oplossing te bereiden die uit de moederoplossing is verdund.
Kan u van dienst zijn: gedistilleerd waterEvenzo kan uit de observatie van vergelijking 3 worden geconcludeerd dat de relatie VF / VJe Het is een andere manier om de Verdunningsfactor. Dat wil zeggen, een van de twee uitdrukkingen (cJe/CF, VF/VJe) zijn geldig om de FD te berekenen. Het gebruik van het een of het ander hangt af van de beschikbare gegevens.
Voorbeelden
voorbeeld 1
Een NaCl -oplossing van 0,3 M werd gebruikt om een verdunde oplossing van 0,015 M te bereiden. Bereken de verdunningsfactorwaarde.
De verdunningsfactor is 20. Dit geeft aan dat om de verdunde oplossing van NaCl 0,015 m te bereiden, de 0,3 M NaCl -oplossing 20 keer moest worden verdund:
FD = CJe / CF
0,3 m / 0,015 m
twintig
Voorbeeld 2
Wetende dat de verdunningsfactor 15 is: welk volume water moet worden toegevoegd aan 5 ml van een geconcentreerde glucoseoplossing om de gewenste verdunning te maken?
Als eerste stap wordt het volume van de verdunde oplossing berekend (vF)). Eenmaal berekend, wordt het toegevoegde watervolume berekend om de verdunning te maken.
FD = VF / VJe.
VF = FD X VJe
15 x 5 ml
75 ml
Watervolume toegevoegd = 75 ml - 5 ml
70 ml
Vervolgens werden om de verdunde oplossing te bereiden met een verdunningsfactor van 15, 5 ml van de geconcentreerde oplossing 70 ml water toegevoegd aan het voltooien van het uiteindelijke volume van 75 ml.
Voorbeeld 3
De concentratie van een fructose -moederoplossing is 10 g/l. Het is gewenst om er een fructose -oplossing voor te bereiden met een concentratie van 0,5 mg/ml. Afnemen van de 20 ml moederoplossing naar verdunning: wat zou het volume van de verdunde oplossing moeten zijn?
De eerste stap om het probleem op te lossen is om de verdunningsfactor (FD) te berekenen. Eenmaal verkregen, wordt het volume van de verdunde oplossing berekend (VF)).
Maar voordat de berekening wordt verhoogd, is het noodzakelijk om de volgende observatie te maken: u moet de hoeveelheden fructoseconcentraties in dezelfde eenheden plaatsen. In dit specifieke geval is 10 g/L gelijk aan 10 mg/ml, wat deze situatie illustreert door de volgende transformatie:
(mg/ml) = (g/l) x (1.000 mg/g) x (l/1.000 ml)
Daarom:
10 g/l = 10 mg/ml
Doorgaan met de berekeningen:
Kan u van dienst zijn: aminesFD = CJe / CF
Fd = (10 mg/ml)/(0,2 mg/ml)
vijftig
Maar zoals VF = FD X VJe
VF = 50 x 20 ml
1.000 ml
Dus, 20 ml van de 10 g/L fructose -oplossing, 1L van 0,2 g/l -oplossing werd verdund.
Voorbeeld 4
Een methode voor het maken van seriële verdunningen zal worden geïllustreerd. Er is een glucose -oplossing met een concentratie van 32 mg/100 ml, en daaruit is deze gewenst/100 ml, 2 mg/100 ml en 1 mg/100 ml.
Procedure
5 testbuizen worden gelabeld voor elk van de concentraties die in de verklaring worden aangegeven. In elk van elk wordt 2 ml water bijvoorbeeld geplaatst.
Vervolgens aan buis 1 met water worden 2 ml van de moederoplossing toegevoegd. Het gehalte van buis 1 wordt geroerd en 2 ml van zijn inhoud wordt overgebracht naar buis 2. Op zijn beurt wordt buis 2 geagiteerd en worden 2 ml van de inhoud overgebracht naar buis 3; Op dezelfde manier gaan met buizen 4 en 5.
Uitleg
Aan buis 1 worden 2 ml water toegevoegd en 2 ml van de moederoplossing met een glucoseconcentratie van 32 mg/100 ml. Dus de uiteindelijke glucoseconcentratie in deze buis is 16 van mg/100 ml.
Aan buis 2 worden 2 ml water toegevoegd en 2 ml van het gehalte van buis 1 met een glucoseconcentratie van 16 mg/100 ml. Vervolgens wordt in buis 2 de concentratie van buis 1 2 keer verdund (FD). Dus de uiteindelijke concentratie van glucose in deze buis is 8 mg/100 ml.
Aan buis 3 2 ml water en 2 ml buis 2 -gehalte worden toegevoegd, met een glucoseconcentratie van 8 mg/100 ml. En net als de andere twee buizen, is de concentratie verdeeld in twee: 4 mg/100 ml glucose in buis 3.
Om de hierboven uitgelegde reden is de uiteindelijke concentratie van glucose in buizen 4 en 5 respectievelijk 2 mg/100 ml en 1 mg/100 ml.
De FD van buizen 1, 2, 3, 4 en 5, in relatie tot de moederoplossing, zijn respectievelijk: 2, 4, 8, 16 en 32.
Referenties
- Aus en tute. (S.F). Berekeningen van verdunningsfactor. Uitgebracht van: Ausetute.com.Au
- J.T. (S.F.)). Verdunningsfactor. [PDF]. Genomen uit: CSUS.Edu
- Verdunningen helpen (s.F.)). Genomen uit: uregina.AC
- Joshua (2011). Verschil tussen verdunning en verdunningsfactor. Verschil tussen.netto. Hersteld van: verschil tussen.netto
- Whitten, Davis, Peck & Stanley. Chemie (8e ed.)). Cengage leren.
- Innovarte (2014). Seriële verdunningen. Opgehaald uit: 3.Uah.is

