Dystrofine -eigenschappen, structuur en functies
- 3672
- 408
- Ernesto McKenzie
De dystrofine Het is een eiwit in de vorm van een stok of staaf geassocieerd met het membraan van skelet-, gladde en hartspiercellen, presenteert ook zenuwcellen en in andere organen van het menselijk lichaam.
Het heeft functies die vergelijkbaar zijn met die van andere cytoskeleteiwitten, en er wordt aangenomen dat het voornamelijk werkt in de stabiliteit van het spiervezelsmembraan en in de vereniging van het extracellulaire basale membraan met het intracellulaire cytoskelet.
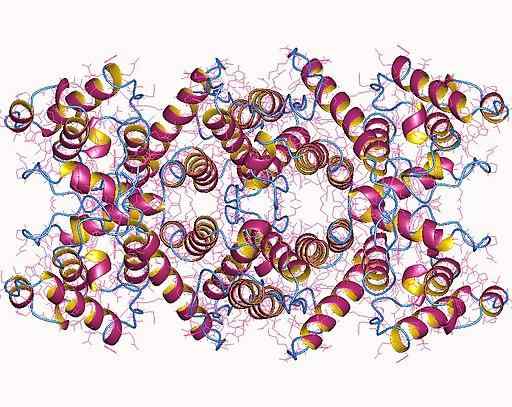
 Moleculaire structuur van dystrofine (Bron: Norwood, F.L., Sutherland-Smith, een.J., Behouden, n.H., Kendrick-Jones, J.; Visualisatie Auteur: gebruiker: Astrojan [CC BY-SA 4.0 (https: // creativeCommons.Org/licenties/by-sa/4.0)] via Wikimedia Commons)
Moleculaire structuur van dystrofine (Bron: Norwood, F.L., Sutherland-Smith, een.J., Behouden, n.H., Kendrick-Jones, J.; Visualisatie Auteur: gebruiker: Astrojan [CC BY-SA 4.0 (https: // creativeCommons.Org/licenties/by-sa/4.0)] via Wikimedia Commons) Het is gecodeerd op het X -chromosoom, in een van de grootste genen die voor mensen worden beschreven, wiens mutaties betrokken zijn bij pathologieën gekoppeld aan sekschromosomen, als Duchenne's spierdystrofie (DMD) (DMD) (DMD) (DMD).
Deze pathologie is de tweede meest voorkomende erfelijke aandoening ter wereld. Het treft een van de 3500 mannen en dat wordt duidelijk tussen 3 en 5 jaar als een versnelde spierslijtage die de levensduur kan verminderen tot niet meer dan 20 jaar.
Het dystrofine -gen werd voor het eerst geïsoleerd in 1986 en werd gekenmerkt met behulp van positionele klonering, wat een grote vooruitgang betekende voor de moleculaire genetica van die tijd.
[TOC]
Kenmerken
Dystrofine is een zeer divers eiwit dat wordt geassocieerd met het plasmamembraan van spiercellen (sarcolema) en dat van andere cellen van verschillende lichaamssystemen.
De diversiteit ervan is te wijten aan de processen die gerelateerd zijn aan de regulatie van de expressie van het gen dat het codeert, een van de grootste genen die voor mensen worden beschreven. Dit komt omdat het meer dan 2 heeft.5 miljoen basenparen, die ongeveer 0 vertegenwoordigen.1% van het genoom.
Deze gen. Het bestaat uit ongeveer 99% introns en het coderingsgebied is alleen weergegeven in 86 exons.
Kan u van dienst zijn: rood van fenol: kenmerken, voorbereiding, toepassingenDrie verschillende isovormen van dit eiwit worden erkend die voortkomen uit de vertaling van boodschappers die worden getranscribeerd uit drie verschillende promoters: een die alleen wordt aangetroffen in corticale en hippocampus -neuronen, een andere in Purkinje -cellen (ook in de hersenen), en de laatste in spier cellen (skelet en hart).
Structuur
Aangezien het dystrofine -gen kan worden "gelezen" van verschillende interne promotors, zijn er verschillende isovormen van dit eiwit die natuurlijk verschillende maten hebben. Op basis hiervan wordt de structuur van de "complete" en "korte" isovormen hieronder beschreven.
"Geheel" of "complete" isovormen
De "hele" isovormen van dystrofine zijn rietvormige eiwitten met vier essentiële domeinen (N-terminaal, centraal domein, rijk domein in cysteïnen en C-terminaal domein) die samen iets meer dan 420 kDa wegen en min of meer 3 hebben.685 aminozuurafval.
N-terminaal domein is vergelijkbaar met a-actinine (een actine-unie-eiwit) en kan tussen 232 en 240 aminozuren hebben, afhankelijk van de isovorm. Het centrale of stokdomein bestaat uit 25 drievoudige spiraalvormige herhaalde die vergelijkbaar met de spectrine en heeft ongeveer 3000 aminooacidaal afval.
Het C-terminale gebied van het centrale domein, dat wordt gevormd door een rijke rijk aan cysteïne, heeft ongeveer 280 afval en is zeer vergelijkbaar met de reden voor calciumunie in eiwitten zoals calmoduline, α-actinine en β β-spectrine. Het C-terminale domein van het eiwit bestaat uit 420 aminozuren.
"Korte" isovormen
Aangezien het dystrofine -gen ten minste vier interne promoters heeft, kunnen er eiwitten zijn met verschillende lengtes, die van elkaar verschillen door de afwezigheid van een van hun domeinen.
Elk van de interne promotors heeft een unieke voormalige exone), die worden uitgedrukt in verschillende regio's van het lichaam.
Kan u dienen: steroïde hormonen: structuur, synthese, werkingsmechanismeDP260 wordt uitgedrukt in het netvlies en bestaat samen met "complete" spier- en hersenvormen. DP140 wordt gevonden in de hersenen, in het netvlies en in de nieren, terwijl DP116 alleen wordt aangetroffen in de perifere zenuwen van volwassenen en DP71 is in de meeste niet -muscle -weefsels.
Functie
Volgens verschillende auteurs heeft dystrofine verschillende functies die niet alleen de deelname ervan als een cytoskeleteiwit impliceren.
Membranale stabiliteit
De belangrijkste functie van dystrofine, als een molecuul geassocieerd met het zenuw- en spiercelmembraan, is om te interageren met ten minste zes verschillende uitgebreide membraaneiwitten, waarmee het samenkomt met dystropine-glucoproteïne-complexen.
De vorming van dit complex genereert een "brug" door de spier- of sarcolema -celmembraan en verbindt "flexibel" het basale vel van de extracellulaire matrix met het interne cytoskelet.
Het dystrofine-glucoproteïne-complex werkt bij de stabilisatie van het membraan en bij de bescherming van spiervezels tegen necrose of schade veroorzaakt door geïnduceerde contractie gedurende lange tijd, die is aangetoond door reverse genetica.
Deze "stabilisatie" wordt meestal gezien als een analoog.
Signaaltransductie
Dystrofine of, liever, het eiwitcomplex dat vormt met glycoproteïnen in het membraan heeft niet alleen structurele functies, maar wees er ook op dat het enkele functies kan hebben in cellulaire signalering en communicatie.
De locatie suggereert dat het kan deelnemen aan de overdracht van spanning van actinefilamenten in spiervezel sarcomers door het plasmamembraan naar de extracellulaire matrix, omdat het fysiek geassocieerd is met deze filamenten en met extracellulaire ruimte.
Het kan u van dienst zijn: Bright Green Agar: wat is, fundering, voorbereiding, gebruikBewijs van andere functies in signaaltransductie is losgemaakt van sommige onderzoeken die zijn uitgevoerd met mutanten voor het dystrofine -gen, waarbij defecten worden waargenomen bij signalering van watervallen die te maken hebben met geprogrammeerde celdood of celafweer.
Referenties
- Ahn, a., & Kunkel, l. (1993). De structurele en functionele diversiteit van dystrofine. Natuurgenetica, 3, 283-291.
- Doubek, r. W. (1950). High-yield histologie (2e ed.)). Philadelphia, Pennsylvania: Lippinott Williams & Wilkins.
- Ervasti, J., & Campbell, K. (1993). Dystrofine en het membraankelet. Huidige mening in celbiologie, 5, 85-87.
- Hoffman, E. P., Bruin, r. H., & Kunkel, l. M. (1987). Dystrofine: het eiwitproduct van de Duchenne -spierdystrofie -locus. Cel, 51, 919-928.
- Koenig, m., Monaco, een., & Kunkel, l. (1988). Het complete sequentie staafvormige cytoskelet van dystrofine-eiwit voorspelt een. Cel, 53, 219-228.
- Lezen., Winder, s. J., & Hubert, J. (2010). Biochimica et biophysica acta dystrophin: meer dan alleen de som van zijn delen. Biochimica et Biophysica Acta, 1804(9), 1713-1722.
- Liefde, D., Byth, b., Tensley, J., Blake, D., & Davies, K. (1993). Dystrofine en dystrofine-gerelateerde eiwitten: een overzicht van eiwit- en RNA-onderzoeken. Neuromusc. Afnemen., 3(1), 5-21.
- MUNTONI, F., Torelli, s., & Ferlini, tot. (2003). Dystrofine en mutaties: één gen, verschillende eiwitten, meerdere fenotypes. De Lancet -neurologie, 2, 731-740.
- Pasternak, c., Wong, s., & Elson, E. L. (negentienvijfennegentig). Mechanische functie van dystrofine in spiercellen. Journal of Cell Biology, 128(3), 355-361.
- Sadoulet-puccio, h. M., & Kunkell, l. M. (1996). Dystrofine en zijn lsovormen. Hersenpathologie, 6, 25-35.
- « OxiHemoglobin -kenmerken, structuur en junctie curve
- Tropomiosine -kenmerken, structuur en functies »

