Dihydroxyacetonstructuur, eigenschappen, het verkrijgen, gebruiken
- 988
- 6
- Pete Heaney V
De Dihydroxyaceton Het is een saccharide of suiker die bestaat uit de eenvoudigste ketose van allemaal, en waarvan de moleculaire formule c is3H6OF3. Het is daarom een structureel isomeer van de glyceraldehyde, die kan worden beschouwd als een geoxideerde versie van glycerine. Zijn naam is afgekort met de DHA-letters, zowel in het Engels als in het Spaans, en kent hem ook met de namen 1,3-dihydroxyaceton, glyceone of 1.3-dihydroxi-2-propanone.
In tegenstelling tot andere suikers mist de DHA asymmetrische koolstofatomen, dus heeft het geen D- of L -configuratie of presenteert deze optische activiteit; dat wil zeggen, je kunt het gepolariseerde licht niet afleiden. Wat het gemeen heeft met suikers, een Zea zijn, is een karakteristieke zoete smaak en een geweldige oplosbaarheid in water.
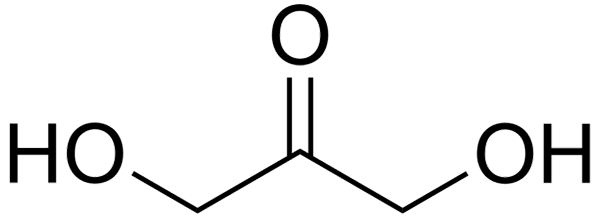 Structurele formule van dihydroxyaceton
Structurele formule van dihydroxyaceton In het superieure beeld hebben we de structurele formule van dihydroxyaceton. Groep C = O Central is de reden waarom de DHA een kettose is.
De DHA is in staat om te reageren met de amineische groepen van de keratines die het buitenste oppervlak van onze huid vormen, het stratum corneum genoemd, waardoor pigmenten van oranje tonaliteiten worden geproduceerd die uiteindelijk het uiterlijk geven van een natuurlijke kleur. Dit is de reden waarom de DHA wordt gebruikt als een actief ingrediënt in de bronzen producten zonder zon.
[TOC]
Structuur

In het bovenste beeld hebben we de structuur van een DHA -molecuul voorgesteld met een bollen en barsmodel. Zoals te zien is, komen de rode bollen overeen met zuurstofatomen. De geometrie is bijna plat, omdat de OH- en H -groepen enigszins opvallen van het vlak gevormd door de drie koolstofatomen en het carbonyloxygenatoom.
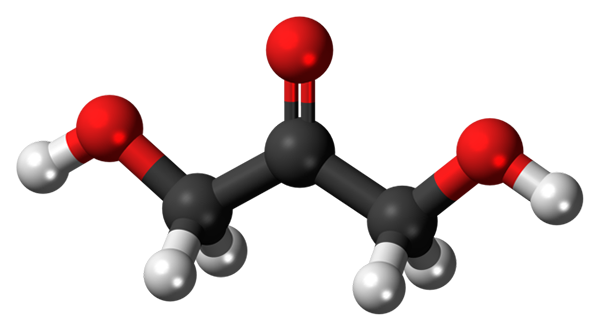 Moleculaire structuur van dihydroxyaceton. Bron: Jynto / CC0
Moleculaire structuur van dihydroxyaceton. Bron: Jynto / CC0 Het molecuul van DHA is behoorlijk polair. Groepen C = O en C-OH laten een hoge elektronische dichtheid achter, terwijl hun koolstofskelet slechte elektronen is.
Kan u van dienst zijn: acetophenoneDe intermoleculaire interacties zijn daarom gebaseerd op de dipool-dipolo-krachten, vooral die van waterstofbruggen. Dit alles draagt bij aan de DHA bestaat als een kristallijne vaste stof onder normale omstandigheden.
Eigenschappen van dihydroxyaceton
Fysiek uiterlijk
Kleurrijke kristallijne vaste stof, met een zoete en karakteristieke geur en smaak. Het is zeer hygroscopisch, dus het absorbeert het vocht van de omgeving.
Molaire massa
90.078 g/mol
Smeltpunt
89 tot 91 ºC. Deze onnauwkeurige waarde is te wijten aan het feit dat niet alle DHA -moleculen in de verklaarde staat zijn, maar dat de overgrote meerderheid van hen schemering vormt.
Kookpunt
Onbepaald, omdat het kapot gaat.
Oplosbaarheid
Het is erg oplosbaar in water, met een geschatte oplosbaarheid van 930 kg/l tot 25 ºC. Dit komt door zijn zeer polaire karakter, en het vermogen van water om het te hydrateren door waterstofbruggen te vormen met een van de drie zuurstofatomen van zijn molecuul. Het lost echter langzaam op in een mengsel van water-stanol 1:15.
Hydrolyse en oplossing
In de vaste toestand bestaat de DHA vaak als een dommer. De transformatie zou hieronder worden getoond:
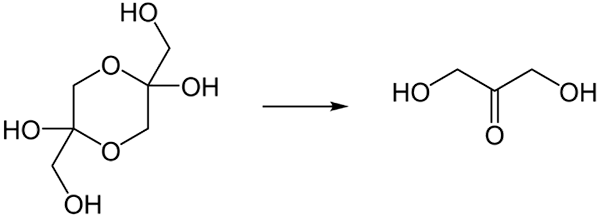 DHA's dimeerconversie naar uw monomeer wanneer opgelost in het water. Bron: Steffen 962 bij Duitse Wikipedia / Public Domain
DHA's dimeerconversie naar uw monomeer wanneer opgelost in het water. Bron: Steffen 962 bij Duitse Wikipedia / Public Domain De DHA zijn in zijn zeer hygroscopische monomere vorm, snel wanneer het droogde en het vocht van het vocht blijkt om het dimeer te vestigen met zijn dioxaanse ring.
Het verkrijgen en synthese
Natuurlijk kan de DHA worden verkregen door deze te extraheren uit suikerrieten of suikerbieten.
Aan de andere kant, als het gaat om het synthetiseren of produceren van deze zijn er verschillende alternatieven, allemaal gebaseerd op de oxidatiereactie van glycerine. Een daarvan is om glycerine of glycerol te oxideren met waterstofperoxide met behulp van ijzers zouten zoals katalysatoren. In een andere reactie oxideert glycerine met lucht, zuurstof of benzoquinon maar met behulp van speciale paladiumkatalysatoren.
Kan u van dienst zijn: Perrin Atomic Model: kenmerken, postulatenWe hebben ook de commerciële productiemethode van de DHA, waarbij glycerine wordt geoxideerd met behulp van azijnzuurbacteriën in een gistingsproces.
Tijdens de synthese van de DHA is er ook glyceraldehyde, zijn structurele isomeer.
Risico's
De risico's rond de DHA zijn niet helemaal duidelijk. In zijn gefosfeerde vorm is het dihydroxyacetonfosfaat een product van glycolyse en een intermediair in fructosemetabolisme, omdat het isomerase-triosofosfaat-enzym het transformeert in d-glyceraldehyde 3-fosfaat. Volgens medische studies kan een overmatige dosis DHA echter dit hele mechanisme negatief veranderen en zelfs celdood veroorzaken.
Daarom wordt de DHA als gevaarlijk beschouwd als deze wordt ingenomen of als deze vooral wordt ingeademd. Daarnaast zijn er studies die bevestigen dat hun actuele toepassingen de concentratie van reactieve geoxygeneerde soorten (ROS) verhogen, die huidcellen aanvallen die hun veroudering produceren en het uiterlijk van rimpels.
Deze onderpandreactie ziet er nog meer geaccentueerd uit wanneer de huid geïmpregneerd met DHA wordt blootgesteld aan de UV -stralen van de zon, dus de risico's van schade aan de huidverhoging.
Experts raden daarom aan om DHA niet te gebruiken in buitenruimtes onmiddellijk nadat de bruiningslotions op de huid zijn aangebracht.
Om dit risico te verminderen, bevatten lotions additieven zoals groente- en antioxiderende oliën, naast microcapsulas die geleidelijk de DHA afgeven.
Dihydroxyaceton gebruik
 De bruine lotions met DHA zijn een veiligere optie wanneer de huid bruist is zonder zichzelf bloot te stellen aan de zonnestralen
De bruine lotions met DHA zijn een veiligere optie wanneer de huid bruist is zonder zichzelf bloot te stellen aan de zonnestralen Dihydroxyaceton is synoniem met cosmetica, omdat het het actieve ingrediënt is van veel zonneproducten, Creams, Sparties, Masks, Lotions, enz. Bij het aanbrengen van deze bronzers op de huid vindt de reactie van Mailrd plaats, verantwoordelijk voor dat het een meer oranje kleur krijgt, zonder het strand te bezoeken of zichzelf bloot te stellen aan lange uren onder de ochtendzon.
Het kan u van dienst zijn: chemische ondoordringbaarheidAanvankelijk, tegen 1960, waren de bruin overdreven oranje, in die mate dat het grote publiek gedurende tientallen jaren dit soort leerlooier heeft afgewezen. Sindsdien waren de formuleringen echter aan het verbeteren, zodat de gebruinde er natuurlijker, stralend en aangenaam uitzagen, terwijl ze na hun gebruik lagere risico's garanderen, terwijl ze een lagere risico's garanderen.
Verschillende merken, waaronder Coco Channel, verlaagden DHA -concentraties tot een maximum van 20%, die ze ook erythrule opnemen, een andere suiker die ook reageert met huideiwitten en componenten die de effecten van UV -stralen neutraliseren. Ze probeerden ook de duurzaamheid van de bruin na toepassing te verlengen.
Tegenwoordig komen er nieuwe zonnebankproducten op de markt, die zullen bloeien totdat medische studies verklaren dat de TAN niet de mogelijke risico's van de actuele DHA -toepassing gebruikt, waarvan wordt aangenomen dat het zichzelf kan absorberen in de diepste lagen van de huid.
Referenties
- Graham Solomons T.W., Craig B. Friteuse. (2011). Organische chemie. (10e Editie.)). Wiley Plus.
- Carey F. (2008). Organische chemie. (Zesde editie). MC Graw Hill.
- Morrison en Boyd. (1987). Organische chemie. (Vijfde editie). Addison-Wesley IberoAmericana.
- Cyriminna, r., Fidalgo, een., Ilharco, l. M., & Pagliaro, m. (2018). Dihydroxyaceton: een bijgewerkt inzicht in een belangrijk bioproduct. Chemie, 7(3), 233-236. doen.org/10.1002/Open.201700201
- Wikipedia. (2020). Dihydroxyaceton. Opgehaald uit: in.Wikipedia.borg
- Nationaal centrum voor biotechnologie -informatie. (2020). Dihydroxyaceton. PubChem Comunund Samenvatting voor CID 670. Hersteld van: pubchem.NCBI.NLM.NIH.Gov
- Mary Gallagher. (2018). Blootstelling aan dihydroxyaceton bij zonloze zonnebankproducten inzicht in de risico's. Dermatology Nurses 'Association. Doi: 10.1097/jdn.0000000000000366

