Coprecipitatie
- 2001
- 134
- Ernesto McKenzie
Wat is coprecipitatie?
De Coprecipitatie Het is de neerslag van een vaste stof die normaal oplosbare stoffen sleept en die optreden in de vaste stof of op het oppervlak tegelijkertijd met dit neerslag.
Op deze manier gezien kunt u besmetting genereren van een onoplosbare stof die opgeloste opgeloste opgeloste stoffen van het vloeibare medium draagt. Het woord 'vervuiling' wordt toegepast op die gevallen waarin oplosbare opgeloste opgeloste stoffen die worden neergeslagen door onoplosbare ondersteuning zijn ongewenst, maar als ze dat niet zijn, is het een alternatieve analytische of synthetische methode.
Aan de andere kant is onoplosbare ondersteuning de steile substantie. Dit kan de oplosbare opgeloste stof binnen (absorptie) of op het oppervlak (adsorptie) dragen. De manier waarop het de fysicochemische eigenschappen van de resulterende vaste stof volledig zal veranderen.
Hoewel het concept van coprecipitatie misschien een beetje verwarrend lijkt, komt het vaker voor dan wordt gedacht, omdat meer dan eenvoudige besmette vaste stoffen, solide oplossingen van complexe structuren en rijk aan onschatbare componenten worden gevormd. Het land waaruit planten worden gevoed, is een voorbeeld van coprecipitatie.
Evenzo zijn mineralen, keramiek, klei en onzuiverheden in ijs ook een product van dit fenomeen. Zo niet, dan zouden de bodem een groot deel van hun essentiële elementen verliezen, zouden mineralen niet zijn zoals ze bekend zijn, en er zou ook geen belangrijke methode zijn voor de synthese van nieuwe materialen.
Voorbeeld van coprecipitatie
Om het idee van coprecipitatie beter te begrijpen, wordt het volgende voorbeeld geboden.
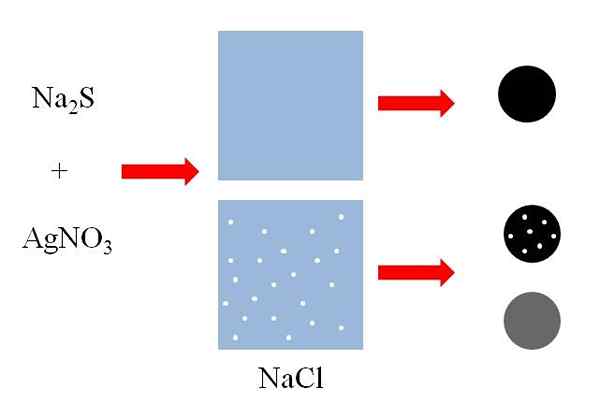
 Voorbeelden van coprecipitatie. Bron: Gabriel Bolívar
Voorbeelden van coprecipitatie. Bron: Gabriel Bolívar Top (superieure afbeelding) Er zijn twee containers met water, waarvan er één opgeloste NaCl bevat. NaCl is een zeer oplosbaar zoutzout, maar witte puntengroottes zijn overdreven voor verklarende doeleinden. Elk wit punt wordt kleine NaCl -aggregaten in een oplossing voor de rand van verzadiging.
Kan u van dienst zijn: Fermio (FM)Aan beide containers toegevoegd een mengsel van natriumsulfide, na2S en zilvernitraat, agno3, Het zal een solide onoplosbare zwarte zilveren zwavel, AGS neerslaan:
NA2S + Agno3 => Ags + nano3
Zoals te zien is in de eerste container met water, neerslaat. Deze vaste stof in de opgeloste NaCl -container draagt echter deeltjes van dit zout (zwarte bol met witte punten). NaCl is in water oplosbaar, maar wanneer de ags neerslaat, adsorbeert het op het zwarte oppervlak.
Er wordt dan gezegd dat de NaCl coprecipiteerde over de AGS. Als de zwarte vaste stof werd geanalyseerd, kunnen NaCl -microcristallen op het oppervlak worden waargenomen.
Deze kristallen kunnen echter ook in de AG's zijn, dus de vaste stof zou grijs "worden" (wit + zwart = grijs).
Soorten Coprecipitatie
De zwarte bol met witte punten, en de grijze bol laat zien dat een oplosbare opgeloste stof op verschillende manieren kan coprecipiteren.
In het eerste doet het zo oppervlakkig, geadsorbeerd op de onoplosbare ondersteuning (Ags in het vorige voorbeeld), terwijl het in het tweede de zwarte kleur van het neerslag "verandert".
Kunnen andere soorten vaste stoffen worden verkregen? Dat wil zeggen een sfeer met zwarte en zwarte fasen, dat wil zeggen van AGS en NaCl (samen met Nano3 dat ook coprecipita). Dit is waar de vindingrijkheid van de synthese van nieuwe vaste stoffen en materialen ontstaat.
Terugkerend naar het initiële punt, in principe de oplosbare coprecipita opgeloste opgeloste stof die verschillende soorten vaste stoffen genereert. De soorten coprecipitatie en de vaste stoffen die daaruit voortvloeien, worden hieronder vermeld.
Het kan u van dienst zijn: materialen die weinig weerstand hebben tegen de doorgang van elektriciteitInclusie
Er is sprake van inclusie wanneer in het kristallijne netwerk een van de ionen kan worden vervangen door een deel van de coprecipiteerde oplosbare stof.
Als NaCl bijvoorbeeld had gecoprecipiteerd door inclusie, na ionen+ Ze zouden de plaats van de AG hebben bezet+ In een deel van de kristallijne opstelling.
Van alle soorten coprecipitatie is dit echter het minst waarschijnlijk, omdat, om te voorkomen, ionische radio's zeer vergelijkbaar moeten zijn. Terugkerend naar de grijze sfeer van het beeld, zou inclusie worden weergegeven door een van duidelijkere grijze tonen.
Zoals gezegd, wordt opname gegeven in kristallijne vaste stoffen en om ze te verkrijgen, domein van de chemie van oplossingen en verschillende factoren (t, pH, agitatietijd, molaire relaties, enz.)).
Occlusie
In occlusie worden de ionen gevangen in het kristallijne netwerk, maar zonder een ion van de opstelling te vervangen. Binnen de AGS kunt u bijvoorbeeld OCLUIDO -kristallen vormen. Grafisch kan het worden gevisualiseerd als een wit kristal omgeven door zwarte kristallen.
Dit type coprecipitatie is een van de meest voorkomende, en dankzij het is er de synthese van nieuwe kristallijne vaste stoffen. Obluiddeeltjes kunnen niet worden geëlimineerd met eenvoudige wasbeurten. Om dit te doen, zou het nodig zijn om de gehele set te herkrytiseren, dat wil zeggen de onoplosbare ondersteuning.
Zowel inclusie als occlusie zijn absorptieprocessen gegeven in kristallijne structuren.
Adsorptie
Bij adsorptie ligt de coprecipiteerde vaste stof op het oppervlak van de onoplosbare ondersteuning. De grootte van de deeltjes van deze ondersteuning definieert het type vaste vaste stof.
Kan u van dienst zijn: isóbarosAls ze klein zijn, wordt een gecoaguleerde vaste stof verkregen, waaruit het gemakkelijk is om onzuiverheden te elimineren. Maar als ze erg klein zijn, zal de vaste stof overvloedige hoeveelheden water absorberen en gelatineus zijn.
Terugkerend naar de zwarte bol met witte punten, kunnen coprecipiteerde NaCl -kristallen op de AG's worden gewassen met gedestilleerd water. Dus aan, tot het zuiveren van de AG's, die dan kunnen verwarmen om al het water te verdampen.
Toepassingen van de Coprecipitatie
Sommige van de coprecipitatietoepassingen zijn de volgende:
- Maakt het mogelijk om oplosbare stoffen te kwantificeren die niet gemakkelijk uit het medium kunnen worden neergeslagen. Door een onoplosbare ondersteuning leidt het dus bijvoorbeeld, bijvoorbeeld radioactieve isotopen, zoals Francio, voor latere studie en analyse.
- Bij coprecipiterende ionen in gelatineuze vaste stoffen wordt het vloeibare medium gezuiverd. Occlusie is in deze gevallen nog meer gewenst, omdat onzuiverheid niet zal kunnen ontsnappen.
- Coprecipitatie maakt het mogelijk om stoffen in vaste stoffen op te nemen tijdens hun formatie. Als de vaste stof een polymeer is, absorbeert het oplosbare opgeloste stoffen die vervolgens binnen coprecipiteren, waardoor het nieuwe eigenschappen krijgt. Als het bijvoorbeeld cellulose is, kan kobalt (of ander metaal) worden gemaakt voor coprecipiet.
- Naast al het bovenstaande is coprecipitatie een van de belangrijkste methoden voor de synthese van nanodeeltjes over een onoplosbare ondersteuning. Dankzij dit zijn bionanomaterialen en magnetiet nanodeeltjes gesynthetiseerd, onder vele anderen.
Referenties
- Neerslag en co-precipitatie. Nptel hersteld.AC.in
- Wat is coprecipitatie. Hersteld van WISEGEEK.com

