Ketogenesetypen van lichamen, synthese en afbraak
- 897
- 215
- Pete Heaney V
De ketogenese Het is het proces waarbij acetoacetaat, β-hydroxybutiraten en aceton worden verkregen, die samen ketonlichamen worden genoemd. Dit complexe en fijn gereguleerde mechanisme wordt uitgevoerd in mitochondriën, van het katabolisme van vetzuren.
Het verkrijgen van de ketonlichamen vindt plaats wanneer het lichaam wordt onderworpen aan uitputtende perioden van vasten. Hoewel deze metabolieten meestal worden gesynthetiseerd in levercellen, worden ze gevonden als een belangrijke energiebron in verschillende weefsels, zoals skeletspier en in hart- en cerebrale weefsels.
 Bron: Sav Vas [CC0]
Bron: Sav Vas [CC0] Β-hydroxibutirate en acetoacetaat zijn metabolieten die worden gebruikt als substraten in hartspier en nierschors. In de hersenen worden ketonlichamen belangrijke energiebronnen wanneer het lichaam zijn glucose -reserve heeft uitgeput.
[TOC]
Algemene karakteristieken
Ketogenese wordt beschouwd als een zeer belangrijke fysiologische of metabole route. Over het algemeen wordt dit mechanisme in de lever uitgevoerd, hoewel is aangetoond dat het kan worden uitgevoerd in andere weefsels die in staat zijn om vetzuren te metaboliseren.
De vorming van ketonlichamen is de belangrijkste metabole afleiding van acetyl-CoA. Deze metaboliet wordt verkregen vanaf de metabole route die bekend staat als β-oxidatie, wat de afbraak van vetzuren is.
De beschikbaarheid van glucose in de weefsels waar β-oxidatie optreedt, bepaalt de metabole bestemming van acetyl-CoA. In bepaalde situaties worden geoxideerde vetzuren bijna volledig gericht op de synthese van ketonlichamen.
Typen en eigenschappen van ketonlichamen
Het belangrijkste ketonische lichaam is acetoacetaat of acetoazijnzuur, dat meestal wordt gesynthetiseerd in levercellen. Van acetoacetaat zijn de andere moleculen die deel uitmaken van de ketonlichamen afgeleid.
De reductie van acetoazijnzuur geeft aanleiding tot D-β-hydroxybutiraten, het tweede ketonische lichaam. Aceton is een moeilijke verbinding om af te breken en wordt geproduceerd door een spontane decarboxyleringsreactie van acetoacetaat (dus het vereist geen interventie van enzym), wanneer het aanwezig is in hoge concentraties in bloed.
De denominatie van ketonlichamen is gerangschikt door conventie, omdat strikt genomen β-hydroxybutiraten geen ketonfunctie heeft. Deze drie moleculen zijn oplosbaar in water, wat hun bloedtransport vergemakkelijkt. De belangrijkste functie is om bepaalde weefsels energie te leveren als skelet- en hartspier.
De enzymen die betrokken zijn bij de vorming van ketonlichamen zijn voornamelijk in de lever en nieren, waarin wordt verklaard dat deze twee locaties de belangrijkste producenten van deze metabolieten zijn. De synthese ervan vindt alleen plaats en uitsluitend in de mitochondriale matrix van cellen.
Het kan u van dienst zijn: sporulatie: in planten, in schimmels en in bacteriënZodra deze moleculen zijn gesynthetiseerd, gaan ze naar de bloedbaan die de weefsels aanpakken die ze vereisen, waar ze afbreken tot Acetyl-CoA.
Synthese van ketonlichamen
Voorwaarden voor ketogenese
De metabole bestemming van acetyl-CoA van β-oxidatie hangt af van de metabolische vereisten van het organisme. Dit is geoxideerd voor CO2 en h2Of door de citroenzuurcyclus of de synthese van vetzuren, als het metabolisme van lipiden en koolhydraten stabiel is in het lichaam.
Wanneer het lichaam koolhydraten nodig heeft, wordt oxalacetaat gebruikt voor glucoseproductie (gluconeogenese) in plaats van het starten van de citroenzuurcyclus. Dit gebeurt, zoals vermeld, wanneer het lichaam enig onvermogen heeft om glucose te verkrijgen, in gevallen zoals langdurig vasten of de aanwezigheid van diabetes.
Hierdoor wordt de acetyl-CoA als gevolg van de oxidatie van vetzuren gebruikt voor de productie van ketonlichamen.
Mechanisme
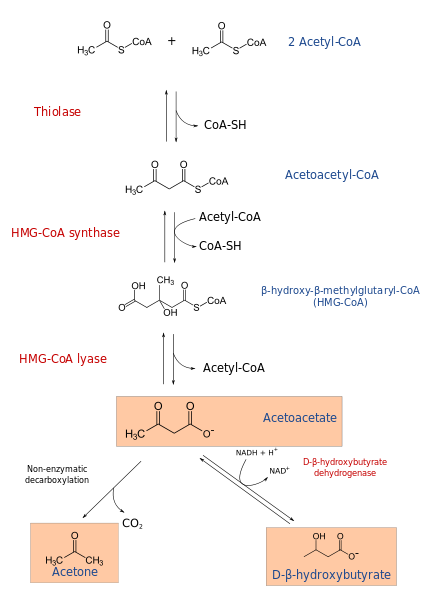
Het ketogenese-proces begint uit de producten van β-oxidatie: acetacetyl-CoA of acetyl-CoA. Wanneer het substraat acetyl-CoA is, bestaat de eerste stap uit de condensatie van twee moleculen, acetyl-CoA-transferase-reactie, om acetacetyl-CoA te produceren.
De acetacetyl-CoA wordt gecondenseerd met een derde acetyl-CoA door de werking van het HMG-CoA-synthase, om HMG-CoA te produceren (β-hydroxy-β-methylglutaril-coa). De HMG-CoA wordt afgebroken tot acetoacetaat en acetyl-CoA door HMG-CoA liasa-actie. Op deze manier wordt het eerste ketonische lichaam verkregen.
Acetoacetaat wordt gereduceerd tot β-hydroxybutiraat door de interventie van β-hydroxybutiraat dehydrogenase. Deze reactie hangt af van NADH.
Het belangrijkste ketonische acetoacetaatlichaam is een β-cethoacid, die niet-enzymatische decarboxylering ervaart. Dit proces is eenvoudig en produceert aceton en co2.
Deze reeks reacties resulteert dus in ketonlichamen. Deze worden oplosbaar in water kan op een eenvoudige manier worden getransporteerd door de bloedcirculatie, zonder de noodzaak om te verankeren naar een albuminestructuur, zoals het geval is van vetzuren die onoplosbaar zijn in waterig medium.
Β-oxidatie en ketogenese zijn gerelateerd
Vetzuurmetabolisme produceert substraten voor ketogenese, dus deze twee manieren zijn functioneel gerelateerd.
Acetoacethyl-CoA is een remmer van het metabolisme van vetzuren, omdat het de activiteit van het acyl-CoA-dehydrogenase stopt dat het eerste enzym van β-oxidatie is. Bovendien oefent het ook remming uit op acetyl-CoA-overdracht en HMG-CoA-synthase.
Het HMG-CoA-synthase-enzym, onderworpen aan het CPT-I (enzym dat betrokken is bij de productie van acylcarnitine bij β-oxidatie), vertegenwoordigt een belangrijke regulerende rol bij de vorming van vetzuren.
Het kan u van dienst zijn: Flora en Fauna van Zacatecas: meer representatieve soortenRegulatie van β-oxidatie en het effect ervan op ketogenese
Organisme -voeding reguleert een complexe set hormonale signalen. Koolhydraten, aminozuren en lipiden die in het dieet worden geconsumeerd, worden afgezet in de vorm van triacylglycerolen in het vetweefsel. Insuline, een anabolisch hormoon, komt tussenbeide in de synthese van lipiden en de vorming van triacylglyceroles.
Op mitochondriaal niveau wordt β-oxidatie geregeld door de invoer en deelname van sommige substraten in de mitochondria. Het enzym cpt i synthetiseert carnitine -acyl van acil cytosolische acil.
Wanneer het lichaam wordt gevoed, verhoogt acetyl-CoA-carboxylase en citraat de niveaus van CPT I, terwijl het zijn fosforylering vermindert (cyclische AMP-afhankelijke reactie).
Dit veroorzaakt een accumulatie van Malonil CoA, die de synthese van vetzuren stimuleert en de oxidatie ervan blokkeert, waardoor een zinloze cyclus wordt gegenereerd,.
In het geval van vasten is de activiteit van carboxylase zeer laag omdat de niveaus van het enzym CPT I zijn verlaagd en ook gefosforyleerd, activering en bevordering van de oxidatie van lipiden, die vervolgens de vorming van de ketonlichamen tot acetyl mogelijk maken -Coa.
Degradatie
De ketonlichamen verspreiden zich buiten de cellen waar ze werden gesynthetiseerd en worden door de bloedbaan naar de perifere weefsels getransporteerd. In deze weefsels kunnen ze worden geoxideerd door de cyclus van tricarbonzuren.
In perifere weefsels wordt β-hydroxybutiraat geoxideerd tot acetoacetaat. Vervolgens wordt het huidige acetoacetaat geactiveerd door de werking van het 3-ZOA-transferase-enzym.
Succinil-Coa fungeert als een COA-donor die succinaat wordt. De activering van acetoacetaat treedt op om succinyl-CoA te voorkomen.
De resulterende aceoacetyl-CoA lijdt aan een thiolithische breuk die twee acetyl-CoA-moleculen produceert die zijn opgenomen in de cyclus van tricarbonzuren, beter bekend als Krebs-cyclus.
Levercellen missen de overdracht van 3-cotoacil-CoA, waardoor deze metaboliet in deze cellen wordt geactiveerd. Op deze manier is het gegarandeerd dat de ketonlichamen niet oxideren in de cellen waar ze zijn geproduceerd, maar dat ze kunnen worden overgebracht naar de weefsels waar hun activiteit vereist is.
Medische relevantie van ketonlichamen
In het menselijk lichaam kunnen hoge concentraties ketonlichamen in het bloed speciale aandoeningen veroorzaken die acidose en ketonemie worden genoemd.
Kan u dienen: Sphingomyeline: wat is, structuur, functies, syntheseDe productie van deze metabolieten komt overeen met het katabolisme van vetzuren en koolhydraten. Een van de meest voorkomende oorzaken van een toestand van pathologische ketogenese is de hoge concentratie van aërische gedicarboneerde fragmenten die niet afbreken op de oxidatieroute van tricarbonzuren.
Als gevolg hiervan is er een toename van de niveaus van bloedketonlichamen boven 2 tot 4 mg/100 N en hun aanwezigheid in urine. Dit vertaalt zich in de verstoring van het intermediaire metabolisme van deze metabolieten.
Bepaalde defecten in de hypofyse -neuroglandulaire factoren die de afbraak en synthese van de ketonlichamen reguleren, samen met aandoeningen in koolwaterstofmetabolisme, zijn de oorzaak van de toestand van hypercetonemie.
Diabetes mellitus en accumulatie van ketonische lichamen
Diabetes mellitus (type 1) is een endocriene ziekte die een toename van de productie van ketonlichamen veroorzaakt. Insuline ontoereikende productie schakelt glucose uit aan de spieren, lever en vetweefsel, dus accumuleren in bloed.
Cellen in afwezigheid van glucose beginnen het proces van gluconeogenese en afbraak van vet en eiwitten om hun metabolisme te herstellen. Als gevolg hiervan nemen de oxalacetaatconcentraties af en verhogen ze de oxidatie van lipiden.
Een acetyl-CoA-accumulatie treedt op, die in afwezigheid van oxalacetaat het pad van citroenzuur niet kan volgen en vervolgens de hoge producties van de ketonlichamen veroorzaakt, kenmerkend voor deze ziekte.
De accumulatie van aceton wordt gedetecteerd door zijn aanwezigheid in de urine en in de adem van mensen die deze aandoening presenteren, en is in feite een van de symptomen die wijzen op de manifestatie van deze ziekte.
Referenties
- Blázquez Ortiz, C. (2004). Ketogenese in astrocyten: karakterisering, regulatie en mogelijk cytoprotectief papier (Proefschrift doctoraat, Complutense University of Madrid, Publications Service).
- Devlin, T. M. (1992). Textbook of Biochemistry: met klinische correlaties.
- Garrett, r. H., & Grisham, c. M. (2008). Biochemie. Thomson Brooks/Cole.
- McGry, J. D., Mannaerts, g. P., & Foster, D. W. (1977). Een mogelijke rol voor malonyl-CoA bij de regulatie van hepatische vetzuuroxidatie en ketogenese. The Journal of Clinical Investigation, 60(1), 265-270.
- Melo, v., Ruiz, v. M., & Cuamatzi, of. (2007). Biochemie van metabolische processen. Galm.
- Nelson, D. L., Lehninger, een. L., & Cox, m. M. (2008). Lehninger -principes van biochemie. Macmillan.
- Pertierra, a. G., Gutiérrez, c. V., & Anderen, c. M. (2000). Fundamentals of Metabolic Biochemistry. Redactionele Tébar.
- VOET, D., & Voet, J. G. (2006). Biochemie. ED. Pan -American Medical.
- « Continentaal ontbijt wat is en welk voedsel het omvat?
- Calciumperoxide (CaO2) eigenschappen, risico's en gebruik »

