Lithiumoxide
- 3575
- 83
- James Dach
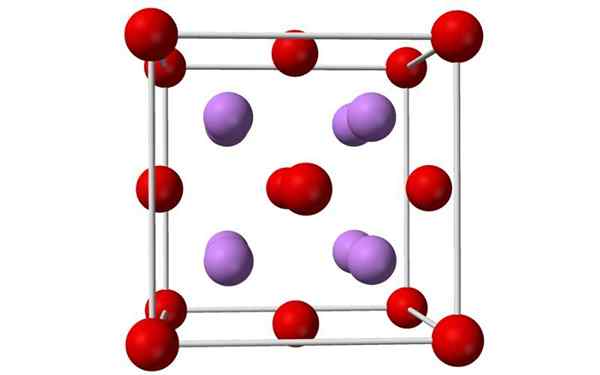
 Bollen en stavenmodel van een unitaire lithiumoxide -cel. Bron: Benjah-Bmm27, Wikimedia Commons
Bollen en stavenmodel van een unitaire lithiumoxide -cel. Bron: Benjah-Bmm27, Wikimedia Commons Wat is lithiumoxide?
Hij Lithiumoxide Het is een anorganische chemische verbinding van formule li2Of dat wordt gevormd samen met kleine hoeveelheden lithiumperoxide wanneer het lithiummetaal in de lucht wordt verbrand en combineert met zuurstof.
Tot de jaren 90 werd de metaal- en lithiummarkt gedomineerd door de Amerikaanse productie van minerale afzettingen, maar aan het begin van de 21ste eeuw was de meeste productie afgeleid van andere bronnen: Australië, Chili en Portugal waren de belangrijkste leveranciers ter wereld. Bolivia heeft de helft van de lithiumafzettingen ter wereld, maar het is geen geweldige producent.
De belangrijkste commerciële vorm is lithiumcarbonaat, li2CO3, Geproduceerd uit mineralen of Salmuelas door verschillende processen.
Wanneer lithium in de lucht brandt, is het hoofdproduct wit lithiumoxide -oxide, li2OF. Bovendien treedt er wat lithiumperoxide voor, li2OF2, Ook wit.
Het kan ook worden gedaan door de thermische ontleding van lithiumhydroxide, lioh of lithiumperoxide, li2OF2.
4li (s) + o2(g) → 2LI2Jij)
2lioH (s) + warmte → li2Of (s) + h₂o (g)
2LI2OF2(s) + warmte → 2LI2Of (s) + of2(G)
Fysische en chemische eigenschappen
- Lithiumoxide is een witte vaste stof die bekend staat als lithia, die aroma mist en zoute smaak heeft.
- Lithiumoxide zijn kristallen met antiflorietgeometrie, vergelijkbaar met natriumchloride (kubus gecentreerd op gezichten).
- Het molecuulgewicht is 29,88 g/mol, de dichtheid is 2,013 g/ml en de fusie- en kookpunten zijn respectievelijk 1438 ° C en 2066 ° C.
Het kan je van dienst zijn: Epid- De verbinding is zeer oplosbaar in water, alcohol, ether, pyridine en nitrobenzeen.
- Lithiumoxide reageert gemakkelijk met waterdamp om hydroxide en koolstofdioxide te vormen om carbonaat te vormen; Daarom moet het worden opgeslagen en beheerd in een schone en droge sfeer.
- Oxideverbindingen leiden geen elektriciteit. Bepaalde gestructureerde oxiden van Perovskita zijn echter elektronisch geleidend die toepassing vinden in de kathode van de vaste oxide -brandstofcel- en zuurstofgeneratiesystemen.
- Het zijn verbindingen die ten minste één zuurstofanion en een metalen kation bevatten.
Risico's
Lithiumoxide is een stabiele verbinding die onverenigbaar is met sterke zuren, water en koolstofdioxide. Voor zover we weten, zijn de chemische, fysische en toxicologische eigenschappen van lithiumoxide niet onderzocht en grondig gerapporteerd.
De toxiciteit van lithiumverbindingen is een functie van hun oplosbaarheid in water. Het lithiumion heeft toxiciteit in het centrale zenuwstelsel. De verbinding is zeer corrosief, irritant als het in contact komt met de ogen en de huid, wanneer het wordt ingeademd of ingenomen.
In geval van oogcontact moet u controleren of contactlenzen worden gebruikt en deze onmiddellijk verwijderen. Ze moeten minimaal 15 minuten worden gespoeld met stromend water, waardoor de oogleden open blijven. Koud water kan worden gebruikt, en geen oogzalf.
Als de chemische stof in contact komt met de kleding, behoudt deze dan zo snel mogelijk en beschermt het zijn eigen handen en lichaam. Plaats het slachtoffer onder een veiligheidsdouche.
Als de chemische stof zich ophoopt in de blootgestelde huid van het slachtoffer, zoals de handen, wordt de huid besmet met stromend water en niet -schaapszeep zacht gewassen en voorzichtig. Koud water kan worden gebruikt. Als irritatie aanhoudt, zoek dan medische aandacht. Was besmette kleding voordat u het opnieuw gebruikt.
Kan u van dienst zijn: Rankine Scale: wat is, conversies, voorbeeldenIn het geval van inhalatie moet het slachtoffer in een goed geventileerd gebied worden toegestaan. Als de inademing ernstig is, moet het slachtoffer zo snel mogelijk naar een veilig gebied worden geëvacueerd.
Draai strakke kleding los, zoals shirthals, riemen of stropdas. Als het slachtoffer moeilijk te ademen is, moet zuurstof worden toegediend. Als het slachtoffer niet ademt, wordt een mondreanimatie van de mond gemaakt.
Altijd rekening houdend dat het gevaarlijk kan zijn voor de persoon die hulp biedt om mond aan mondreanimatie te geven wanneer het geïnhaleerde materiaal giftig, besmettelijk of corrosief is. In alle gevallen moet onmiddellijk medische hulp worden gevraagd.
Toepassingen
- Lithiumoxide wordt gebruikt als oprichter in keramische email en creëert blauw met koper en rozen met kobalt. Reageert met water en stoom, vormt lithiumhydroxide en moet van hen worden geïsoleerd.
- Lithiumoxide (li2O), met zijn hoge tritio -potentieel, is het een aantrekkelijke kandidaat voor het vaste teeltmateriaal van een DT -fusie -energieplant, vanwege de hoge dichtheid van lithiumatomen (vergeleken met ander lithium- of metallisch lithiumceramiek) en de relatief hoge thermische geleidbaarheid.
Li2O Het zal worden blootgesteld aan hoge temperaturen onder neutronenbestraling tijdens de werking van fusiedekens. In deze omstandigheden zal een groot aantal bestralingsdefecten worden geproduceerd in LI2Of, zoals door helium geïnduceerde zwelling, relatief hoge thermische expansie, korrelgroei, LYH (T) -vorming en neerslag bij lage temperaturen en transport van LIOH (T) -massa bij hoge temperaturen.
Bovendien, de li2Of zal worden onderworpen aan spanningen die voortkomen uit thermische expansieverschillen tussen LI2O en structurele materialen. Deze kenmerken van Li2Of leiden tot uitdagende technische problemen, zowel in de productie als in het Manta -ontwerp.
Kan u van dienst zijn: strontiumhydride (srh2)- Een mogelijk nieuw gebruik is als een vervanging voor kobalt en lithiumoxide, zoals kathode in lithium -ionbatterijen die worden gebruikt om elektronische mobiele telefoonapparaten te stimuleren naar laptops, evenals auto's met batterijen.
Referenties
- Amerikaanse elementen. Lithiumoxide. Hersteld van Amerikaan Amerikaan.com.
- Lithiumoxide. Hersteld uit espimetals espimetals.com.
- Lithiumoxide (li2o). FERP is hersteld.UCSD.Edu ferp.UCSD.Edu.

