IJzersulfaat (FESO4) Wat is, structuur, eigenschappen, synthese
- 4117
- 467
- James Dach
Wat is ijzersulfaat?
Hij IJzersulfaat Het is een anorganisch zout waarvan de chemische formule feso is4. Het bestaat uit een kristallijne vaste stof van een variabele kleur, industrieel verkregen als een secundair product van staalverwerking.
Het wordt in de natuur in verschillende vormen gevonden, het meest voorkomende zijn heptohydrated ferro sulfaat, feso4· 7h2O ("Vitriolo Verde", aanwezig bij het Melenteritite Mineral). Dit hydraat wordt gemakkelijk onderscheiden door de blauwe groene kleur van zijn kristallen. Andere hydraten zijn over het algemeen FESO4· XH2Of, waar x varieert van 1 tot 7.
Heptahydraat ferro sulfaat verliest watermoleculen als gevolg van verwarming en kan worden omgezet in andere vormen van ijzerstoffensulfaat; Dus wanneer 57 ºC wordt verwarmd, verliest het drie watermoleculen en transformeert het in ferro tetrahydraatsulfaat. Hoeveel in totaal kunt u verliezen? Zeven watermoleculen, dat wil zeggen teveel water.
Ferrous sulfaat wordt gebruikt bij de behandeling en preventie van bloedarmoede door ijzertekort. Het kan echter toxische effecten hebben, dus u moet voorzichtig zijn in uw dosering.
IJzersulfaatstructuur
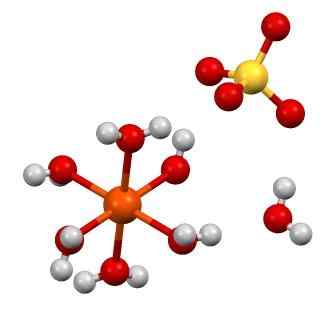
 Structuur van FESO4 · 7H2O. Bron: Smokefoot [CC BY-SA 4.0 (https: // creativeCommons.Org/licenties/by-sa/4.0)]
Structuur van FESO4 · 7H2O. Bron: Smokefoot [CC BY-SA 4.0 (https: // creativeCommons.Org/licenties/by-sa/4.0)] Feso's chemische formule4 Het benadrukt dat dit zout uit geloofsionen bestaat2+ En dus42- In een 1: 1 verhouding. Beide ionen interageren door elektrostatische krachten zodanig dat ze worden geordend in een ortorrombisch kristallijn systeem; die logischerwijs overeenkomt met watervrijzout.
In het bovenste beeld daarentegen wordt de structuur van de FESO getoond4· 7h2OF. De oranje bol vertegenwoordigt het geloofskation2+, Wat wordt gewaardeerd, coördinaten met zes watermoleculen om een octaëder te vormen. De last van geloof2+ trekt anion zo aan42-, En dit op zijn beurt, indien waargenomen, vormt een waterstofbrug met het zevende watermolecuul.
Het zevende watermolecuul (degene die ver van de octaëder is), vormt ook een andere waterstofbrug met een ander watermolecuul dat tot een naburige octaëder behoort. Het resultaat van deze interacties is dat het glas van ortorrombisch naar monoklinisch gaat.
Als de FESO -kristallen4 watervrij hydrateren, de anionen zo42- rond geloof2+ Ze worden vervangen door H -moleculen2OF. Deze substituties verstoren de elektronen D van ijzer, waardoor ze worden gedwongen te reizen op verschillende niveaus van energieën; die verantwoordelijk zijn voor het kleuren van veranderingen tussen wit, blauwachtig groen.
Kan u van dienst zijn: natriumsulfiet (Na2SO3)Fysische en chemische eigenschappen
Namen
Ferrous sulfaat of ijzersulfaat (II)
Moleculaire formule
-Ferrroso anhydro sulfaat (feso4))
-Heptahydraat ferrous sulfaat (feso4.7h2OF)
Molecuulgewicht
Varieert met de mate van sulfaathydratatie. Hepthydraatijzersulfaat heeft bijvoorbeeld een molecuulgewicht van 278,02 g/mol; Terwijl de anhydro een molecuulgewicht heeft van 151,91 g/mol.
Fysiek uiterlijk
Het varieert ook met de mate van hydratatie. De watervrijvorm presenteert bijvoorbeeld ortorrombische witte kristallen; Terwijl ze in de Heptahidra-vorm zijn, zijn de kristallen blauwgroene monoklinica.
Geur
Toilet
Dikte
Ashidro ferrous sulfaat is de meest dichte zoutvorm (3,65 g/cm3)). De heptahydraatvorm is daarentegen het minst dicht (1.895 g/cm3)).
Smeltpunt
Evenzo varieert dit afhankelijk van de mate van hydratatie. De anhydra -vorm heeft een fusiepunt van 680 ºC (1.856 ºF, 973 K) en de heptahydraatvorm, 60-64 ºC (140-147 ºF, 333-337 K).
Oplosbaarheid in water
-Monohydrata -vorm: 44,69 g/100 ml water (77 ºC)
-Heptahydraatvorm 51,35 g/100 ml water (54 ºC).
Alcoholoplosbaarheid
Onoplosbaar.
Dampdruk
1,95 kPa (heptahydraatvorm)
Brekingsindex
1.591 (monohydrata) en 1.471 (heptahidrata).
Stabiliteit
In de lucht kan het snel oxideren en bedekt met een geelbruine kleur, die de aanwezigheid van het geloofskation aangeeft3+. De oxidatiesnelheid wordt verhoogd door de toevoeging van alkali of door blootstelling aan licht.
Ontleding
Wanneer verwarmd tot ontleding zendt giftig zwaveldioxide en zwaveltrioxide uit, waardoor een roodachtig ijzeroxide als residu achterblijft.
Reacties
Het is een reductiemiddel dat op salpeterzuur werkt door het te reduceren tot stikstofmonoxide. Evenzo vermindert het chloor tot chloride, en de toxische foroxische vormen die aanwezig zijn in cement tot chroom (III), van minder toxiciteit.
Synthese
Van staalwol
Ferrous sulfaat wordt geproduceerd door staal (geloof) te reageren met zwavelzuur. In de beschreven methode wordt de volgende procedure gevolgd: het staal wordt gebruikt in de vorm van staalwol, die voorheen ellendig is met aceton.
Kan u van dienst zijn: ferro chloride (FECL2): structuur, gebruik, eigenschappenVervolgens wordt staalwol in een glazen beker geplaatst en is volledig bedekt met 30-40 %zwavelzuur, waardoor zure digestie enkele uren kan optreden; Totdat de staalwol verdwijnt. Meer staalwol kan worden toegevoegd en de procedure meerdere keren herhaald.
Groene kristallen die mogelijk zijn gevormd, worden opnieuw opgelegd met behulp van waterwater 1-2 met zwavelzuur. Deze oplossing wordt gefilterd op filterpapier en de pH wordt aangepast door natriumcarbonaat toe te voegen. De oplossing wordt opgeslagen, om contact met zuurstof te voorkomen en dus de oxidatie van het geloof nadeel2+ tot geloof3+
Vervolgens is de filtering onderhevig aan verdamping bij een temperatuur tussen 80-90 ºC. De procedure wordt uitgevoerd in Pietri -capsules die op een verwarmingsplaat worden geplaatst. Vervolgens worden de gevormde groene kristallen verzameld, die naar een droogator kunnen worden gebracht om hun uitdroging te voltooien.
Van het pyriet
Ferrous sulfaat voor oxidatie van het pyriet wordt ook geproduceerd (FES2)).
2 FES2 + 7 o2 + 2 H2O => 2 feso4 + 2 H2SW4
Risico's
De inademing van de FESO4 veroorzaakt neusirritatie, keel en longen. Als u fysiek contact hebt met dit zout, kunt u irritatie van huid en ogen veroorzaken; Bovendien kan langdurig contact met deze laatste een bruinachtige plek en oogschade veroorzaken.
Herhaalde inname kan misselijkheid, braken, maagpijn, constipatie en onregelmatige darmbewegingen veroorzaken.
Onder de tekenen van ferro sulfaatvergiftiging zijn de volgende: zwarte of bloedige ontlasting; blauwachtige huid en nagels; Veranderingen in het volume uitgescheiden urine; flauwvallen; orale droge of ogen; borstpijn; eten; Ademhalingsproblemen.
Bovendien kunnen snelle en onregelmatige beats optreden, toeneemt in dorst en honger, ongebruikelijke paless en ademhalingsverkorting.
Coagulatieverandering is een indicatie van vergiftiging met ferro sulfaat, waarbij een uitbreiding in trombine, uitsteeksel en tijd van tromboplastine wordt waargenomen.
Studies naar het effect van ferro sulfaat op geïsoleerde spieren van het hart van konijnen, stelden ons in staat te observeren dat het een vermindering van de maximale spanning veroorzaakte die werd ontwikkeld door de bestudeerde hartspieren, evenals de maximale snelheid van spanningsontwikkeling.
Het kan u van dienst zijn: relatie tussen chemie en technologie met mens, gezondheid en milieuToepassingen
In de landbouw
-Het wordt gebruikt als een pesticide om de snuifje tarwe en de ontleding van fruitbomen te regelen.
-Het wordt gebruikt bij de behandeling van chlorose, een ziekte die wordt gekenmerkt door de geelachtige kleur van de bladeren, veroorzaakt door de alkaliteit van de bodem.
-Ferrous sulfaat regelt alkaliteit, waardoor de pH van de bodem wordt verminderd.
- Elimineert mos en staat het gazon uit.
Als reagens en in de industrie
Binnen het gebruik van de FESO4 Als reagens en in de industrie zijn de volgende:
-Analytisch reagens
-Ruwe stof om ferriet en magnetisch ijzeroxide te verkrijgen
-Ingrediënt voor de uitwerking van het anorganische blauwe pigment
-Salpeterzuurreactief, chloor en chroom
-Bij de productie van andere sulfaten
-Het wordt gebruikt in galvanoplastiekbaden met ijzer
-Houten
-In aluminium etsen
-Kwalitatieve nitraatanalyse (bruine gele test door geloof oxidatie2+))
-Polymerisatiekatalysator
-Het wordt gebruikt als een voorloper van de synthese van andere ijzers
-Het wordt industrieel gebruikt als een kleurstoffixeermiddel
-In de vervaardiging van ijzeren kleurstof
-Mordant in wolvlekken
-Om zilveren kleur te geven aan arce hout
-IJzer katalysator in de reactie van Fenton
In de geneeskunde en voor het verrijking van voedsel
Het wordt gebruikt bij de behandeling van bloedarmoede door ijzertekort, met behulp van een dosis van 150-300 mg ferreus sulfaat, drie keer per dag, wat een waarneembare toename van de hemoglobineconcentratie produceert in een week van behandeling.
Het gebruik ervan bij zwangere vrouwen als een aanvulling op hun dieet is ook aanbevolen. Ferrous sulfaat is gebruikt als samentrekkend in de genezing van veewonden.
Anderen
Het wordt gebruikt bij de behandeling van afvalwater door flocculatie en ook voor de eliminatie van fosfaat uit deze wateren. Ferrous hepthydraatsulfaat wordt gebruikt bij de identificatie van schimmelsypen.
Referenties
- Labbereiding van ferro sulfaat. Hersteld van: crscientific.com
- Ferrous sulfaat hepthydraat. Hersteld van: pubchem.NCBI.NLM.NIH.Gov
- « Directionele selectie Wat is, definitie, voorbeelden
- De 4 renners van de apocalyps en de betekenis ervan »

