Chiraliteit
- 1864
- 481
- Ernesto McKenzie
 De chiraliteit wordt geassocieerd met asymmetrie en gebeurt wanneer een element niet kan worden gesuperponeerd in een spiegel in een spiegel. Bron: Gabriel Bolívar
De chiraliteit wordt geassocieerd met asymmetrie en gebeurt wanneer een element niet kan worden gesuperponeerd in een spiegel in een spiegel. Bron: Gabriel Bolívar Wat is chiraliteit?
De chiraliteit Het is een geometrische eigenschap waarin een object twee afbeeldingen kan hebben: één rechts en één links, die niet uitwisselbaar zijn. Dat wil zeggen, ze zijn ruimtelijk verschillend, hoewel de rest van hun eigenschappen identiek zijn. Een object dat chiraliteit vertoont, wordt eenvoudig gezegd dat het 'chiral' is.
De rechter- en linkerhand zijn chiralen: de ene is de reflectie (spiegelende afbeelding) van de andere, maar ze zijn niet hetzelfde, omdat wanneer ze bovenop de andere worden geplaatst, ze niet overeenkomen met hun duimen.
Meer dan een spiegel, om te weten of een object chiraal is, moet de volgende vraag worden gesteld: heb je "versies" zowel voor de linkerkant als de rechterkant?
Bijvoorbeeld, een doppit voor links -gehanded en een andere voor rechts -zijn chirale objecten. Twee voertuigen van hetzelfde model, maar met het stuur aan de linkerkant of rechts, een paar schoenen, net als de voeten. Slaktrappen in de linkerrichting, en in de goede richting, enz.
En in de chemie zijn de moleculen geen uitzondering: ze kunnen ook chirals zijn. In het bovenste beeld wordt een paar moleculen met tetraëdrische geometrie getoond.
Hoewel links is gedraaid en de bollen van blauw en paars, kijken de bruine en groene kleur "uit het vliegtuig" uit het vliegtuig.
Hoe u moleculaire chiraliteit kunt bepalen?
Met de moleculen is het niet zo eenvoudig om te definiëren, wat de linker- of rechter "-versie" is die er gewoon naar kijkt.
Hiervoor nemen organische chemicaliën hun toevlucht tot de configuraties (r) of (s) van cahn-ingold-prelog, of zijn gebaseerd op de optische eigenschap van deze chirale stoffen om het gepolariseerde licht te roteren (wat ook een chirale element is).
Het kan u van dienst zijn: Lithium: geschiedenis, structuur, eigenschappen, risico's en gebruikHet is echter niet moeilijk om te bepalen of een molecuul of verbinding het chirale is, alleen door de structuur te observeren. Wat opvallende bijzonderheid heeft het koppel van het bovenste beeld?
Het heeft vier verschillende substituenten, elk met zijn eigen karakteristieke kleur, en ook de geometrie rond het centrale atoom is tetraëdral.
Als er een atoom is met vier verschillende substituenten in een structuur, kan (in de meeste gevallen) worden bevestigd dat het molecuul chiraal is.
Dan wordt gezegd dat er in de structuur een centrum van chiraliteit is of Stereogeen centrum. Waar er een is, zullen er een paar stereoisomeren bekend zijn enantiomeren.
De twee moleculen van het beeld zijn enantiomeren. Hoe groter het aantal chirale centra dat een verbinding bezit, hoe groter zijn ruimtelijke diversiteit.
Het centrale atoom is meestal een koolstofatoom in alle biomoleculen en verbindingen met farmacologische activiteit. Het kan echter ook een fosfor, stikstof of metaal zijn.
Voorbeelden van chiraliteit
Het chirale centrum is misschien een van de belangrijkste elementen bij het bepalen of een verbinding chiraal is of niet.
Er zijn echter andere factoren die onopgemerkt kunnen blijven, maar die in 3D -modellen een spiegelbeeld vertoont dat niet kan worden gesuperponeerd.
Voor deze structuren wordt gezegd dat ze in plaats van het centrum andere elementen van chiraliteit hebben.
Met dit in gedachten is de aanwezigheid van een asymmetrisch centrum met vier substituenten niet langer genoeg, maar ook de rest van de structuur moet zorgvuldig worden geanalyseerd en dus in staat zijn om een stereoisomeer van een andere te onderscheiden.
Het kan u van dienst zijn: zinkhydroxide (Zn (OH) 2)Axiaal
 Structuren van een aleno en een bifenylverbinding. Bron: Wikimedia Commons
Structuren van een aleno en een bifenylverbinding. Bron: Wikimedia Commons In de bovenste beeld worden verbindingen getoond die misschien plat lijken voor het blote oog, maar dat zijn ze echt niet.
Links heb je de algemene structuur van een aleno, waarbij r de vier verschillende substituenten aangeeft. En rechts, de algemene structuur van een bifenylverbinding.
Het einde waar r wordt gevonden3 en r4 Het kan worden gevisualiseerd als een "vin" loodrecht op het vlak waar ze liegen1 en r2.
Als een waarnemer dergelijke moleculen analyseert die het oog positioneren voor de eerste koolstof die is gekoppeld aan R1 en r2 (Voor de Aleno), zul je R zien1 en r2 aan de linker- en rechterkant, en naar r4 en r3 omhoog en omlaag.
Ja r3 en r4 Ze blijven vast, maar r1 Aan de rechterkant, en r2 Links zal een andere "ruimteversie" dan zijn.
Dit is waar de waarnemer kan concluderen dat hij een as van chiraliteit voor de Aleno heeft gevonden. Hetzelfde geldt voor bifenyl, maar met de aromatische ringen die bij de visie betrokken zijn.
Ringen of heliciteitsschroeven
 As van chiraliteit in heptheliicenos. Bron: Wikimedia Commons
As van chiraliteit in heptheliicenos. Bron: Wikimedia Commons Merk op dat in het vorige voorbeeld de as van de chiraliteit in het skelet c = c = c lag, voor de aleno en in de AR-AR-link, voor de bifenyl.
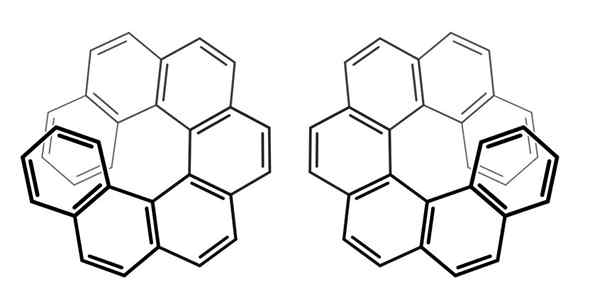
Voor verbindingen hierboven, hepthehelicenos genoemd (voor het hebben van zeven ringen), is de chiraliteitsas de z -as, de propeller.
Daarom moet u deze moleculen van bovenaf zien om van de ene enantimer van een andere te onderscheiden.
Op deze manier kan worden gedetailleerd dat een hepptheliicen draait in de richting van de kloknaalden (linkerkant van het beeld), of in een antihorariumrichting (rechterkant van het beeld).
Kan u dienen: natriumhydroxide (NaOH): structuur, eigenschappen, gebruik, synthesePlan
Stel dat er niet langer een helicenus is, maar een molecuul met niet -coplanaire ringen, dat wil zeggen, de ene is boven of onder de andere (of niet in hetzelfde vlak).
Hier rust het chirale karakter niet zo veel in de ring, maar in zijn substituenten, omdat het deze zijn die elk van de twee enantiomeren definiëren.
 Vlakke chiraliteit. Bron: Wikimedia Commons
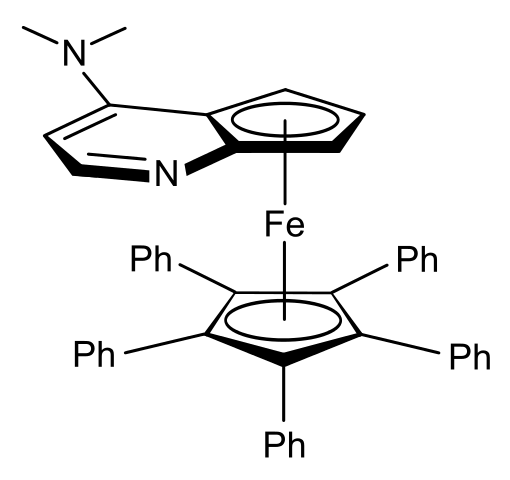
Vlakke chiraliteit. Bron: Wikimedia Commons Bijvoorbeeld, in de ferroen van het bovenste beeld heb je de ringen die het 'insluiten' het atoom van geloof niet veranderen, maar de ruimtelijke oriëntatie van de ring met het stikstofatoom en de groep -n (cho (kies3))2.
In de afbeelding, de groep -n (cho3))2 wijst naar links, maar in zijn enantiómero zal het naar rechts wijzen.
Anderen
Voor macromoleculen of die met unieke structuren begint het panorama te vereenvoudigen. Dit komt omdat je uit de 3D -modellen de vlucht van een vogel kunt zien als ze chirals zijn of niet, zoals bij de objecten van de eerste voorbeelden.
Een koolstofnanobuis kan bijvoorbeeld wendingen naar links laten zien, en daarom is het chiraal als er een identieke is, maar met beurten naar rechts.
Hetzelfde geldt voor andere structuren waar, ondanks dat ze geen centra van chiraliteit hebben, de ruimtelijke opstelling van al zijn atomen chirale vormen kan aannemen.
Er wordt dan gesproken over een inherente chiraliteit, die niet afhankelijk is van een atoom maar van de hele set.
Een chemisch krachtige vorm van het onderscheiden van het "linker beeld" van die rechts, is door een stereoselectieve reactie, dat wil zeggen waar het alleen met een enantiomeer kan passeren, terwijl met de andere niet.
Referenties
- Chiraliteit (chemie). Opgehaald van.Wikipedia.borg
- Chirraliteit. Hersteld uit chemie -uitexplaed.com

