Subatomische deeltjes
- 770
- 42
- Ernesto McKenzie
 Belangrijkste subatomaire deeltjes
Belangrijkste subatomaire deeltjes Wat zijn subatomaire deeltjes?
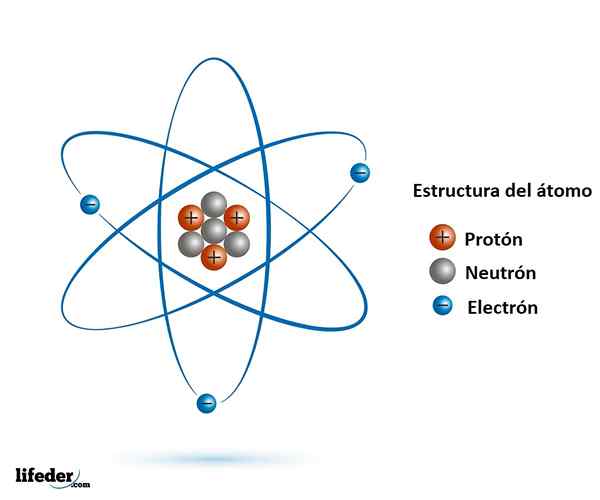
De Subatomische deeltjes Ze zijn kleiner dan het atoom en worden in de natuur gevonden, er zijn er bijna allemaal deel van uit. We kennen de belangrijkste en meest stabiele, die het elektron, het proton en het neutron zijn.
Alle materie bestaat uit deze deeltjes, hoewel er anderen zijn, hoewel het bestaan lang het bestaan is genegeerd. De eerste atoommodellen, die van enkele eeuwen vóór Christus dateren, gingen ervan uit dat atomen ondeelbaar waren, zoiets als knikkers die op een bepaalde manier aanleiding gaven tot de verschillende elementen.
Toen werd geleerd dat het niet zo was, dankzij de ontdekkingen van het elektron in de 19e eeuw en de atomaire kern aan het begin van de 20e eeuw, vroegen wetenschappers zich af of deze deeltjes een interne structuur hadden.
Het bleek dat zowel het proton als het neutron deeltjes zijn die bestaan uit nog kleinere, die geen interne structuur hebben: het zijn de elementaire deeltjes.
Daarom zijn subatomaire deeltjes verdeeld in:
- Samengestelde deeltjes.
- Elementaire deeltjes.
Elementaire deeltjes zijn Quarks, Gluons en Leptones. Quarks en Gluons vormen protonen en neutronen, terwijl het elektron, een elementair deeltje, een lepton is.
Ontdekking van subatomaire deeltjes
De ontdekkingen van de subatomaire deeltjes begonnen vanaf de negentiende eeuw en de eerste die werd gevonden was het elektron.
Tegen 1890 waren natuurkundigen erg druk bezig met het bestuderen van straling en overdracht van elektromagnetische golven. J. J. Thomson was een van hen en voerde talloze experimenten uit met een buis waarnaar de lucht was geëxtraheerd en op een paar elektroden geplaatst.
 J. J. Thomson
J. J. Thomson Toen een spanning werd toegepast, werden mysterieuze stralen geproduceerd, kathodestralen genoemd, wiens aard onbekend was, tot J. J. Thomson (1856-1940) ontdekte dat ze bestonden uit negatief geladen deeltjes.
Thomson verkreeg het quotiënt tussen de belasting en massa van deze deeltjes: 1.76 x 108 C/g, waar C betekent Coulomb, De eenheid voor elektrische lading in het internationale systeem van eenheden en G is gram.
Kan u van dienst zijn: Lichtbreking: elementen, wetten en experimentEn hij vond twee zeer belangrijke dingen, de eerste dat de massa van de deeltjes extreem klein was, en ten tweede dat deze waarde voor alle allemaal hetzelfde was, ongeacht wat de elektroden werden gemaakt.
De waarde van de lading werd kort daarna gevonden, aan het begin van de jaren 1900, door de Amerikaanse natuurkundige Robert Millikan (1868-1953) en zijn medewerkers, dankzij het experiment van de oliedruppel.
De atoomkern: protonen en neutronen
 Henri Becquerel Portret
Henri Becquerel Portret Aan het einde van de 19e eeuw had Henri Becquerel (1852-1908) het fenomeen van natuurlijke radioactiviteit ontdekt, die andere natuurkundigen intrigeerde, zoals de echtgenoten Marie en Pierre Curie, evenals de neozygous Ernest Rutherford.
De laatste vond drie verschillende soorten straling uit uraniummonsters, een goed bekend radioactief element. Hij noemde ze met de eerste drie letters van het Griekse alfabet: α, β en γ.
Rutherford dispersie -experimenten
 De jonge Ernest Rutherford
De jonge Ernest Rutherford Met behulp van de α -deeltjes, zeer energieke en positief geladen, Rutherford Bombard.
Maar merkwaardig genoeg werd een kleine fractie deeltjes omgeleid en een paar stuiterden zelfs in de tegenovergestelde richting. De laatste was onvoorstelbaar, want zoals Rutherford zei, was het alsof je met een geweer een dunne zakdoek schoot en zag dat de kogels terugkeren.
De reden dat de α -deeltjes afwijken is dat er binnen het blad iets is dat ze afstoot en daarom positief moet worden geladen. Dit is de atomaire kern, klein van grootte, maar dat bevat bijna de hele massa van de atoom.
De ontdekking van neutron
 James Chadwick
James Chadwick Het neutron duurde iets langer om te worden gevonden en was te wijten aan de Engelse natuurkundige James Chadwick (1891-1974), Rutherford Student. Rutherford zelf had het bestaan van een deeltje zonder belasting in de kern voorgesteld om uit te leggen waarom dit niet uiteenvaart vanwege elektrostatische afstoting.
Chadwick -experimenten onthulden in 1932 het bestaan van een massa massa zeer vergelijkbaar met die van het proton, maar zonder load. Daarom noemden ze haar neutron en naast het proton zijn ze de essentiële componenten van de atoomkern.
Kan u van dienst zijn: elektromagnetische energie: formule, vergelijkingen, gebruik, voorbeeldenDe belangrijkste subatomaire deeltjes
Over het algemeen worden subatomaire deeltjes gekenmerkt door te hebben:
- Massa.
- Elektrische lading.
- Spinnen.
De spin is een kwaliteit analoog aan rotatie op de as, maar van een volledig kwantumkarakter. En aan de andere kant zijn er deeltjes met belasting en massa 0, zoals foton.
Elektron
Het elektron is een stabiel subatomair deeltje, negatief geladen en behorend tot de Leptones -groep, die het is met de laagste massa. Het is een essentieel onderdeel van het atoom, maar het kan hieruit geïsoleerd bestaan in de vorm van Gratis elektronen.
In feite is het de kleinste elektrische lading die in de natuur kan worden gevonden, dus elk ander is het veelvoud van het elektron, volgens het kwantificeringsprincipe van de belasting.
De belangrijkste kenmerken zijn:
- Massa: 9.1 x 10-31 kg
- Laad: E = -1.6 x 10-19 C
- Spin: ± ½
- Antiparticle: positron.
Het elektron is verantwoordelijk voor de vorming van chemische bindingen, evenals in elektrische en thermische geleiding. En dankzij de kwantummechanica weten we dat het elektron een dubbel gedrag heeft: golf en deeltjes tegelijkertijd.
Proton
Het is een elektrisch geladen deeltje, waarvan de belasting in grootte hetzelfde is als dat van het elektron, maar van het tegenovergestelde teken.
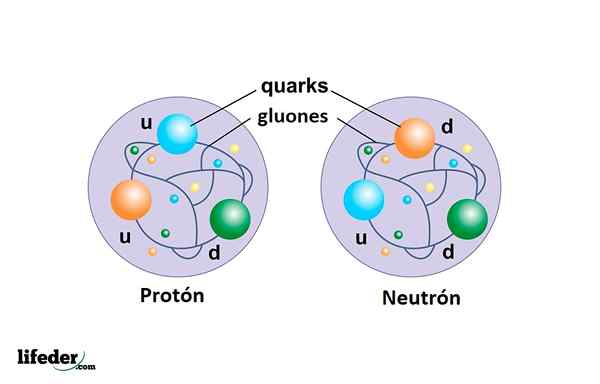
Het proton is geen elementair deeltje zoals het elektron, maar bestaat uit drie quarks verenigd door Gluonen En het is veel massiever dan het elektron.
Anders dan dit is het proton beperkt tot de atoomkern, en de hoeveelheid bepaalt welk element het is, evenals zijn eigenschappen.
- Massa: 1.672 x 10-27 kg
- Laad: E = +1.6 x 10-19 C
- Spin: ½
- Antiparticle: antiproton.
Neutron
Het neutron naast het proton vormt de atoomkern en bestaat ook uit drie quarks: twee van het type Omlaag en een van het type OMHOOG.
- Massa: 1.675 x 10-27 kg
- Geen netto belasting.
- Spin: ½.
Het is een stabiel deeltje in de atoomkern, maar als een vrij deeltje daalt het met een halfwaardetijd van ongeveer 10.Ongeveer 3 minuten. De massa ervan is nauwelijks groter dan die van het proton en zoals we hebben gezegd, ontbreekt het netto -lading.
Kan u van dienst zijn: latente hitteHet aantal neutronen van een atoom is belangrijk, want hoewel het niet de aard van het element bepaalt, zoals het proton doet, bepaalt het de isotoopklasse.
De isotopen van een element zijn varianten van hetzelfde en hun gedrag kan heel anders van elkaar verschillen. Er zijn stabiel en onstabiel, bijvoorbeeld waterstof heeft als isotopen het deuterium en tritium.
Het bombarderen van neutronenatomen van bepaalde uranium- en plutoniumverbindingen, de kern is bont. De nucleaire kettingreactie die optreedt, kan een grote hoeveelheid energie uitzenden.
Karks

Het zijn de bestanddelen van protonen en neutronen. Tot nu toe zijn er 6 soorten quarks gevonden, maar geen enkele als een vrij deeltje, maar geassocieerd om andere composietdeeltjes te vormen.
Het bewijs van het bestaan ervan werd verkregen door experimenten die sinds de jaren 60 werden uitgevoerd, met de Stanford Linear Accelerator en vervolgens in CERN.
- Laad: +2/3e, -1/3e
- Spin: ½
- Antiparticle: antiquark.
Andere deeltjes
Vanaf 1930 volgden de ontdekkingen van nieuwe deeltjes, velen voorspeld door de theorie. Het standaarddeeltjesmodel beschouwt het bestaan van 17 soorten fundamentele deeltjes, tussen quarks, leptones, bosonen en het boson van Higgs.
Ze hebben ook hun respectieve antipartikelen, die bij het interactie worden vernietigd en nieuwe deeltjes genereren. Hier zijn er een aantal:
-Positron, identiek aan het elektron maar met positieve belasting.
-Neutrino, zonder belasting.
-meson.
-Bosones, die de dragers zijn van de fundamentele interacties, behalve de zwaartekracht.
-Het boson van Higgs, verantwoordelijk voor de massa.
-Gravitón, is een voorgesteld deeltje om de zwaartekracht te verklaren, maar er is nog steeds geen bewijs dat er is.
Referenties
- Chang, R. 2013. Scheikunde. 11VA. Editie. Mc Graw Hill Education.
- Cobian, J. Het standaard deeltjesmodel. Hersteld van: SNE.is.
- Fernández de sala, p. Elementaire deeltjes, samengestelde deeltjes en virtuele deeltjes. Hersteld van: ific.UV.is.
- Giambattista, een. 2010. Natuurkunde. 2e. ED. McGraw Hill.
- Olmo, m. Protonen en neutronen. Hersteld van: hyperfysica.Phy-Astr.GSU.Edu.

