Heisenberg Atomic Model
- 4982
- 983
- Glen Armstrong
Wat is het atoommodel van Heisenberg?
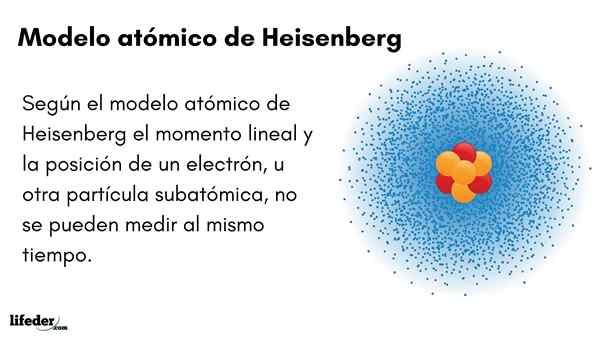
Hij Heisenberg Atomic Model (1927) introduceert het onzekerheidsprincipe in elektronenorbitalen rond de atoomkern. De uitstekende Duitse fysicus vestigde de basis van de kwantummechanica om het gedrag van subatomaire deeltjes die een atoom vormen te schatten.
Het onzekerheidsprincipe van Werner Heisenberg geeft aan dat het niet mogelijk is om met zekerheid de lineaire positie van een elektron tegelijkertijd te weten. Hetzelfde principe is van toepassing op tijd- en energievariabelen; Dat wil zeggen, als we een indicatie hebben over de positie van het elektron, zullen we het lineaire moment van het elektron negeren en vice versa.
Kortom, het is niet mogelijk om tegelijkertijd de waarde van beide variabelen te voorspellen. Het bovenstaande betekent niet dat een van de eerder genoemde magnitudes niet bekend kan zijn met precisie. Wanneer het afzonderlijk is, is er geen belemmering voor het verkrijgen van de waarde van rente.
Er vindt echter onzekerheid plaats als het gaat om tegelijkertijd twee geconjugeerde magnitudes te kennen, zoals het geval is met de lineaire positie en moment.
Dit principe ontstaat als gevolg van strikt theoretisch redeneren, als de enige haalbare verklaring om reden te geven over wetenschappelijke observaties.
Kenmerken van het Atomic -model van Heisenberg
 Werner Heisenberg
Werner Heisenberg In maart 1927 publiceerde Heisenberg zijn werk Over de perceptuele inhoud van cinematica en kwantummechanica, waar hij het principe van onzekerheid of onbepaaldheid beschreef.
Dit principe, fundamenteel in het door Heisenberg voorgestelde atoommodel, wordt gekenmerkt door het volgende:
- Het onzekerheidsprincipe ontstaat als een verklaring die een aanvulling vormt op de nieuwe atomaire theorieën over het gedrag van elektronen. Ondanks het gebruik van meetinstrumenten met een hoge precisie en gevoeligheid, is onbepaald nog steeds aanwezig in elke experimentele proef.
- Vanwege het onzekerheidsprincipe, bij het analyseren van twee gerelateerde variabelen, als u een nauwkeurige kennis van een van deze hebt, zal de onbepaaldheid over de waarde van de andere variabele toenemen.
- Het lineaire moment en de positie van een elektron, of een ander subatomair deeltje, kunnen niet tegelijkertijd worden gemeten.
- De relatie tussen beide variabelen wordt gegeven door een ongelijkheid. Volgens Heisenberg, het product van de variaties van het lineaire moment -3. 4 Jules x seconden) en 4π, zoals gedetailleerd in de volgende wiskundige uitdrukking:
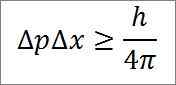
De legende die overeenkomt met deze uitdrukking is als volgt:
∆P: Bepaling van het lineair moment.
∆x: Bepaling van de positie.
H: Plank Constant.
π: PI 3.14 -nummer.
- Gezien het bovenstaande heeft het product van onzekerheden als lagere stop de relatie h/4π, wat een constante waarde is. Daarom, als een van de magnitudes nul neigt, moet de andere in dezelfde verhouding toenemen.
- Deze relatie is geldig voor alle paren van geconjugeerde canonieke magnitudes. Bijvoorbeeld: het onzekerheidsprincipe van Heisenberg is perfect van toepassing op het Energy-Time Duo, zoals hieronder gedetailleerd:
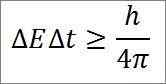
In deze uitdrukking:
∆E: Energie onbepaaldheid.
∆T: Bepaling van de tijd.
H: Plank Constant.
π: PI 3.14 -nummer.
- Uit dit model volgt het dat absoluut causaal determinisme in gecombineerde canonieke variabelen onmogelijk is, omdat om deze relatie tot stand te brengen, kennis van de initiële waarden van de onderzoeksvariabelen moet worden vastgesteld.
- Bijgevolg is het Heisenberg -model gebaseerd op probabilistische formuleringen, vanwege de willekeur die bestaat tussen de variabelen tot subatomaire niveaus.
Experimentele tests
Het onzekerheidsprincipe van Heisenberg ontstaat als de enige mogelijke verklaring voor de experimentele tests die plaatsvonden tijdens de eerste drie decennia van de 21ste eeuw.
Voordat Heisenberg het onzekerheidsprincipe heeft uitgesproken, suggereerden de voorschriften van kracht toen de lineaire momentumvariabelen, hoekmomentum, tijd, energie, onder andere, voor de subatomaire deeltjes die ze operationeel waren gedefinieerd.
Dit betekende dat ze werden behandeld alsof ze klassieke fysica waren; dat wil zeggen, een initiële waarde werd gemeten en de uiteindelijke waarde werd geschat volgens de vooraf ingestelde procedure.
Kan u van dienst zijn: vectorgrootteHet bovenstaande betekende het definiëren van een referentiesysteem voor metingen, het meetinstrument en de vorm van het gebruik van dit instrument, volgens de wetenschappelijke methode.
Volgens dit moesten de variabelen beschreven door subatomaire deeltjes zich deterministisch gedragen. Dat wil zeggen, zijn gedrag moet exact en precies worden voorspeld.
Telkens wanneer een essay van deze aard werd uitgevoerd, was het echter onmogelijk om in de meting de geschatte waarde theoretisch te verkrijgen.
De maatregelen werden verkeerd weergegeven vanwege de natuurlijke omstandigheden van het experiment, en het verkregen resultaat was niet nuttig om de atoomtheorie te verrijken.
Voorbeeld
Bijvoorbeeld: als het gaat om het meten van de snelheid en positie van een elektron, moet de assemblage van het experiment overwegen de botsing van een foton van licht met het elektron.
Deze botsing induceert een variatie in de intrinsieke snelheid en positie van het elektron, zodat het object van de meting wordt gewijzigd door experimentele omstandigheden.
Daarom moedigt de onderzoeker het optreden van een onvermijdelijke experimentele fout aan, ondanks de nauwkeurigheid en precisie van de gebruikte instrumenten.
Kwantummechanica anders dan klassieke mechanica
Naast het bovenstaande stelt het Heisenberg Onbeperkingsprincipe dat de kwantummechanica per definitie anders werkt met betrekking tot de klassieke mechanica.
Bijgevolg wordt aangenomen dat de precieze kennis van de subatomaire maatregelen wordt beperkt door de dunne lijn die de klassieke en kwantummechanica scheidt.
Heisenberg -modelbeperkingen
Ondanks het verklaren van de onbepaaldheid van subatomaire deeltjes en het zitten van de verschillen tussen klassieke en kwantummechanica, stelt het atoommodel van Heisenberg geen unieke vergelijking vast om de willekeur van dit type fenomenen te verklaren.
Kan u van dienst zijn: Gravitational Energy: formules, kenmerken, toepassingen, oefeningenBovendien impliceert het feit dat de relatie wordt vastgesteld door een ongelijkheid dat het bereik van mogelijkheden voor het product van twee geconjugeerde canonieke variabelen onbepaald is. Bijgevolg is de onzekerheid die inherent is aan subatomaire processen aanzienlijk.
Interessante artikelen
Schrödinger atomair model.
Broglie Atomic Model.
Chadwick Atomic Model.
Perrin Atomic Model.
Thomson Atomic Model.
Dalton Atomic Model.
Dirac Jordan Atomic Model.
Democritus Atomic Model.
Leucipo -atoommodel.
Bohr Atomic Model.
Sommend Atomic Model.
Huidig atoommodel.
Referenties
- Beyler, r. (1998). Werner Heisenberg. Encyclopædia Britannica, Inc. Hersteld van: Britannica.com
- Heisenberg's onzekerheidsprincipe (s.F.)). Hersteld van: Hiru.EUS
- Garcia, J. (2012). Heisenberg onzekerheidsprincipe. Hersteld van: Hiberus.com
- Atomische modellen (s.F.)). National Autonomous University of Mexico. Mexico Stad, Mexico. Hersteld van: advies.Cuautitlan2.UNAM.mx
- Werner Heisenberg (s.F.)).Opgehaald uit: The-History-off-the-Atom.Wikispaces.com
- Wikipedia, Free Encyclopedia (2018). Plankconstante. Hersteld van: is.Wikipedia.borg
- Wikipedia, Free Encyclopedia (2018). Heisenberg onbepaalde relatie. Hersteld van: is.Wikipedia.borg

