Joseph Thomson

- 4516
- 145
- Cecil Graham
 J.J. Thomson
J.J. Thomson Joseph John Thomson (1856-1940) Het was een Britse chemicus high. Hij won de Nobelprijs voor natuurkunde in 1906.
Hij werd geboren in Cheetam Hill, een district in Manchester, Engeland, op 18 december 1856. Ook bekend als "J.J."Thomson studeerde engineering aan Owens College, momenteel onderdeel van de Universiteit van Manchester, en vervolgens wiskunde in Cambridge.
In 1890, j.J. Thomson trouwde met Rose Elizabeth Paget, dochter van dokter Sir Edward George Paget, met wie ze twee kinderen had: een meisje, genaamd Joan Paget Thomson, en een kind, George Paget Thomson.
De laatste zou een beroemde wetenschapper worden en in 1937 een Nobelprijs voor natuurkunde verkrijgen voor hun werk met elektronen.
Van jonge leeftijd concentreerde Thomson zijn studies over de structuur van atomen, waardoor het bestaan van elektronen en isotopen werd ontdekt, naast vele andere bijdragen.
In 1906 ontving Thomson de Nobelprijs voor de natuurkunde, "als erkenning van de grote verdienste van zijn theoretische en experimenteel onderzoek naar de geleiding van elektriciteit door gassen", zoals vastgesteld door de jury in het vonnis van de bovengenoemde prijs.
In 1908 werd hij benoemd tot ridder door de Britse kroon en diende als eredoctoraat professor in de natuurkunde in Cambridge en het Royal Institute, Londen.
Hij stierf op 30 augustus 1940 op 83 -jarige leeftijd in de stad Cambridge, Engeland. De natuurkundige werd begraven in Westminster Abbey, in de buurt van het graf van Sir Isaac Newton.
Bijdragen van Joseph Thomson aan wetenschap en scheikunde
Elektronenontdekking
In 1897, j.J. Thomson ontdekte een nieuw lichtdeeltje dan waterstof, dat "elektron" werd gedoopt.
Het kan u van dienst zijn: Bepaling van Ashes: methoden en voorbeeldenWaterstof werd beschouwd als een eenheid voor het meet van atoomgewicht. Tot die tijd was het atoom de kleinste verdeling van materie.
In die zin was Thomson de eerste die de negatief geladen corpusculaire subatomaire deeltjes ontdekte.
Thomson Atomic Model
Het atoommodel van Thomson was de structuur die de Engelse fysicus toeschreef aan atomen. Voor de wetenschapper waren atomen een positieve ladingssfeer.
Er waren in die positieve belastingswolk gelijkmatig verdeeld elektronen, dat wil zeggen de positieve belasting van het atoomdeeg neutraliseren.
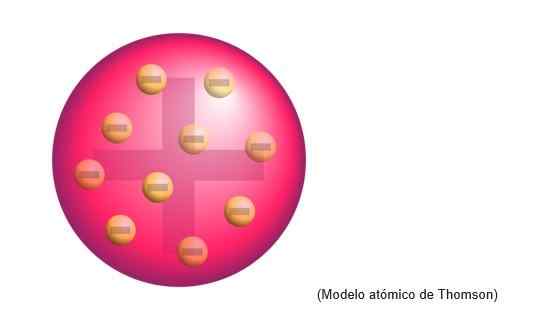
Dit nieuwe model vervangt de uitgewerkte door Dalton en zal later worden weerlegd door Rutherford, Thomson's Disciple in de Cavendish Laboratories van Cambridge.
Scheiding van atomen
Thomson gebruikte positieve of anodische stralen om atomen van verschillende massa te scheiden. Met deze methode kon hij de door elk atoom getransporteerde elektriciteit berekenen en het aantal moleculen per kubieke centimeter.
In staat om de atomen van verschillende massa en belasting te verdelen, ontdekte de fysicus het bestaan van isotopen. Ook op deze manier, met zijn studie van positieve stralen, produceerde hij een grote vooruitgang naar massaspectrometrie.
Ontdekking van isotopen
J.J. Thomson ontdekte dat neonionen verschillende massa's hadden, dat wil zeggen ander atoomgewicht. Dit is hoe Thomson aantoonde dat de neon twee subtypen van isotopen heeft, de neon-20 en de neon-22.
De isotopen, die tot vandaag zijn bestudeerd, zijn atomen van hetzelfde element, maar hun kernen hebben een ander massagummer, omdat ze zijn samengesteld uit verschillende hoeveelheden neutronen in hun centrum.
Experimenten met kathodestralen
Kathodestralen zijn elektronenstromen in vacuümbuizen, dat wil zeggen glazen buizen met twee elektroden, één positief en één negatief.
Kan u dienen: chroomhydroxide: structuur, eigenschappen, synthese, gebruikWanneer de negatieve elektrode wordt verwarmd, ook wel kathode genoemd, straalt deze straling uit die is gericht op de positieve elektrode of anode, in een rechte lijn als er geen magnetisch veld in die route optreedt.
Als de glazen wanden van de buis bedekt zijn met fluorescerend materiaal, produceert de staatsgreep van de kathoden tegen die laag de projectie van licht.
Thomson bestudeerde het gedrag van kathodestralen en kwam tot de conclusies dat de stralen zich rechtstreeks verspreiden.
Hij concludeerde ook dat deze stralen van hun traject konden worden afgeleid door de aanwezigheid van een magneet, dat wil zeggen van een magnetisch veld. Bovendien konden de stralen de messen verplaatsen met de sterkte van de circuleren van de elektronen, wat aantoont dat de elektronen massa hadden.
J.J. Thomson ervoer het gas in de kathodestraalbuis, maar het gedrag van elektronen varieerde niet. Evenzo verwarmden de kathodestralen de objecten die tussen de weg tussen elektroden tussenbeide kwamen.
Concluderend had Thomson aangetoond dat kathodestralen lichte, mechanische, chemische en thermische effecten hadden.
De kathodestraalbuizen en hun lichte eigenschappen waren transcendentaal voor de daaropvolgende uitvinding van Tube Television (CTR) en videocamera's.
Massaspectrometer
J.J. Thomson creëerde een eerste benadering van Massaspectrometer. Met deze tool kon de wetenschapper studeren.
Met dit onderzoek concludeerde hij dat de kathodestralen waren samengesteld uit negatieve lading corpuscles, die zich binnen de atomen bevinden, waardoor de deelbaarheid van het atoom wordt gepostuleerd en aanleiding gaf tot de elektronenfiguur.
Het kan u van dienst zijn: Bijnrinezuur: formule, eigenschappen, risico's en gebruikOok ging de vooruitgang in massaspectrometrie tot vandaag door, in verschillende methoden om de elektronen van atomen te scheiden.
Bovendien was Thomson de eerste die suggereerde De eerste golfgids in 1893. Dit experiment bestond uit verspreiding.
Golfgidsen zouden in de toekomst veel worden gebruikt, zelfs vandaag, met gegevensoverdracht en optische vezels.
Thomson's erfenis
De Thomson (TH) werd opgericht als een massa-lading-eenheid in massaspectrometrie, voorgesteld door Cooks en Rockwood Chemicals, ter ere van Thomson.
Deze techniek maakt het mogelijk om de verdeling van de moleculen van een substantie te bepalen volgens hun massa en, hiermee te erkennen, die aanwezig zijn in een steekproef van materie.
Thomson -formule (TH):
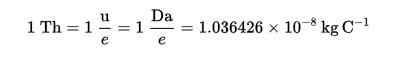
Uitstekende werken
- De discarge van elektriciteit door gassen, elektriciteit door gassen (1900).
- De corpusculaire theorie van materie, het elektron in chemie en herinneringen en reflecties (1907).
- Beyond the Electron (1928).
Referenties
- Nobelmedia AB (2014). J. Thomson - Biografisch. Nobelprijs.borg. Nobelprijs.borg.
- Thomson, Joseph J., Elektriciteit door gassengedrag. Cambridge, University Press, 1903.
- Menchaca Rocha, Arturo. De discrete charme van elementaire deeltjes.
- Christen, Hans Rudolf, Fundamentals of General and Anorganic Chemistry, Volume 1. Barcelona, Spanje. Edities keren s.NAAR., 1986.
- Arzani, Aurora Cortina, Elementaire algemene chemie. Mexico, Porrúa Editorial, 1967.
- R. G. Kookt, a. L. Rockwood. Snelle communicatie. Massaspectrom. 5, 93 (1991).

