Groeihormoon (somatotropine) structuur, functies
- 979
- 85
- Ernesto McKenzie
De Somatotropin (STH) U -groeihormoon (GH) is een relatief klein eiwit dat wordt geproduceerd op het niveau van adenohypophysis en betrokken bij ontwikkelingsprocessen, longitudinale groei van het organisme en bij de controle van verschillende metabolische processen.
Het is een niet -glaro hormoon. De klierhormonen van de hypofyse verzamelen.
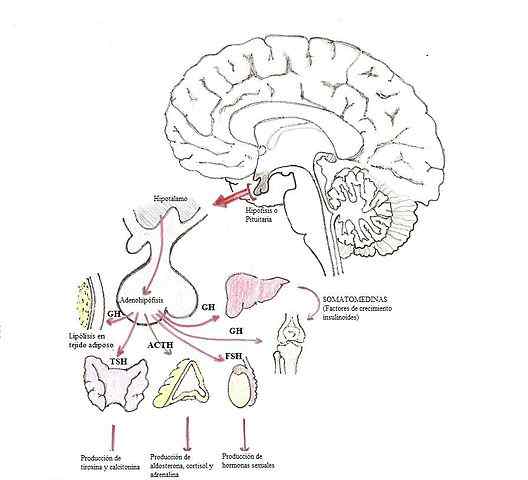
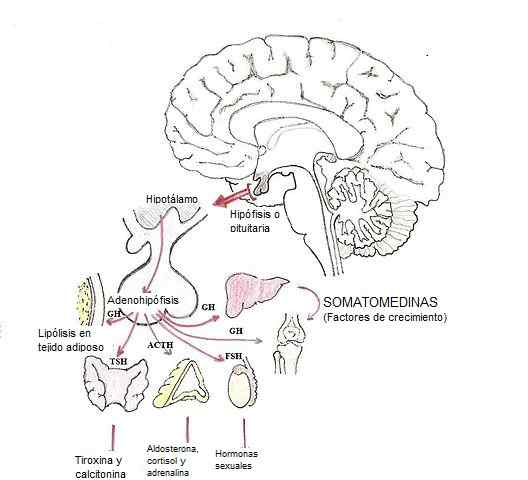 Modificatie van hormonen in de hypofyse (Bron: Dubaele / Public Domain, via Wikimedia Commons)
Modificatie van hormonen in de hypofyse (Bron: Dubaele / Public Domain, via Wikimedia Commons) Glandotropashormonen zijn bijvoorbeeld adrenocortopine (ACTH), gonadotropines (FSH en LH) en schildklierstimulerend hormoon (TSH).
Niet -Glandropas -hormonen daarentegen, en waaronder prolactine en groeihormoon worden opgenomen, handelen zonder de wedstrijd van een andere endocriene klier, omdat ze hun acties rechtstreeks uitoefenen op de witte cellen waarvan de activiteiten reguleren.
[TOC]
Structuur
Groeihormoon is een relatief klein eiwit dat optreedt in verschillende isovormen. De belangrijkste isovorm bestaat uit ongeveer 191 aminozuren, heeft een molecuulgewicht van 22 kDa en komt van een langer voorloperpeptide (pre-GH) van 28 kDa, dat ook wordt uitgescheiden maar dat fysiologische functies mist.
In zijn structuur lijkt somatotropine te worden gehomologeerd met prolactine en chorionsomatomamamototropine (CS), produceerde de laatste in de placenta. Dat is de gelijkenis, die wordt geacht dat de drie een hormonale familie vormen.
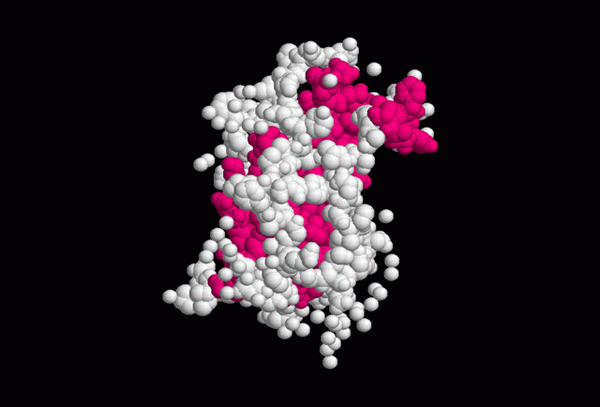 Geschat de structuur van het groeiphormoon (bron: раан бекер, via Wikimedia Commons)
Geschat de structuur van het groeiphormoon (bron: раан бекер, via Wikimedia Commons) De secundaire structuur van somatotropine toont 4 alfa -propellers gestabiliseerd met twee disulfidebruggen, waarvan de configuratie nodig is voor de interactie van het hormoon met zijn ontvanger.
Een feit in relatie tot de structuur, en waardig om te worden benadrukt, vertegenwoordigt het feit dat ondanks het feit dat de groeihormonen van verschillende soorten opmerkelijke overeenkomsten hebben met de mens, alleen de laatste, en die van primaten, effecten hebben die significant zijn bij mensen.
Functie
Somatotropin -functies worden meestal beschreven als die welke geassocieerd zijn met de ontwikkeling en groei van het organisme. Ook die geassocieerd met het metabolisme, waaronder modificaties in het lipidenmetabolisme en glucose bevorderd door hormoon.
Groeifuncties kunnen echter ook worden beschouwd als metabolisch, omdat ze anabole functies impliceren die geassocieerd zijn met eiwitsynthese, die sommige andere functies niet uitsluit zonder directe associatie met metabolisme zoals celproliferatie.
Sommige van de functies of acties die door somatotropine worden geïmplementeerd, worden door dit hormoon rechtstreeks over zijn witte weefsels uitgeoefend, maar veel van hen worden uitgevoerd door enkele andere stoffen waarvan de synthese en afgifte worden gestimuleerd door het groeihormoon.
IGF -synthese
De eerste lijn van somatotropine -werking is precies de synthese van deze stoffen die bekend staan als groeifactoren die vergelijkbaar zijn met insuline (IGF), waarvan typen 1 en 2 zijn geïdentificeerd. Ze worden aangeduid als IGF1 (de belangrijkste) en IGF2, volgens het acroniem in het Engels.
Deze factoren waren aanvankelijk bekend en worden nog steeds aangeduid als mediatoren van somatotropine of somatomedins C (IGF1) en A (IGF2) of ook als een activiteit vergelijkbaar met niet -onderdrukbare insuline (NSILA). Ze worden gesynthetiseerd door veel celtypen, maar komen voornamelijk voor in de lever.
De acties van de STH en de IGF1 zijn erg divers. Sommigen oefenen elk van deze stoffen onafhankelijk uit, soms in combinatie en synergetisch en sommige andere keren handelen ze antagonisch.
Kan u van dienst zijn: elektroforese: foundation, techniek, waarvoor is het voor, voorbeeldenInductie van groei
Dit is een van de belangrijkste acties die worden gepromoot door somatotropine, maar uitgevoerd in combinatie met de IGF1. Hoewel beide de groei van talloze lichaamsweefsels veroorzaken, wordt hun meest prominente effect op skeletgroei uitgeoefend.
Dit eindresultaat wordt geproduceerd door verschillende effecten geïnduceerd door het hormoon en de IGF1. Ze omvatten de toename van eiwitafzetting door chondrocytische en osteogene cellen, de hoogste reproductiesnelheid van deze cellen en de omzetting van chondrocyten in osteogene cellen; Dit alles leidt tot de nieuwe botafzetting.
Tijdens de groei en ontwikkeling van het organisme, en vóór de sluiting van botepiphyses, wordt nieuw kraakbeen afgezet in epifyses gevolgd door de conversie ervan in een nieuw bot, dat de diafyse verlengt en de epifyses worden gescheiden.
De progressieve consumptie van epiphyseale kraakbeen put het uit en het bot kan niet blijven groeien. Aan het einde van de adolescentie worden de diafyse en epifyses en de groei in lange botlengte aan elk uiteinde vertraagd en stopt uiteindelijk.
Een tweede mechanisme kan de toename van de botdikte verklaren. De osteoblasten van het periosteium afzetten in nieuw bot op de oude, en de osteoclasten elimineren het oude bot. Als de afzettingssnelheid de eliminatie overschrijdt, neemt de dikte toe.
Naarmate de groeihormoon intense stimulatie uitoefent op osteoblasten, kan de dikte van de botten onder het effect blijven toenemen, hoewel de lengte ervan niet langer wordt gemodificeerd vanwege de sluiting van epifyses.
Promotie van eiwitafzetting in weefsels
Dit effect kan worden bereikt door verschillende mechanismen: de toename van het transport van aminozuren door celmembranen, de toename van RNA -translatie op het niveau van de ribosomen, de toename van transcriptie van DNA naar RNA in de kern en een vermindering van eiwitten en aminozuur katabolisme.
Andere metabole acties
In vetweefsel bevordert groeihormoon lipolyse en afgifte van vetzuren aan de bloedsomloopstroom, die de concentratie in lichaamsvloeistoffen verhoogt. Tegelijkertijd bevordert het in alle weefsels de omzetting van vetzuren in acetyldenzym A en het gebruik ervan als een energiebron.
De stimulatie van het gebruik van vetten, samen met de accumulatie van eiwitten vanwege hun anabole effect, leidt tot een toename van mager weefsel.
De toename van de mobilisatie van vetten kan zo hoog zijn dat de lever grote hoeveelheden acetoazijnzuur produceert die leiden tot ketose en een vettige lever kan worden gegenereerd.
In relatie tot het metabolisme van koolhydraten omvatten de effecten van somatotropine de afname van glucosecollectie in vet en spierspierweefsel, verhoogde glucose leverproductie en verhoogde insulinesecretie.
Al deze effecten worden diabetogenen genoemd, en hoge groeihormoonafscheiding kan metabole veranderingen reproduceren die gepaard gaan met niet -insuline -afhankelijke type II diabetes.
Andere functies
De anabole en mitogene acties van de GH en de IGF1 manifesteren zich ook in de groei en functie van het hart, de lever, de milt, van de schildklier, van de thymus en van de tong. Het hormoon kan bijdragen aan de verdikking van de huid, aan de stimulatie van de zweetklieren en de haargroei.
In de nieren neemt de glomerulaire filtratiesnelheid en de synthese van calcitriol toeneemt, die niet alleen groei bevordert, maar ook bottenmineralisatie. Het bevordert ook erytropoëse en fibrinogeensynthese en immuunrespons door stimulatie van T -lymfocyten en macrofagen.
Kan u dienen: Epitheliaal weefsel: kenmerken, beschrijving, functies, typenReceptoren voor somatotropine
Somatotropine -acties, inclusief de bevordering van de synthese van groeifactoren die vergelijkbaar zijn met insuline, worden gemedieerd door hun vereniging met specifieke receptoren die tot expressie worden gebracht in membranen van witte cellen.
Er zijn twee vormen van deze receptoren, waarvan de tweede een korte (afgeknotte) variant van de eerste is; Afgeknotte vorm die de functie van de lange ontvanger remt, en dat, als het tot overexpressie wordt gebracht, het weefselongevoeligheid voor het hormoon zou veroorzaken.
De lange ontvanger bestaat uit 638 aminozuren en heeft een extracellulair domein van 250, een alfa -transmembaal domein van ongeveer 38 en een intracellulair domein van 350 aminozuren. Elk somatotropinemolecuul bundelt uiteindelijk twee ontvangermoleculen en produceert wat de receptordimerisatie wordt genoemd.
Deze dimerisatie activeert een JAK2 -kinase -eiwit dat zich op de intracellulaire uiteinden van elke monomeer van de ontvanger bevindt en deze actieve kinase fosforyleren andere substraten zoals de STAT5 en de somatotropineceptor zelf.
De gefosforyleerde STAT5 -moleculen hebben ook een dimerisatie die hen zeer precieze regulatoren van genexpressie en eiwitsynthese maakt.
Productie
Somatotropine wordt gesynthetiseerd op het niveau van de adenohypophysis somatotropascellen. Deze cellen worden intens geverfd met zure stoffen, zodat ze ook Acidophils worden genoemd. Ze zijn samen de meest voorkomende celgroep van de klier, omdat ze 50% van het totaal van 5 verschillende typen vertegenwoordigen.
Er is een genetisch complex van 5 genen in de lange arm van het menselijke chromosoom 17 dat codeert voor de verschillende isovormen van het groeihormoon en het menselijke chorion somatomamototropine (HCS).
Een van hen is de normale HGH-N, die codeert voor de meest voorkomende vorm van menselijk groeihormoon dat de eerder genoemde is van 22 kDa en 75% van het totale circulerende groeihormoon vertegenwoordigt.
Zijn RNA van de boodschapper wordt onderworpen "Snijden en splitsen" Om een kleinere vorm van het hormoon te produceren, van 20 kDa, die aminozuurafval mist van 32 naar 46 en 10% vertegenwoordigt.
Een tweede gen (HGH-V) wordt voornamelijk tot expressie gebracht in de placenta en codeert. De andere 3 genen coderen voor isovormen van Somatomamototropin Human.
Uitgave
Zowel synthese als de secretie of afgifte van groeihormoon worden gereguleerd door stimulerende en remmende factoren van dergelijke functies.
Stimulerende invloeden
Een van de belangrijkste humoristische invloeden zijn stimulerende synthese en somatotropine -secretie GHRH -peptiden (groeihormoon vrijgevend hormoon) en ghrelin.
Het groeihormoon bevrijdende hormoon (GHRH) is een hypothalamisch peptide dat bestaat in twee varianten van respectievelijk 40 en 44 aminozuren. Het leidt in somatotropascellen naar de synthese van AMPC en naar de activering van de specifieke PIT1 -transcriptiefactor voor het groeihormoon.
Ghrelin is een endogeen van groeihormoon van groeihormoon. Het is een peptide van ongeveer 28 aminozuren gesynthetiseerd op de hypothalamus en maagniveau. Het werkt synergetisch met GHRH wiens release bevordert, terwijl het somatostatine remmen. Werkt door receptoren die fosfolipase c activeren.
Sommige metabole parameters zoals hypoglykemie, lage niveaus van vrije vetzuren in bloed en hoge aminozuurconcentraties zijn belangrijke stimuli voor de secretie van groeihormoon.
Kan u van dienst zijn: de 12 fasen van de menselijke ontwikkeling en de kenmerken ervanAndere stimulerende factoren die tellen zijn acute stress, lichaamsoverbelasting, pijn, geslachtssteroïden (puberteit), dopamine, stimulatie van α2-receptoren, acetylcholine, galanine, serotonine en β-endorfine.
Remmende invloeden
Onder deze zijn somatostatine of hormoonremmer van de afgifte van groeihormoon (GHRIH) en negatieve feedback.
Somatostatine is een hypothalamisch peptide van 14 aminozuren die secretie remt, maar geen synthese, van groeihormoon. Een lange variant, 28 aminozuren, wordt gesynthetiseerd in het maagdarmkanaal. Beide varianten binden aan dezelfde ontvanger en remmen cyclische AMP -synthese.
Wat betreft negatieve feedback, belt de GH, door een zelf -sociale actie, zijn eigen verdere vrijgave. De IGF1 remt de hypothalamus voor het groeihormoon van groeihormoon en stimuleert somatostatine, terwijl de GH -synthese in de hypofyse remt.
Sommige metabole parameters zoals hyperglykemie, hoge plasmaspiegels van vrije vetzuren en lage aminozuurniveaus zijn somatotropinesecretie -remmers.
Remmers zijn ook koud, chronische stress, adipositeit, progesteron, schildklierhormonen, tekorten of cortisol -excessen en stimulatie van adrenerge receptoren β2 β2.
Dosis
Het therapeutische gebruik van biosynthesized groeihormoon is geïndiceerd voor de behandeling van dat lijden waarin een tekort aan de secretie is onthuld, in hypofyse dwergdarfisme en bij kinderen met een laag grootte door Turner's syndroom.
De toediening wordt gemaakt in de vorm van een injecteerbare oplossing herbouwd vanuit een weg die een gelyofiliseerde met 40 us bevat.Je. van het biosynthetische hormoon, en waaraan de 2 ml metgezellen van 0,9 % natriumchloride -oplossing worden toegevoegd.
In groeihormoontekort bij kinderen wordt het aanbevolen tussen 0,07 en 0,1 u.Je./kg lichaamsgewicht per dag. In het Turner -syndroom 0,14 u.Je./kg lichaamsgewicht per dag. Voor groeihormoontekort bij volwassenen: 0,018 tot 0,036 u.Je./kg lichaamsgewicht per dag.
Effecten
De therapeutische toediening van groeihormoon kan gepaard gaan met enkele nadelige onderpandeffecten, zoals manifeste overgevoeligheid door gegeneraliseerde urticaria, vastende hypoglykemie, ontsteking op de injectieplaats en passagiershoofdpijn.
De ontwikkeling van een zekere goedaardige intracraniële hypertensie is beschreven, vaker voor kinderen en minder bij volwassenen.
Wat betreft het koolhydraatmetabolisme, is de ontwikkeling van diabetes mellitus gemeld bij patiënten die behandeling hebben ontvangen met groeihormoon.
In relatie tot het skeletspiersysteem zijn er aanwijzingen voor inflammatoire myositis met myalgie en spierzwakte, geproduceerd niet door het hormoon, maar misschien door de metacresol die als conservatief in de formule wordt gebruikt.
Gevallen van gynaecomastie, bloedarmoede en acute pancreatitis zijn gemeld.
Referenties
- Ganong WF: The hypofyse, 25e ed. New York, McGraw-Hill Education, 2016.
- Guyton AC, Hall JE: hypofysehormonen en hun controle door de hypothalamus, in Leerboek van medische fysiologie, 13e ed, AC Guyton, JE Hall (eds). Philadelphia, Elsevier Inc., 2016.
- Lang F, Verrey F: Hormone, In Physiologie des Menschen Mite Pathophysiologie, 31 e ed, RF Schmidt et al (eds). Heidelberg, Springer Medizin Verlag, 2010
- Voigt K: Endokrines System, in Physiologie, 6e ed; R Klinke et al (eds). Stuttgart, Georg Thieme Verlag, 2010.
- Widmaier EP, Raph H en Strang KT: het endocriene systeem. De hypothalamus en hypofyse, in de menselijke fysiologie van Vander: de mechanismen van lichaamsfunctie, 13e ed; EP Windmaier et al (eds). New York, McGraw-Hill, 2014.
- « Alliteratieconcept, kenmerken en voorbeelden
- Groepscommunicatiekenmerken, elementen, voorbeelden »

