Calciumfosfaat (CA3 (PO4) 2)

- 4556
- 1465
- Kurt Aufderhar Jr.
Hij calciumfosfaat Het is een anorganisch en tertiair zout waarvan de chemische formule CA is3(PO4))2. De formule stelt vast dat de samenstelling van dit zout 3: 2 is voor respectievelijk calcium en fosfaat. Dit is direct te zien in de onderste afbeelding, waar het ca -kation wordt getoond2+ en de anion po43-. Voor elke drie CA2+ Er zijn twee PO43- Interactie met hen.
Aan de andere kant verwijst calciumfosfaat naar een reeks zouten die variëren afhankelijk van de Ca/P -verhouding, evenals de mate van hydratatie en pH. In feite zijn er veel soorten calciumfosfaten die bestaan en kunnen worden gesynthetiseerd. Na de brief verwijst de nomenclatuur, calciumfosfaat echter alleen naar de driewieler, de eerder genoemde.
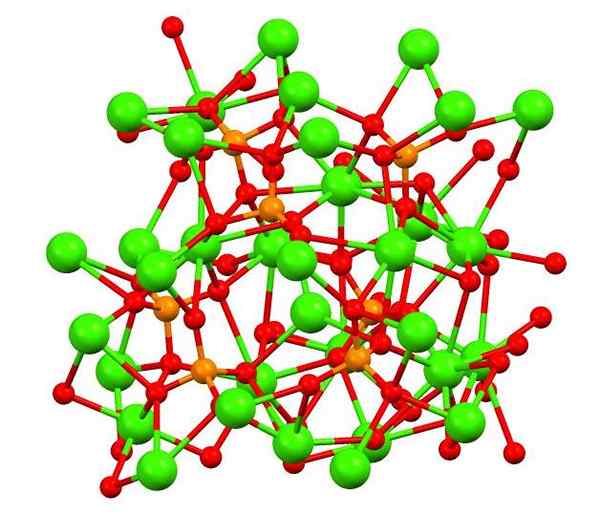
 Verhouding en ionen in tricycal fosfaat. Bron: Richard-59 [CC BY-SA 3.0 (https: // creativeCommons.Org/licenties/by-sa/3.0)], van Wikimedia Commons
Verhouding en ionen in tricycal fosfaat. Bron: Richard-59 [CC BY-SA 3.0 (https: // creativeCommons.Org/licenties/by-sa/3.0)], van Wikimedia Commons Alle calciumfosfaten, inclusief CA3(PO4))2, Het zijn witte vaste stoffen met lichte grijze tonen. Ze kunnen korrelig, fijn, kristallijn zijn en hebben deeltjesgroottes rond de micrometers; En zelfs nanodeeltjes van deze fosfaten zijn bereid, waarmee biocompatibele materialen voor de botten zijn ontworpen.
Deze biocompatibiliteit is omdat deze zouten in de tanden worden gevonden en in korte verslagen in zoogdierbotweefsels. Hydroxyapatiet is bijvoorbeeld een kristallijn calciumfosfaat, dat op zijn beurt interageert met een amorfe fase van hetzelfde zout.
Dit betekent dat er fosfaten zijn van amorfe en kristallijne calcio's. Om die reden is het niet verwonderlijk de diversiteit en meerdere opties bij het synthetiseren van materialen op basis van calciumfosfaten; Materialen in wiens eigenschappen elke dag meer geïnteresseerde onderzoekers wereldwijd zijn om zich te concentreren op botherstel.
Calciumfosfaatstructuur
 Calciumfosfaat in het mineraal van Whitlockita. Bron: Smokefoot [CC BY-SA 4.0 (https: // creativeCommons.Org/licenties/by-sa/4.0)], van Wikimedia Commons
Calciumfosfaat in het mineraal van Whitlockita. Bron: Smokefoot [CC BY-SA 4.0 (https: // creativeCommons.Org/licenties/by-sa/4.0)], van Wikimedia Commons Het bovenste beeld toont de structuur van tribasisch calisch fosfaat in het vreemde Whitlockita -mineraal, dat magnesium en ijzer als onzuiverheden kan bevatten.
Hoewel het op het eerste gezicht mogelijk complex lijkt, is het noodzakelijk om te verduidelijken dat het model covalente interacties veronderstelt tussen de zuurstofatomen van fosfaten en calciummetaalcentra.
Kan u van dienst zijn: berylliumhydride (Beh2)Als weergave is het echter geldig, de interacties zijn echter elektrostatisch; dat wil zeggen, cations2+ Voel een aantrekkingskracht voor PO43- (AC2+- O-po33-)). Met dit in gedachten is het te begrijpen waarom in het beeld calcium (groene bollen) wordt omgeven door negatief geladen zuurstofatomen (rode bollen).
Wanneer er zoveel ionen zijn, laat een symmetrische opstelling of patroon niet zichtbaar. De CA3(PO4))2 goedkeuring bij lage temperaturen (t<1000°C) una celda unitaria correspondiente a un sistema cristalino romboédrico; a este polimorfo se le conoce con el nombre de β-Ca3(PO4))2 (β-TCP, voor zijn acroniem in het Engels).
Bij hoge temperaturen wordt het daarentegen de a-CA-polymorf3(PO4))2 (α-TCP), waarvan de eenheidscel overeenkomt met een monoklinisch kristallijn systeem. Bij nog hogere temperaturen kan de a'-Ca polymorf ook worden gevormd3(PO4))2, dat is zeshoekige kristallijne structuur.
Amorf calciumfosfaat
Kristallijne structuren voor calciumfosfaat zijn genoemd, die wordt verwacht van een zout. Dit is echter in staat om weer te geven.
Wanneer dit gebeurt, wordt gezegd dat calciumfosfaat een amorfe structuur heeft (ACP, Amorf calciumfosfaat)). Verschillende auteurs wijzen op dit type structuur als verantwoordelijk voor de biologische eigenschappen van de CA3(PO4))2 In botweefsels zijn reparatie en biomimetisatie mogelijk.
De rest van het gezin
Calciumfosfaten zijn in feite een familie van anorganische verbindingen, die op hun beurt kunnen interageren met een organische matrix.
De andere fosfaten worden verkregen "eenvoudig" de anionen die gepaard gaan met calcium (PO43-, HPO42-, H2Po4-, Oh-), zoals het type onzuiverheden in de vaste stof. Aldus kunnen tot elf calcium of meer fosfaten, elk met hun eigen structuur en eigenschappen, op natuurlijke wijze of kunstmatig worden gepresenteerd.
Sommige fosfaten en hun respectieve chemische structuren en formules worden hieronder vermeld:
-Waterstof dihydrado calciumfosfaat, cahpo4∙ 2H2O: monoklinisch.
Kan u van dienst zijn: ammoniumoxalaat-Dihydrogen monohydrated calciumfosfaat, Ca (h2Po4))2∙ H2O: Triclinic.
-Watervrije dease fosfaat, ca (h2Po4))2: Triclinic.
-Waterstof octacalcisch fosfaat (OCP), CA8H2(PO4))6: Triclinic. Het is een voorloper in de synthese van hydroxyapatiet.
-Hydroxyapatite, ca5(PO4))3Oh: zeshoekig.
Fysische en chemische eigenschappen
Namen
-Calciumfosfaat
-Tricalcium fosfaat
-Triccal difosfaat
Molecuulgewicht
310.74 g/mol.
Fysieke beschrijving
Het is een witte vaste stof.
Smaak
Smaakloos.
Smeltpunt
1670 ºK (1391 ºC).
Oplosbaarheid
-Praktisch onoplosbaar in water.
-Onoplosbaar in ethanol.
-Oplosbaar in zoutzuur en verdund salpeterzuur.
Dikte
3.14 g/cm3.
Brekingsindex
1.629
Standaard training enthalpie
4126 kcal/mol.
Bewaar temperatuur
2-8 ºC.
pH
6-8 in een waterige suspensie van 50 g/l calciumfosfaat.
Opleiding
Calcium- en waterstofnitraat ammoniumfosfaat
Er zijn talloze methoden om calciumfosfaat te produceren of te vormen. Een van hen bestaat uit een mengsel van twee zouten, CA (nee3))2∙ 4H2Of, en (NH4))2HPO4, eerder opgelost in respectievelijk absoluut alcohol en water. Het ene zout draagt calcium en het andere fosfaat bij.
Uit dit mengsel gaat de ACP neer, die vervolgens verwarming ondergaat in een oven bij 800 ° C en gedurende 2 uur. Als gevolg van deze procedure wordt β-CA verkregen3(PO4))2. De vorming van nanocristals kan zorgvuldig de temperaturen, agitatie en contacttijden beheersen, de vorming van nanocristallen kan optreden.
Om de a-Ca polymorf te vormen3(PO4))2 Het is noodzakelijk om het fosfaat boven 1000 ° C te verwarmen. Deze opwarming wordt uitgevoerd in aanwezigheid van andere metaalionen, die deze polymorf voldoende stabiliseren zodat deze bij kamertemperatuur kan worden gebruikt; dat wil zeggen, het blijft in een stabiele doelstatus.
Calciumhydroxide en fosforzuur
Calciumfosfaat kan ook worden gevormd door het mengen van calciumhydroxide en fosforzuuroplossingen, optredende zuur-base neutralisatie. Na een halve dag rijping bij de moedersgeesten, en hun gepaste filtratie, wassen, drogen en gezeefd, een korrelig stof van amorf fosfaat, wordt ACP verkregen.
Dit ACP -reacties van hoge temperaturen, transformerend volgens de volgende chemische vergelijkingen:
2CA9(HPO4) (PO4))5(Oh) => 2ca9(P2OF7))0,5(PO4))5(Oh) + h2O (a t = 446,60 ° C)
2CA9(P2OF7))0,5(PO4))5(Oh) => 3CA3(PO4))2 + 0,5 uur2O (A T = 748.56 ° C)
Kan u van dienst zijn: selenium: geschiedenis, eigenschappen, structuur, verkrijgen, gebruikOp deze manier wordt de β-CA verkregen3(PO4))2, Uw meest voorkomende en stabiele polymorf.
Toepassingen
In botweefsel
De CA3(PO4))2 Het is het belangrijkste anorganische bestanddeel van botas. Het is een component van botvervangingstransplantaties, dit wordt verklaard door zijn chemische gelijkenis met de mineralen die in het bot aanwezig zijn.
Biomaterialen van calciumfosfaat worden gebruikt om botdefecten te corrigeren en bij het bedekken van metalen prothesen. Calciumfosfaat wordt erop afgezet, isoleert ze uit de omgeving en vertraagt het corrosieproces van het titanium.
Bioceramic Cements
Calciumfosfaatcement (CPC) is een ander biokeramiek dat wordt gebruikt bij beperken van botweefsel. Het wordt uitgewerkt door het stof van verschillende soorten calciumfosfaten met water te mengen, waardoor een pasta wordt gevormd. Pasta kan worden geïnjecteerd of aangepast aan het botdefect of de holte.
De cementen zijn gevormd, geleidelijk opnieuw geabsorbeerd en worden vervangen door het nieuw gevormde bot.
Artsen
-De CA3(PO4))2 Het is een basiszout, dus het wordt gebruikt als een antacida om overtollige maagzuurgraad te neutraliseren en de pH te verhogen. In tandheelkundige pasta levert een bron van calcium en fosfaat om het proces van remineralisatie van tanden en bothemostase te vergemakkelijken.
-Het wordt ook gebruikt als een voedingssupplement, hoewel de meest economische manier om calcium te leveren is door het carbonaat en citraat te gebruiken.
-Calciumfosfaat kan worden gebruikt bij de behandeling van Tethany, latente hypocalciëmie en onderhoudstherapie. Bovendien is het nuttig bij calciumsuppletie tijdens zwangerschap en borstvoeding.
-Het wordt gebruikt bij de behandeling van besmetting met radioactieve isotopos-radio (RA-226) en strontium (SR-90). Calciumfosfaat blokkeert de absorptie van radioactieve isotopo's in het spijsverteringskanaal, waardoor de schade wordt beperkt die ertoe wordt veroorzaakt.
Anderen
-Calciumfosfaat wordt gebruikt als voer voor vogels. Bovendien wordt het gebruikt in tandpasta's in de controle van de wijnsteen.
-Het wordt gebruikt als een anti -gomerant middel, bijvoorbeeld om te voorkomen dat tafelzout compacte is.
-Het werkt als een bleekmiddel van de bloem. Ondertussen voorkomt in Cochino Butter een ongewenste kleuring en verbetert de toestand van frituren.
Referenties
- Calciumfosfaat. Hersteld van: pubchem.NCBI.NLM.NIH.Gov
- Calciumfosfaat. Wetenschap direct. Opgehaald uit: Scientedirect.com
- « Indonesische vlaggeschiedenis en betekenis
- Tlachichinol Wat is, kenmerken, voordelen, toepassing »

