Fenolen of fenolische verbindingen eigenschappen, typen, toepassingen

- 3919
- 1227
- Dewey Powlowski
De Fenolen Ze zijn een familie van organische verbindingen (alcoholen) die worden gekenmerkt door een aromatische ring waarin een of meer van de waterstofatomen geassocieerd met de koolstofatomen van de ring worden vervangen door een of meer hydroxylgroepen (-OH).
De fenolen en hun derivaten zijn normaal aanwezig in de natuur, omdat ze als organische moleculen praktisch worden geproduceerd door alle levende wezens.
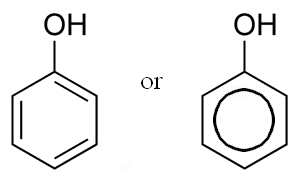 Chemische structuur van fenol, de eenvoudigste fenolische verbinding (Bron: Dbenbenn, via Wikimedia Common)
Chemische structuur van fenol, de eenvoudigste fenolische verbinding (Bron: Dbenbenn, via Wikimedia Common) Van de meest voorkomende voorbeelden van fenolen kunnen we het aminozuurtyrosine noemen, een van de 20 eiwitaminozuren, die als substituent groep A fenolring heeft; Ze hebben ook fenolische groepen adrenaline en serotonine, twee zeer belangrijke hormonen voor zoogdieren.
Planten zijn de "leraren" bij de productie van fenolische verbindingen, omdat veel van hun secundaire metabolieten (fundamenteel voor hun groei, reproductie, bescherming, enz.) Ze hebben een of meer van deze chemische groepen in hun structuren, die meestal afkomstig zijn van metabole routes zoals het pentosefosfaat, die van shiquimato en die van fenylpropanoïden.
 Tyrosine -aminozuurstructuur, waarvan de groep R een fenolische ring is (benzeen + OH) (Bron: Neurotokeker, via Wikimedia Commons)
Tyrosine -aminozuurstructuur, waarvan de groep R een fenolische ring is (benzeen + OH) (Bron: Neurotokeker, via Wikimedia Commons) De fenolen zijn op grote schaal bestudeerd vanwege de kenmerken die ze vertonen in het gezicht van oxidatieve stress (zoals antioxidanten) bij mensen, vooral bij mensen die lijden aan metabole pathologieën zoals obesitas, diabetes of een cardiovasculaire toestand.
Met deze antioxiderende eigenschappen valt α-tocoferol op, een fenolische derivatencomponent van vitamine E, die aanwezig is in bloedplasma en in staat is om vrije peroxide-radicalen te "vangen" die mogelijk schadelijk zijn voor cellen voor cellen voor cellen voor cellen.
Bovendien heeft de mens in de antropogene context "geleerd" om de eigenschappen van fenolische verbindingen te benutten vanuit industrieel oogpunt voor de productie van kleurstoffen, polymeren, geneesmiddelen en andere organische stoffen met een breed scala aan verschillende toepassingen en eigenschappen , hoewel veel hiervan helaas belangrijke bronnen van milieuvervuiling vertegenwoordigen.
[TOC]
Eigenschappen van fenolen
Fenolische verbindingen hebben een grote diversiteit aan fysicochemische eigenschappen, die direct gerelateerd zijn aan hun gunstige eigenschappen voor dieren- en plantencellen.
De hydroxylgroepen van de fenolen bepalen hun zuurgraad, terwijl hun bentnische ring (de aromatische ring) de basiciteit bepaalt. Vanuit fysicochemisch oogpunt kunnen we dat fenolen zeggen:
- Het zijn verbindingen met een laag smeltpunt.
- Evenals alle andere alcohol, fenolen hebben hydroxylgroepen die kunnen deelnemen aan intermoleculaire waterstofbruggen (waterstofbruggen), zelfs sterker dan die welke andere alcoholen kunnen vormen.
- Bij het kristalliseren vormen deze verbindingen een soort kristallen als kleurloze "prisma's" die een karakteristieke doordringende geur hebben.
Kan u van dienst zijn: ovalbumin: structuur, functies, denaturatie- Bij het smelten vormen fenolen kristallijne "mobiele" vloeistoffen (kleurloos).
- Dankzij het feit dat ze waterstofbruggen kunnen vormen, kunnen deze verbindingen zeer oplosbaar zijn in water, wat afhangt van de temperatuur en algemene kenmerken van de andere groepen waaraan ze worden geassocieerd.
- Ze worden snel opgelost in de meeste organische oplosmiddelen, vooral bij degenen wier samenstelling bestaat uit aromatische koolwaterstoffen, alcoholen, ketonen, ethers, zuren, gehalogeneerde koolwaterstoffen, enz. (die ook afhangt van de algemene structuur van het molecuul dat de fenolische groepen herbergt).
- Ze hebben een vriespunt van ongeveer 40 ° C.
- Het molecuulgewicht varieert tussen 94 en 100 g/mol.
Cellen
Wat cellen betreft, daarentegen, worden fenolverbindingen gekenmerkt door:
- Wees antioxidantverbindingen, omdat ze een reducerende eigenschappen hebben, functionerend als "donoren" -middelen van waterstof of elektronen (ze fungeren als "ontvoerders" van vrije radicalen).
- Wees chelars van metaalionen, met name ijzer en koper, die de vorming van vrije radicalen onderdrukken die worden gekatalyseerd door metalen.
- Antimicrobiële activiteit hebben, omdat ze in staat zijn om de invasie van microben uit te stellen en rot en groentotrot te voorkomen (zodat ze ook industrieel worden benut).
Classificatie: soorten fenolen
Afhankelijk van de context kunnen fenolen op verschillende manieren worden geclassificeerd, maar de meest gebruikte chemische classificatie is gebaseerd op het aantal hydroxylgroepen (-OH) die binden aan dezelfde aromatische ring (een waterstofatoom vervangen). In die zin zijn ze gedefinieerd:
- Fenolen monohydric, Met een enkele hydroxylgroep
- Fenolen Dihydries, Met twee hydroxylgroepen
- Fenolen trihydric, Met drie hydroxylgroepen
- Fenolen Polyhydric, Met meer dan drie hydroxylgroepen
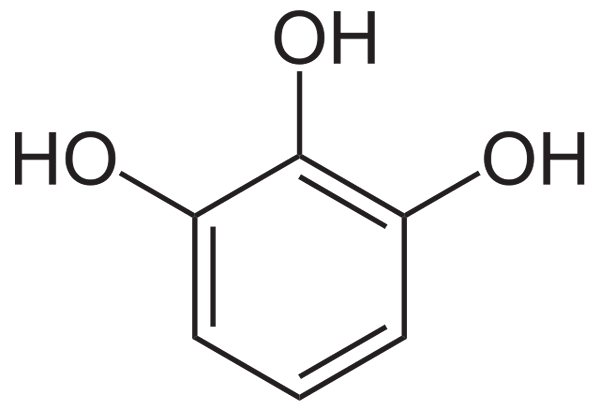 Pyrogalol (Trihydroxyfenol), een fenolische verbinding die gewoonlijk wordt gebruikt voor de productie van capillaire kleurstoffen, als een antiseptisch en als een "ontwikkelaar" -agent in de wit-neger-ontwikkelaars (Bron: Neurotoger / Public Domain, Via Wikimedia Commons via Wikimedia)
Pyrogalol (Trihydroxyfenol), een fenolische verbinding die gewoonlijk wordt gebruikt voor de productie van capillaire kleurstoffen, als een antiseptisch en als een "ontwikkelaar" -agent in de wit-neger-ontwikkelaars (Bron: Neurotoger / Public Domain, Via Wikimedia Commons via Wikimedia) Deze organische verbindingen kunnen eenvoudige fenolische moleculen of gepolymeriseerde verbindingen van grote complexiteit zijn en er is aangetoond dat de meeste fenolen die in de natuur worden gevonden, optreden als mono- en polysaccharide-conjugaten, van esters en methylesters.
Opgemerkt moet worden dat andere classificaties ook gerelateerd zijn aan het "niet -fenolische gedeelte" van de verbindingen, maar dit hangt grotendeels af van de bron van het verkrijgen (natuurlijk of kunstmatig).
Extractiemethoden
De fenolen werden in 1834 ontdekt door Friedlieb Runge, die geïsoleerd is fenol (De eenvoudigste fenolische verbinding) van minerale teermonsters en noemde het "carbolzuur" of "kolenolie" zuur ". Het pure fenol werd echter een paar jaar later door Auguste Laurent bereid, in 1841.
Kan u van dienst zijn: dieren- en plantenorganogenese en de kenmerken ervanMomenteel worden kleine hoeveelheden fenol nog steeds geïsoleerd uit tarry- en cola -planten (planten krakend)). Veel synthetische methoden die zowel in het verleden als tegenwoordig worden gebruikt, omvatten echter de synthese van fenol van benzeen als voorloperring, ondanks het feit dat het een extreem vluchtige en carcinogeenverbinding is.
De synthese van deze verbindingen van benzeen kan prima zijn door hydrolyse van chloorbenzeen of oxidatie van het isopropylbenzeen (cumeno).
- Uittreksel
Een groot aantal fenolische verbindingen van natuurlijke oorsprong wordt geëxtraheerd uit preparaten uit verschillende delen van de anatomie van groenten. Helaas zijn er voor dit doel geen gestandaardiseerde protocollen, omdat veel afhankelijk is van het doel van extractie, het type weefsel, de specifieke klasse van fenol, onder andere factoren.
Monsterbereiding
Over het algemeen worden de monsters eerder bereid door technieken zoals drogen of uitdroging, verpletterd, homogenisatie of filtratie.
Er moet rekening mee worden gehouden dat bij het extraheren van fenolen van plantenmonsters een complex mengsel van fenolverbindingen van verschillende klassen daadwerkelijk wordt verkregen, vooral die welke kenmerken hebben die ze meer oplosbaar maken in de oplosmiddelen die voor dit doel worden gebruikt.
Extractietechnieken
De extractie, zodra de monsters zijn verkregen en voor dit doel zijn bereid, wordt meestal uitgevoerd door incubatie van de monsters verkregen in organische oplosmiddelen, waarbij de organische fase vaak wordt gezuiverd door methoden zoals vaste fase -extractie, kolomchromatografie en tegenstroomchromatografie.
Naast oplosmiddelextractie omvatten andere technieken het gebruik van echografie, magnetron of voorgelicht en superkritische vloeistoffen.
Fenolen -toepassingen
De fenolen hebben meerdere toepassingen, zowel die geïsoleerd zijn van levende organismen als die welke kunstmatig worden gesynthetiseerd.
In de voedselproductie
De voedingsindustrie maakt gebruik van veel fenolische verbindingen om producten te "versterken", waardoor de halfwaardetijd van sommige voedingsmiddelen wordt vergroot en zelfs deel uitmaakt van de actieve voedingsverbindingen daarvan.
De belangrijkste reden waarom ze zo nuttig zijn, is omdat ze een goede "bio -drukker" hebben bewezen voor bederfelijke voedingsmiddelen en bovendien mogelijk voedselproductie mogelijk maken zonder synthetische additieven te gebruiken die negatieve gevolgen kunnen hebben voor de gezondheid van de consument.
Industriële toepassingen van sommige synthetische fenolen
Het fenol, dat een van de eenvoudigste fenolische verbindingen is en de meest vervuilende, wordt verkregen uit minerale teer en sommige synthetische methoden en wordt vaak gebruikt voor de productie van:
Kan u van dienst zijn: primaire bouillon of primitieve soep- Verhuur (voor herbiciden en kunststoffen)
- Cresoles (voor oplosmiddelen)
- Xilenolen (voor de productie van antioxidanten en redox -indicatoren)
- fenolische harsen
- Anilines (voor de productie van polyurethaan, schilderijen, herbiciden, vernissen, enz.))
- Textielverf
- Explosieven
- pesticiden, etc.
Chloorfenolen, de grootste groep fenolen worden gebruikt voor de synthese van desinfectiemiddelen, herbiciden en pesticiden. Deze leiden de lijst met bodemverontreinigende stoffen, water en landbouwproducten.
Gebruik van sommige natuurlijke fenolen
Veel fenolische verbindingen van natuurlijke oorsprong zijn dagelijkse werknemers in de farmaceutische en medische industrie voor de behandeling en preventie van pathologieën zoals kanker. Deze verbindingen zijn geïsoleerd uit kruiden en medicinale planten en omvatten een reeks fenolzuren, flavonoïden, tannines, curcuminoïden, lignanen, chinonen, enz.
Veel van deze verbindingen zijn actief, zoals antioxidanten, anti -carcinogene, antimutagene en zelfs ontstekingsremmendeheden.
Er is aangetoond dat sommige hiervan geprogrammeerde celdood of de "arrestatie" van de celcyclus kunnen induceren, en metabolisme, celadhesie, migratie en proliferatie kunnen reguleren, dus ze zijn mogelijk gunstig voor de behandeling van tumoren.
 2,3-hydroxycinaminezuur, een fenol dat aanwezig is als een metaboliet in menselijke urine (Bron: ED (Edgar181) / Public Domain, via Wikimedia Commons)
2,3-hydroxycinaminezuur, een fenol dat aanwezig is als een metaboliet in menselijke urine (Bron: ED (Edgar181) / Public Domain, via Wikimedia Commons) Voedsel met fenolische verbindingen
Aangezien veel secundaire metabolieten geproduceerd door planten een groot aantal fenolische verbindingen hebben, zijn de meeste groenten die we dagelijks consumeren rijk aan deze.
Op dezelfde manier hebben alle celeiwitten (van dieren, groenten en schimmels) verschillende verhoudingen tyrosine, het aminozuureiwit met een fenolische ring.
 Vrij-de afbeelding in www.Pixabay.com
Vrij-de afbeelding in www.Pixabay.com Onder de belangrijkste rijke voedingsfenolen en/of de derivaten ervan vallen op:
- de olijven
- Druiven
- Een groot aantal groenten en fruit
- rijst
- De aromatische kruiden (oregano, peper, koriander, bioscoop, kaneel, geurnagels, mosterd, gember, anijs, kurkuma, munt, etc.))
- de kruiden
- Thee en koffie
- het zeewier
- Noten en andere noten
- de wijn
- de chocolade
- Peulvruchten en andere zaden
Referenties
- Bento, c. & Gonçalves, Ana Carolina & Jesus, Fábio & Simões, Manuel & Silva, Luis. (2017). Fenolische verbindingen: bronnen, eigenschappen en toepassingen.
- Michałowicz, J., & Twijfel, w. (2007). Fenolen en toxiciteit. Pools Journal of Environmental Studies, 16 (3).
- Minatel, ik. OF., Borges, c. V., Ferreira, m. Je., Gomez, h. NAAR. G., Chen, c. EN. OF., & Lima, g. P. P. (2017). Fenolische verbindingen: functionele eigenschappen, impact van verwerking en biologische beschikbaarheid. Fenolische verbindingen Biologische activiteit. ED. Intech. Rijaka, Kroatië, 1-24.
- Santos-Buelga, c., Gonzalez-Manzano, s., Dueñas, m., & Gonzalez-paramas, een. M. (2012). Extractie en isolatie van fenolische compunds. In isolatie van natuurlijke producten (PP. 427-464). Mens.
- Serie, p. (2003). De chemie van functionele groep. The Chemistry of Phenols, ed. Z. Rappoport.
- Tyman, J. H. (1996). Synthetische en natuurlijke fenolen. Elsevier.
- Vuolo, m. M., Lima, v. S., & Junior, m. R. M. (2019). Fenolische verbindingen: structuur, classificatie en antioxidantkracht. In bioactieve verbindingen (PP. 33-50). Woodhead Publishing.
- Wade, l. (2018). Britannica Encyclopaedia. Ontvangen op 6 mei 2020, vanuit Britannica.com
- « Sociale instellingen verschijnen, kenmerken, functies, voorbeelden
- Lood nitraatstructuur, eigenschappen, verkrijgen, gebruik »

