Dibenzalacetona -eigenschappen, reactiemechanisme, gebruik, risico's

- 4044
- 46
- Alton D'Amore
De Dibenzalacetona (DBA) is een organische verbinding waarvan de moleculaire formule c is17H14OF. Het is een geelachtige vaste stof die, afhankelijk van de zuiverheid, kan worden gepresenteerd als kristallen. Het wordt gebruikt in zonnebrandmiddelen en organomethalische synthese waarin het paladium wordt gebruikt als katalysator.
Hoewel de synthese ervan een relatief eenvoudig, vrij terugkerend proces is in het onderwijzen van laboratoria om aldolische condensatie te verklaren, is het mechanisme een beetje uitgebreid, er moeten rekening worden gehouden met verschillende factoren. De gebruikte benzaldehyde, die zal condenseren met aceton, moet nieuw worden gedestilleerd om de lage oxidatie in contact met de lucht te garanderen.
 Dibenzalacetona monster in glazen container. Bron: StephanB [CC BY-SA (http: // creativeCommons.Org/licenties/by-sa/3.0/]]
Dibenzalacetona monster in glazen container. Bron: StephanB [CC BY-SA (http: // creativeCommons.Org/licenties/by-sa/3.0/]] Evenzo wordt een ethanolwatermedium gebruikt om de reagentia op te lossen en tegelijkertijd de uiteindelijke neerslag van het dibenzalaceton, hydrofobe en onoplosbare verbinding te bevorderen. Tot nu toe is het niet bekend welke negatieve effecten dibenzalaceton kunnen uitoefenen op het organisme of de omgeving, in plaats van een irritante stof te zijn.
[TOC]
Eigenschappen
Fysiek uiterlijk
Vast geelachtig stoffige of kristallijn uiterlijk.
Molaire massa
234.29 g/mol
Isomeren
Dibenzalaceton wordt gepresenteerd als drie geometrische isomeren: trans-trans-trans-trans-CIS en cis-cis. De trans-trans-isomeer is de meest stabiele en daarom degene die het meest voorkomt tijdens de synthese.
Smeltpunt
110-111 ºC. Dit bereik varieert afhankelijk van de zuiverheidsgraad van de gesynthetiseerde vaste stof.
Oplosbaarheid in water
Onoplosbaar.
Structuur
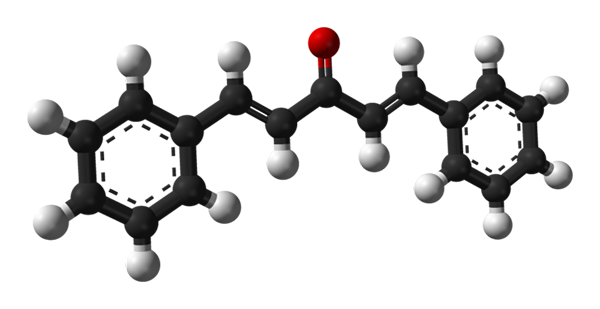 Moleculaire structuur van dibenzalaceton. Bron: Benjah-bmm27 [Public Domain]
Moleculaire structuur van dibenzalaceton. Bron: Benjah-bmm27 [Public Domain] In het bovenste beeld wordt het molecuul van de trans-trans-trans-transomeer getoond. In het midden ervan hebben we de carbonylgroep, en aan de zijkanten, dubbele obligaties en twee aromatische bonenceno -ringen.
Dibenzalaceton is in apolaire en hydrofobe essentie, omdat de gehele structuur vrijwel is samengesteld uit koolstof- en waterstofatomen. De carbonylgroep geeft het slechts een klein dipoolmoment.
Kan u van dienst zijn: aluminium fosfuro (AIP): structuur, eigenschappen, gebruik, risico'sDe structuur kan worden gelijkgesteld aan die van een blad, omdat al zijn koolstofatomen SP -hybridisatie hebben2; Daarom rusten ze in hetzelfde vlak.
Lichtfotonen interageren met het geconjugeerde π -systeem van de dibenzalacetona; Vooral die van UV -straling, geabsorbeerd om verhuisde elektronen op te wekken. Deze eigenschap maakt Dibenzalacetona een uitstekend absorberend ultraviolet licht.
Dibenzalacetona -reactiemechanisme
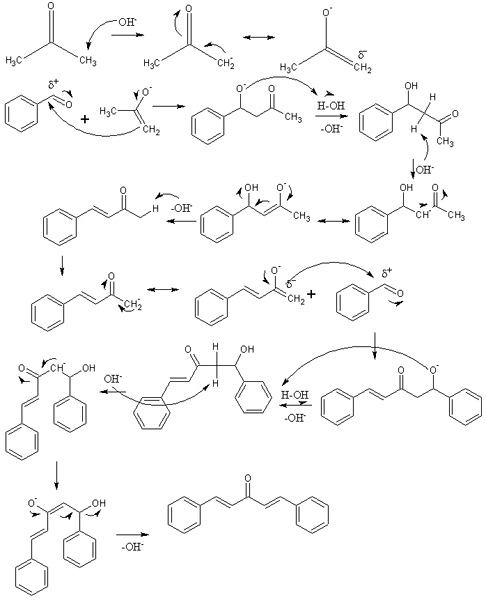 Mechanisme van aldolische condensatie bij de synthese van dibenzalacetona. Bron: Izmaelt [CC BY-S (https: // creativeCommons.Org/licenties/by-sa/3.0)]
Mechanisme van aldolische condensatie bij de synthese van dibenzalacetona. Bron: Izmaelt [CC BY-S (https: // creativeCommons.Org/licenties/by-sa/3.0)] In het superieure beeld hebben we het mechanisme van aldolische condensatie tussen benzaldehyde en aceton weergegeven om het dibenzalaceton te ontstaan; In het bijzonder zijn trans-trans isomeer.
De reactie begint met aceton in basismedium. OH- Uit een zuur proton van een van de twee methylgroepen, -CH3, aanleiding geven tot een ininolie: Cho3C (O) CH2-, die zijn negatieve resonantiebelasting verplaatst (eerste rij van de afbeelding).
Dit inolie werkt dan als een nucleofiel middel: valt de carbonylgroep van een benzaldehyde molecuul aan. De opname in de benzaldehyde genereert een alcoxide, dat omdat het een zeer basale verwoesting van een watermolecuul is en een aldol wordt (tweede rij). Het aldol of β-hydroxychithon wordt gekenmerkt door groepen C = O en OH.
Het basismedium dehydrateert deze aldol en een dubbele binding wordt gevormd in zijn structuur, die de benzylidenaceton genereert (derde rij). Dan, oh- Ook onheruitvoudigd een van zijn zure hydrogenen, die een andere nucleofiele aanval herhaalt op een tweede benzaldehyde -molecuul. Deze keer vindt de aanval zo snel plaats (vierde rij).
Het product vormde een ander watermolecuul en lijdt opnieuw een uitdroging om de OH -groep te elimineren en een tweede dubbele binding te vestigen (vijfde en zesde rijen). Dus en ten slotte treedt Dibenzalacetona voor.
Kan je van dienst zijn: Boyle LawSynthese
Reagentia
De reagentia om de synthese van het dibenzalaceton uit te voeren, zijn de volgende:
- 95% ethanol.
- Nieuw gedistilleerde benzaldehyde van bittere amandelolie.
- NaOH als een basiskatalysator in gedestilleerd water.
De te gebruiken bedragen zijn afhankelijk van hoeveel dibenzalaceton het is bedoeld om te synthetiseren. Er is echter een teveel aan benzaldehyde, omdat een deel ervan is geoxideerd tot benzoëzuur. Het is ook gegarandeerd dat de reactie minder tijd kost en dat het ongewenste benzylidenaceton in mindere mate wordt geproduceerd.
Ethanol fungeert als een oplosmiddel van benzaldehyde, omdat het anders niet zou oplossen in de basisomgeving van NaOH.
Procedure
In een groot neerslagglas wordt ethanol gemengd met benzaldehyde. Dan wordt het basismedium van NaOH toegevoegd tijdens constante magnetische agitatie. In deze stap treedt de cannizzaro -reactie op; Dat wil zeggen, twee benzaldehyde moleculen onevenredig zichzelf in een van benzylalcohol en een andere benzoëzuur, gemakkelijk herkenbaar door zijn karakteristieke zoete geur.
Ten slotte wordt aceton toegevoegd en wordt een half uur verwacht dat de oplossing bewolkt wordt en een geeloranje kleur. Dibenzalacetona zal neerslaan als gevolg van water, dus een aanzienlijk volume water wordt toegevoegd om de volledige neerslag te bevorderen.
Dibenzalacetona filtert in een vacuüm en de geelachtige vaste stof was meerdere keren lava met gedestilleerd water.
Herkristallisatie
 Een herkristalliseerd monster van Dibenzalacetona moet een glans dragen die vergelijkbaar is met die van de kristallen van dit beeld. Bron: Smokefoot [CC BY-SA (https: // creativeCommons.Org/licenties/by-sa/4.0)]
Een herkristalliseerd monster van Dibenzalacetona moet een glans dragen die vergelijkbaar is met die van de kristallen van dit beeld. Bron: Smokefoot [CC BY-SA (https: // creativeCommons.Org/licenties/by-sa/4.0)] Om dibenzalaceton te zuiveren, wordt 95% ethanol of hete ethylacetaat gebruikt, zodat meer zuiverheidskristallen worden verkregen voor elke keer dat de herkristallisatie wordt herhaald. Aldus zal het initiële geelachtige stof worden omgezet in kleine gele kristallen van dibenzalacetona.
Kan u van dienst zijn: benzoëzuur (c6h5cooh)Toepassingen
Dibenzalacetona is een verbinding die niet te veel toepassingen heeft. Vanwege het vermogen om ultraviolet licht te absorberen, wordt het gebruikt bij de formulering van zonnebrandcrème, of een ander product dat de incidentie van UV -stralen, coatings of schilderijen plaagt.
Aan de andere kant wordt dibenzalaceton gebruikt bij de organometallische synthese van het paladium. Het werkt als een binding die de metallic paladiumatomen coördineert, PD0, Om het Tris Complex (Dibenzeacetona) Dipaladio te vormen (0).
Deze organometallische verbinding biedt PD -atomen0 In verschillende organische synthese, dus het gedraagt het zich als een homogene katalysator, omdat het oplost in veel organische oplosmiddelen.
Evenzo is dibenzalacetona als bindmiddel gemakkelijk te vervangen door andere organische bindmiddelen, waardoor de organometallische synthese van het paladium kan ontwikkelen.
Risico's
Wat de risico's betreft, is er niet veel beschikbare informatie die rapporteert over de mogelijke effecten op de gezondheid of het milieu dat kan leiden tot dibenzalaceton. In zijn pure toestand is het een irritante vaste stof voor inname, ademhaling of direct contact met de ogen of huid.
Het is echter blijkbaar niet genoeg irritant, zodat het geen deel kan uitmaken van de formuleringen van zonnebrandmiddelen. Aan de andere kant, zo onoplosbaar in water, is zijn concentratie erin verwaarloosbaar en presenteert zich als een vaste verontreiniging. In die zin is het onbekend hoe schadelijk het is voor de mariene fauna of bodems de troebelheid die veroorzaakt.
Totdat het tegenovergestelde is aangetoond.
Referenties
- Morrison, r. T. en Boyd, R, n. (1987). Organische chemie. 5e editie. Redactionele addison-wesley inter-Amerikaan.
- Carey F. (2008). Organische chemie. (Zesde editie). MC Graw Hill.
- Graham Solomons T.W., Craig B. Friteuse. (2011). Organische chemie. (10e editie.)). Wiley Plus.
- Wikipedia. (2020). Dibenzylidenaceton. Opgehaald uit: in.Wikipedia.borg
- Nationaal centrum voor biotechnologie -informatie. (2020). Dibenzylidenaceton. PubChem -database., CID = 640180. Hersteld van: pubchem.NCBI.NLM.NIH.Gov
- Organische syntheses. (2020). Dibenzalaceton. Opgehaald uit: Orsyn.borg
- Dibenzalaceton door aldol condensatie. Opgehaald uit: Web.Mnstate.Edu
- « Thermische vervuilingskenmerken, gevolgen, voorbeelden
- Jodometrie fundamentals, reacties, algemene procedure, gebruik »

