Specifieke defecten
- 2906
- 122
- Nathan Wiegand
Wat zijn specifieke defecten?
Punctuele defecten zijn onvolkomenheden of onregelmatigheden die worden gepresenteerd in het kristallijne reticulum van een vaste stof, en die de kristallijne structuur van zijn perfecte status afwijken. Er wordt gezegd dat ze geen dimensie hebben (0) omdat het alleen punten van het kristallijne reticulum zijn; Dit punt kan een atoom, ion, molecuul, clusters zijn, enz.
Vaste stoffen bij een temperatuur van 0 K (absolute nul) vertonen perfecte structuren, omdat in theorie de componenten geïmmobiliseerd, bevroren zijn. De atomen worden echter nauwelijks geüpload, om te zeggen, ze beginnen te trillen, die vroeg of laat uiteindelijk buiten hun bijbehorende locaties bewegen.
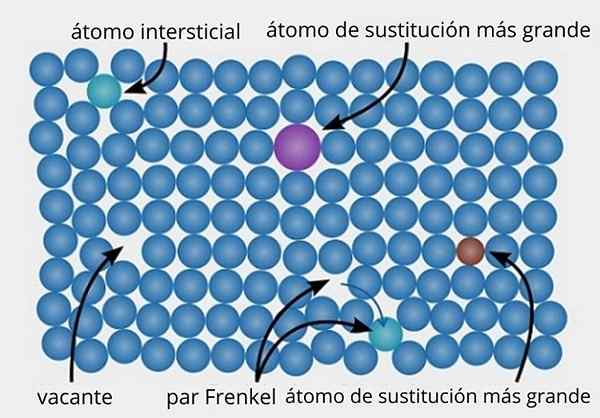
 Weergave van verschillende soorten specifieke defecten gevonden in kristallijne vaste stoffen. Bron: Daniferi, CC BY-SA 3.0, via Wikimedia Commons
Weergave van verschillende soorten specifieke defecten gevonden in kristallijne vaste stoffen. Bron: Daniferi, CC BY-SA 3.0, via Wikimedia Commons Laten we de bovenste afbeelding als een voorbeeld zien. In een geordende en perfecte kristallijne structuur moeten alle blauwachtige punten worden uitgelijnd. Sommige blauwachtige punten kunnen echter afwezig zijn, wat wordt waargenomen door de aanwezigheid van een lege ruimte of een vacature.
Als de vorming van deze vacature te wijten is aan de verplaatsing van een blauwachtig punt van de oorspronkelijke site, hebben we een paar Frenkel, een van de belangrijkste soorten specifieke defecten die bestaan. Het gemobiliseerde blauwachtige punt bevindt zich nu in een interstitiële (groene) positie.
Aan de andere kant kunnen specifieke defecten ook te wijten zijn aan substituties, hetzij door grotere (paarse) atomen of kleinere (bruine) atomen (bruin). We praten over substitutionele specifieke defecten, die vele malen plaatsvinden wanneer onzuiverheden worden geïntroduceerd (geopende) in metaal- en keramische materialen.
Punctuele defecten zijn essentieel om andere defecten te begrijpen die worden geprojecteerd in andere glazen dimensies.
Intrinsieke specifieke defecten
Wanneer een kristallijne structuur altijd wordt gedefinieerd, wordt deze altijd gedaan vanuit idealiteit. Maar in de natuur zijn de defecten onvermijdelijk, hoe klein ze ook zijn. Vaste stoffen hebben dus een natuurlijke aanleg om specifieke defecten in hun structuren te presenteren, waarvan de interactie en sommatie hun chemische en fysische eigenschappen beïnvloeden of wijzigen. De zo -aangedane intrinsieke specifieke defecten vinden plaats in "pure" materialen.
Deze natuurlijke aanleg is te wijten aan thermodynamische en kinetische factoren. De introductie van defecten verhoogt de entropie van de vaste stof, die op zijn beurt toeneemt met de temperatuur. Vervolgens zal bij een bepaalde temperatuur elke vaste stof een status hebben met een minimale configuratie van specifieke defecten.
Naarmate de temperatuur stijgt, zullen er nog meer gebreken zijn, met de maximaal mogelijke hoeveelheid in de buurt van het smeltpunt. Dit alles is logisch als wordt gedacht dat voor hogere thermische trillingen groter de kansen zal zijn dat atomen hun respectieve reticulaire posities verlaten.
Punt extrinsieke defecten
In tegenstelling tot intrinsieke specifieke defecten treden extrinsieke op voor de opname van onzuiverheden. Geen vast van aard is 100% zuiver, dus dit soort defecten zullen zich altijd manifesteren, naast intrinsiek.
Kan u dienen: gluconzuur: structuur, eigenschappen, synthese, gebruikZe rekenen echter een uniek belang en interesse wanneer onzuiverheden opzettelijk worden toegevoegd aan standaardhoeveelheden; We praten over het materiaal dom.
Afhankelijk van de kenmerken van de doponte en het geselecteerde materiaal, worden defecten op een vaste manier in de vaste stof opgenomen, die een impact heeft op de chemische en fysische eigenschappen. Dat is het geval van halfgeleiderformulering, bijvoorbeeld de GaAs.
Aan de andere kant verwijzen extrinsieke specifieke defecten ook op degenen die de samenstelling van materialen of vaste stoffen wijzigen. Dat wil zeggen, ze verliezen hun stoichiometrie om niet -stoichiometrische vaste stoffen te worden.
Punctuele metalen defecten
In metalen hebben we kristallen die in principe elektrische ladingen missen; dat wil zeggen, er zijn geen kationen of anionen aanwezig, maar alleen metaalneutrale atomen. Dus de gebreken die in metalen zouden kunnen zijn, zouden geen invloed hebben op hun neutraliteit, dus geen mechanisme zou geen mechanisme hebben dat dergelijke defecten compenseert.
 Intrinsieke specifieke defecten in kristallen van een hypothetisch metaal. Bron: Gabriel Bolívar.
Intrinsieke specifieke defecten in kristallen van een hypothetisch metaal. Bron: Gabriel Bolívar. In de afbeelding hierboven hebben we een perfect kristal en twee anderen met defecten. Atomen kunnen zich in interstitiële posities bevinden, die de posities van aangrenzende atomen aanstellen en bekend staat als een zelf-interstitieel defect (hieronder in het midden). Ondertussen kunnen sommige atomen hun respectieve plaatsen van de kristallijne opstelling verlaten om vacatures te genereren (rechts).
Daarom is in pure metalen het bestaan van intrinsieke defecten van vacatures en eigenbelang. Hoe meer vacature daar, de dichtheid van de stof neemt af; feit dat in overeenstemming is met de toename van het aantal defecten met de temperatuur.
Wanneer aan de andere kant het metaal met atomen van een ander element wordt gegeven, veroorzaken ze vervangingen of proberen ze zich in de tussenruimten te plaatsen. In dergelijke gevallen neemt de metaaldichtheid toe tot een maximale waarde, waaruit het drastisch begint te dalen.
Specifieke defecten in kristallijne structuren
In kristallijne structuren, die andere vaste stoffen bedekken naast de bovengenoemde metalen, hebben we twee hoofdtypen van specifieke defecten: die van Frenkel en die van Schottky. Beide kunnen voorkomen in dezelfde gebieden van een kristal, en het is ook heel goed mogelijk dat ze samen aanwezig zijn met def -defecten van vacatures of interstitiële beroepen.
Als we het hebben over zouten, oxiden, sulfaten, enz., Er zullen kationen en anionen zijn die een kristal definiëren voor zijn elektrostatische interacties. Daarom, als we een kation elimineren, zullen de negatieve belastingen van de anionen overheersen en zullen het glas negatief worden geladen. Dit is onmogelijk om te gebeuren omdat het het principe van elektroneutraliteit zou schenden.
Aldus genereren de defecten in dit type kristallen elektrische ladingen, die door middel van een mechanisme opnieuw moeten worden gekoppeld. De defecten van Frenkel en Schottky produceren echter niet deze onbalans van elektrische ladingen.
Kan u van dienst zijn: gelijkwaardigheidspuntFrenkel
 Frenkel's punctuele defectrepresentatie. Bron: Gabriel Bolívar.
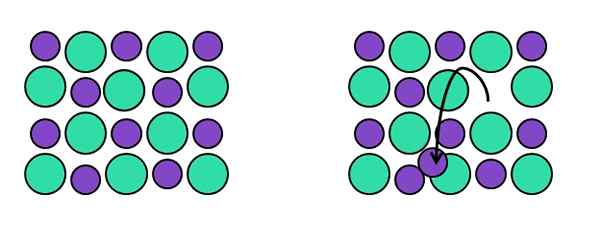
Frenkel's punctuele defectrepresentatie. Bron: Gabriel Bolívar. Farm -Ran -Time Frenkel, ter ere van Yakov Frenkel, verlaat een reticulair punt zijn oorspronkelijke positie om te eindigen in een interstitium. Dat wil zeggen, een atoom, molecuul of ionen gaan door naar een interstitiële positie die een vacature achterlaat.
Zie het voorbeeld van de afbeelding hierboven. Aan de linkerkant hebben we het perfecte kristal bestaande uit twee ionen: één groen, welke ordinarissen van het anion (meer omvangrijk), en een paarse, die het kation wordt (kleiner).
Wanneer een van de paarse kationen hun positie van de kristallijne opstelling verlaat, laat een vacature achter. Let op links de richting waarnaar de zwarte pijl wijst, erop wijzend dat het kation zich nu in een interstitium bevindt.
Omdat het defect van Frenkel bestaat uit kationverplaatsingen (of anionen), blijft het glas neutraal. Ook blijft de samenstelling van het glas constant, omdat in het reticulum de ionen van positie veranderen: ze verlaten het niet, noch voegen anderen eraan toe.
Schottky
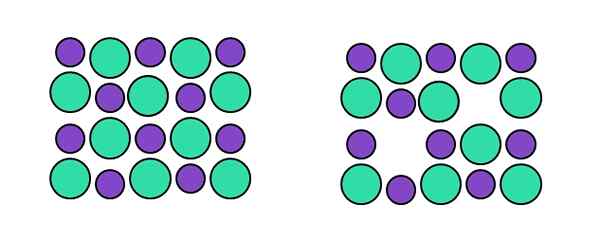 Weergave van het Schottky -defect. Bron: Gabriel Bolívar.
Weergave van het Schottky -defect. Bron: Gabriel Bolívar. In het specifieke Schoottky -type hebben we twee gelijktijdige vacatures: een die overeenkomt met het kation en een andere die overeenkomt met anion. Het gaat bijvoorbeeld niet om een kation om een interstitiële positie te brinque, maar dat het "verdwijnt" vergezeld van een anion (rechts van het bovenste beeld).
Nogmaals, wanneer twee vacatures tegelijkertijd worden gecreëerd, een kationisch (dat zich als een anion zal gedragen), en een anionisch (dat zich als een kation zal gedragen), blijft de samenstelling van het kristal ongewijzigd. Dit is zo zolang dit type defect over is, en geen willekeurige vacatures veroorzaakt door externe of interne agenten.
Van al het bovenstaande wordt geconcludeerd dat de defecten van Frenkel en Shottky intrinsiek punt -tienersstoichiometrische defecten zijn, omdat ze de samenstelling of stoichiometrie van vaste stoffen niet veranderen.
Punctuele defecten in keramische materialen
De keramiek is materialen waarvan het ionenkarakter erg oscillerend is. Sommigen presenteren een duidelijk covalent karakter, zoals bij het silica, SIO2, of met aluminium nituro, aln.
Daarom moeten we twee andere soorten specifieke defecten overwegen die kunnen optreden als een product van de covalente aard van het keramiek: het antisitium en de niet -verzadigde link.
Antisitium
Zoals de naam al doet vermoeden, is het het defect dat optreedt wanneer twee atomen hun van hun site veranderen, in positie zijn in strijd met die van de oorspronkelijke kristallijne reticulum. In de SIC kan het bijvoorbeeld gebeuren dat er C-C of SI-if is waar dat niet zou moeten. Dit type punctuele defect is ook heel gebruikelijk in legeringen:
Kan u van dienst zijn: aluminium fosfuro (AIP): structuur, eigenschappen, gebruik, risico's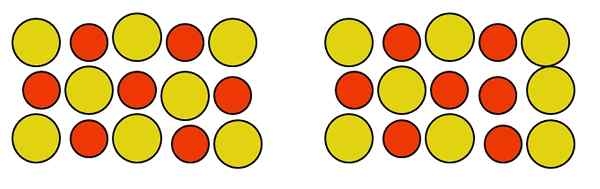 Punctueel antisitiumdefect in een Au-Cu-legering. Bron: Gabriel Bolívar.
Punctueel antisitiumdefect in een Au-Cu-legering. Bron: Gabriel Bolívar. Merk op dat koper- en goudatomen in de Au-How-legering neutraal zijn. Hoe ze zich ook bewegen, de neutraliteit van het glas wordt niet gestoord. Daarom veranderen de twee atomen van plaats in het glas, zoals rechts van de afbeelding hierboven, dit heeft geen invloed op de neutraliteit van de legering.
In keramiek die meer dan één kation hebben, zoals spiners, kunnen twee kationen met gelijke valenties site uitwisselen (bijvoorbeeld naar3+ en Cr3+) zonder de onbalans van elektrische ladingen.
Niet -verzadigde link
De niet -verzadigde schakel (bungelende binding in het Engels) onderbreekt de volgorde in de kristallen van het covalente keramiek, omdat het atoom dat de link vormt afwezig is, waardoor een paar vrije elektronen achterblijft.
In het keramiek worden niet alleen de defecten van anti -itium en niet -verzadigde link gegeven, maar ook alle intrinsieke en extrinsieke defecten, dus het is complex om hun echte, niet perfecte structuren te analyseren.
Voorbeelden van specifieke defecten
Gedurende het artikel zijn enkele voorbeelden van materialen en hun specifieke gebreken genoemd. Vervolgens, en ten slotte, worden andere materialen vermeld, vergezeld van het type defect dat ze meestal aanwezig zijn.
Zilveren halogeniden
Zilveren halogeniden, zoals AgCl of AgBr, presenteren Frenkel -defecten waar het ag -kation+ Het gaat naar interstitiële posities.
Alkaline haluros
De alkalische halogeniden, zoals NaCl, manifesteren Schottky -defecten, waarvan de anionische vacatures zijn gevuld met elektronen wanneer hun kristallen worden verwarmd in aanwezigheid van natrium of metalen kaliumdampen.
Torio dioxide
In de tho2 Het kation th4+ is meer omvangrijk dan anion of2-. Daarom heeft dit oxide een Frenkel -defect waar het O is2- die naar interstitiële posities gaat.
Paladio spons
Het paladium is in staat om waterstof te absorberen, zich gedragen als een spons die ze in de interstitiële posities van hun kristallen behoudt.
Staal
Evenzo zoals gebeurt tussen paladium en waterstof, kan ijzer koolstofatomen opnemen in zijn tussenruimten, wat resulteert in de vorming van staal.
Titaniumlegeringen
Het punctie -defect van de vervanging, hoewel het niet is uitgelegd als de andere defecten, is niets meer dan de vervanging van het ene atoom voor het andere, dat breekt met de bestelling die door het kristal is vastgesteld.
Aldus kunnen atomen van een titaniumkristal worden vervangen door andere atomen (metalen) om een familie van titaniumlegeringen te veroorzaken.
Referenties
- Barry Carter & M. Grant Norton. (2007). Keramische materialen wetenschap en engineering. Springer.
- Shiver & Atkins. (2008). Anorganische scheikunde. (Vierde druk). MC Graw Hill.
- B.S.H. Royce. (S.F.)). Puntdefecten. Hersteld van: Princeton.Edu
- Wikipedia. (2020). Kristallografisch defect. Opgehaald uit: in.Wikipedia.borg
- Nayak, s.K., Opgehangen, c.J., Sharma, V. et al. (2018). Inzicht in puntdefecten en onzuiverheden in titanium uit eerste principes.NPJ Computer MA 4.11. doen.org/10.1038/S41524-018-0068-9
- Byju's. (2020). Puntdefecten. Hersteld van: byjus.com

