Citocroma C oxidasestructuur, functies, remmers
- 4028
- 988
- Ernesto McKenzie
De Citocroma C oxidase Het is een enzymatisch eiwitcomplex dat de lipide dubbellaag van het celmembraan kan kruisen. Het is dat we voornamelijk zijn geassocieerd met het interne membraan van de mitochondriën, die beide zijn in prokaryotische organismen (bacteriën), zoals in eukaryoten (eencellig en multicellulair).
Ook wel complex IV genoemd, dit enzym is van vitaal belang in de aerobe metabole functies van de organismen, omdat het essentieel is in de elektronentransportketen waarin de cel suikers verbrandt en een deel van de vrijgegeven energie vangt om adenosine -tryposfaat of ATP op te slaan.
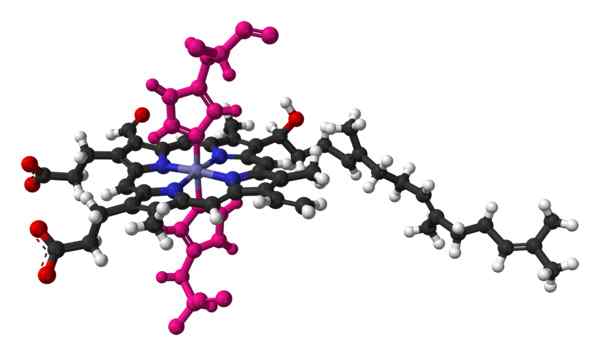
 Bola en Palo -model van het hemo, van een molecuul gevonden in de kristallijne structuur van cytochroom C -oxidase van het runderhart. Genomen en bewerkt uit: Benjah-bmm27 [Public Domain].
Bola en Palo -model van het hemo, van een molecuul gevonden in de kristallijne structuur van cytochroom C -oxidase van het runderhart. Genomen en bewerkt uit: Benjah-bmm27 [Public Domain]. De cytochrome naam betekent "celpigmenten". Dit zijn bloedeiwitten die elektronen transporteren. De cytochromen werden ontdekt door de Ierse dokter Charles Alexander MacMunn in 1884. MacMunn was een pionier in het ontdekken van het ademhalingspigment van het bloed, vandaag Cytochrome genoemd 1.
In de jaren 20 van de vorige eeuw Russische entomoloog en parasitoloog. Hoewel MacMunn ze in 1884 had ontdekt, was de wetenschappelijke gemeenschap vergeten en zelfs sommigen hadden hun werk verkeerd begrepen.
[TOC]
Algemene karakteristieken
Over het algemeen hebben ademhalingspigmenten kenmerkende zichtbare spectra. Het is bekend dat er ten minste vier uitgebreide membraaneiwitcomplexen zijn waar 5 verschillende soorten cytochromen zijn: A, A3, B, C1 en C, geclassificeerd volgens de golflengten van spectrale absorptiemaxima.
Ze worden meestal gevonden in het interne membraan van mitochondria. Ze zijn echter ook waargenomen in het endoplasmatische reticulum en chloroplasten, in eukaryotische en prokaryotische organismen.
Ze presenteren de hemo prothetische groep met ijzer (geloof). Elk van de bekende cytochromen werkt in multienzimatische complexen bij het transport van elektronen van de ademhalingsketen.
Cytochromen hebben de functie van deelname aan oxide-reductiereacties. Reductiereacties, waarbij ze elektronen accepteren, komen anders voor voor elk type cytochroom en hun waarde wordt bepaald door de stroom van de elektronen van de ademhalingsketen.
-Cytochroom c
Er zijn vier soorten cytochroom C bekend, die de volgende zijn.
Klasse I
Binnen deze klasse zijn de cytochromen C -oplosmiddelen van lage beurt (lowspin), aanwezig in bacteriën en mitochondria. Het zijn octaëralen. De hemo -vakbondsplaats bevindt zich aan het einde van de histidine en het zesde ligand wordt geleverd door een metionineresidu aan het einde C.
Uit deze klasse kunt u zelfs verschillende subklassen herkennen, die zijn vastgesteld dat hun drie -dimensionale structuur is.
Klasse II
In deze klasse zijn er cytocromen C van hoge beurt (highspin) en wat lage beurt. De hoge bocht is de bindingsplaats dicht bij de end-C, en in mensen met een lage bocht lijkt het zesde ligand een metionineresidu in de buurt van het N-Termus-einde in het Engels). Ze zijn pentacoonineerd met vijfde ligand histidine.
Kan u van dienst zijn: turgiteit (biologie)Klasse III
Deze klasse wordt gekenmerkt door cytochromen C met meerdere Hemo (C3 en C7) en een lage potentiële oxide-reductor, met slechts 30 aminozuurresten per hemo. In de vertegenwoordigers van deze klasse hebben de Hemo C -groepen structuur en niet -equivalente functies, naast het presenteren van verschillende redox -potentialen. Het zijn octaëralen.
Klasse IV
Volgens sommige auteurs is deze klasse alleen gemaakt om complexe eiwitten op te nemen die worden gepresenteerd door andere prothetische groepen, evenals Hemo C of flavocytocrome C, onder andere.
De cytochrome C -oxidase of complex IV
Het cytochroom C -oxidase is een mitochondriaal enzym dat de uiteindelijke fase van elektronisch transport in cellulaire ademhaling uitvoert. Dit enzym katalyseert elektrontransport van gereduceerde cytochroom C naar zuurstof.
Sommige chemische verbindingen zoals cyanide, koolstofdioxide en azid. Andere vormen van remming van het IV -complex zijn genetische mutaties.
Vanuit het evolutionaire oogpunt wordt cytochroom C -oxidase alleen gevonden in aerobe organismen, en verschillende groepen wetenschappers suggereren dat de aanwezigheid van dit eiwit evolutionaire relaties aangeeft waar planten, schimmels en dieren ook een voorouder gemeen hebben.
Structuur
De cytochroom C -oxidase vormt een homodimeer complex, dat wil zeggen uit twee vergelijkbare monomeren in het interne membraan van de mitochondria. Het enzymatische complex bestaat uit 3 tot 4 subeenheden in prokaryotische organismen en maximaal 13 (sommige suggereren 14) polypeptiden in organismen zoals zoogdieren.
In deze organismen zijn 3 polypeptiden van mitochondriale oorsprong en de rest is ontstaan in de kern. Elk monomeer heeft 28 transmembraan propellers die hydrofiele domeinen scheiden van de membraanmatrix en intermembraanruimte.
Het heeft slechts één katalytische eenheid, die wordt aangetroffen in alle enzymen die oxidatie/reductiereacties katalyseren, met behulp van moleculaire zuurstof (oxidasen, vooral hemo-cobre). Het complex bevat cytochromen A en A3 verenigd door subeenheid I en twee kopercentra.
Het presenteert een of meerdere Hemo C -groepen gekoppeld aan de omringende eiwitstructuur door een of meer (in het algemeen twee) tioreter -links. Andere auteurs suggereren dat er een enkele Hemo C -groep is gekoppeld aan het eiwit tussen de porfyrine -ring en twee cysteïneresten.
De enige hierboven genoemde Hemo C -groep is omgeven door hyodrofoob afval en is hexacoordininated, omdat histidine in positie 18 van de polypeptideketen en methodine in 80.
Kan u van dienst zijn: plantencel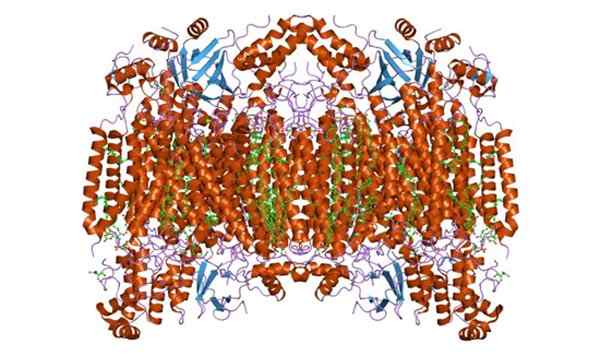 Cytochrome C oxidase -subeenheid F. Genomen en bewerkt uit: Jawahar Swaminathan en MSD -personeel van het European Bioinformatics Institute [Public Domain]
Cytochrome C oxidase -subeenheid F. Genomen en bewerkt uit: Jawahar Swaminathan en MSD -personeel van het European Bioinformatics Institute [Public Domain] Functie
Citocroma C -oxidasen zijn protagonisten in drie primaire fysiologische mechanismen, die we hieronder zullen zien.
Apoptose of geprogrammeerde celdood
Apoptose is de vernietiging of geprogrammeerde celdood, veroorzaakt door hetzelfde organisme en die is bedoeld om de groei, ontwikkeling, eliminatie van beschadigde weefsels en de regulatie van het immuunsysteem te beheersen. In dit fysiologische proces neemt het cytochroom C -oxidase deel als intermediair.
Dit eiwit, vrijgegeven door mitochondria, leidt tot een interactie met het endoplasmatisch reticulum, dat de secretie of afgifte van calcium veroorzaakt. De progressieve toename van calcium veroorzaakt een massale afgifte van cytochroom C -oxidase, totdat het mogelijk is om cytotoxische niveaus van calcium te bereiken.
Cytotoxische calciumspiegels en de afgifte van cytochromen C veroorzaken cascade -activering van verschillende enzymen, die verantwoordelijk zijn voor de vernietiging van cellen.
Cel- of weefselregeneratie
Verschillende studies geven aan dat wanneer cytochroom C -oxidase wordt blootgesteld aan golflengten van 670 nanometers, deelneemt aan een functioneel complex, dat beschadigd of gewond weefsel doordringt en de snelheid van de celregeneratie verhoogt.
Energiemetabolisme
Dit is misschien wel de bekendste en meest relevante functie van cytochroom C -oxidase. Het is precies het oxidasecomplex (van de ademhalingsketen) dat op lading van het verzamelen van de elektronen van de cytochroom C en ze naar het zuurstofmolecuul overbrengt, waardoor het wordt gereduceerd tot twee watermoleculen.
Verbonden met dit proces, is er een translocatie van protonen door het membraan, wat resulteert in het genereren van een elektrochemisch gradiënt dat het ATP -synthesase -complex gebruikt om ATP te produceren of te synthetiseren (Adenosín Triffisphyte).
Remmers
Citocroma C -oxidase wordt geremd door verschillende chemische processen en verbindingen. De manier waarop het zich voordoet, kan ontstaan als een natuurlijke manier om de productie of werking van het enzym te reguleren of kan per ongeluk optreden als gevolg van vergiftiging.
In aanwezigheid van azid. Dit veroorzaakt een onderbreking van het cellulaire ademhalingsproces en veroorzaakt daarom de chemische verstikking van cellen.
Andere verbinding zoals stikstofoxide, waterstofsulfide, methanol en sommige gemethyleerde alcoholen veroorzaken ook cytochroom C -oxidaseremming.
Tekort
De cytochroom C -oxidase is een enzym dat wordt geregeld door genen van zowel de kern als de mitochondria. Er zijn genetische veranderingen of mutaties die een tekort aan cytochroom C -oxidase kunnen dragen.
Deze mutaties verstoren de functionaliteit van het enzym, omdat ze hun enzymatische structuur veranderen, waardoor ze metabole aandoeningen met zich meebrengen tijdens de embryonale ontwikkeling (volgens studies bij mensen), die later het organisme zullen beïnvloeden in hun eerste levensjaren.
Kan u van dienst zijn: dendritische cellen: kenmerken, functie, typenCytochroom C -oxidasedeficiëntie beïnvloedt weefsels met een hoge energievraag, zoals hart, lever, hersenen en spieren. De symptomen van deze mutaties worden weerspiegeld vóór de twee jaar van het leven en kunnen zich manifesteren als sterke of milde aandoeningen.
Milde symptomen kunnen zelfs kort na het eerste jaar oud worden gezien en meestal hebben personen met hen slechts een afname van spierspanning (hypotonie) en spieratrofie (myopathie).
Aan de andere kant kunnen individuen met sterkere symptomen spieratrofie en encefalyopathie hebben. Andere aandoeningen veroorzaakt door de afwezigheid van cytochroom C -oxidase zijn hypertrofische myocardiopathie, pathologische toename van de levergrootte, leight -syndroom en melkzuurzuur.
Gebruik in fylogenie
Fylogenie is de wetenschap die verantwoordelijk is voor de studies van oorsprong, training en evolutionaire ontwikkeling vanuit het standpunt van de voorouder-afnemende organismen, van organismen. In de afgelopen decennia zijn fylogenie -onderzoeken met moleculaire analyse in toenemende mate frequent geweest, veel informatie gooien en taxonomische problemen oplossen.
In deze zin geven sommige fylogenetische studies aan dat het gebruik van cytochroom C -oxidasen kan helpen bij het tot stand brengen van evolutionaire relaties. Dit komt omdat dit eiwitcomplex sterk bewaard is en aanwezig is in een breed scala aan organismen, variërend van eencellige protisten tot grote gewervelde dieren.
Voorbeeld hiervan zijn de tests gedaan met mensen, chimpansees (Broodbrood) en resus makaken (Mulatta Macaca)). Dergelijke tests onthulden dat cytochroom C -oxidasemoleculen van mensen en chimpansees identiek waren.
Hij toonde ook aan dat de cytochroom C -oxidasemoleculen van de resusmakaak.
Referenties
- R.P. Ambler (1991). Sequentievariatie in bacteriële cycromen C. Biochimica et Biophysica Acta (BBA) - Bio -energetics.
- Cytochroom c. Hersteld van Newworldyclopedia.borg.
- V.Colman, E. Kosten. Chaves, V. Tortora (2015). Biologische rollen van cytochroom C: mitochondriaal elektronisch transport, geprogrammeerde celdood en AUS -activiteitstoename. Annals van de Faculteit der Geneeskunde.
- Cytochrome C oxidase -subeenheid I. Hersteld van EBI.AC.Uk.
- L. Youfen, p. Jeong-Oon, D. Jian-Hong & B. Yidong (2007). Cytochroom C oxidase -subeenheid IV is essentieel voor de assemblage- en ademhalingsfunctie van het enzymcomplex. Journal of BioEnergetics and Biomembranes.
- Genengroep: Complex IV Mitochondriaal: Cytochrome C-oxidase-subeenheden (COX, MT-CO). Hersteld uit genenames.borg.
- EN.F. Hartree (1973). De ontdekking van cytochroom. Biochemisch onderwijs.
- Citocroma C oxidase, tekort aan .. . Hersteld van Ivami.com.
- C.K. Mathews, k.EN. Van Hold & K.G. Ahern (2002). Biochemerie. 3e editie. Benjamin / Cummings Publishing Company, Inc.
- « Opotillo -kenmerken, habitat, eigenschappen en ongedierte
- Pinus Patula -kenmerken, habitat, taxonomie, gebruik, ongedierte »

