Wijnsteenzuur
- 2401
- 598
- Cecil Graham
We leggen uit wat wijnsteenzuur is, zijn fysische en chemische eigenschappen, zijn structuur en zijn toepassingen
Wat is wijnsteenzuur?
Hij wijnsteenzuur Het is een organische verbinding waarvan de moleculaire formule COOH (CHOH) is2COOH. Het heeft twee carboxylgroepen; Dat wil zeggen, je kunt twee protonen vrijgeven (h+)). Met andere woorden, het is een diprotisch zuur. Het kan ook worden geclassificeerd als een aldarinezuur (zuursuiker) en een derivaat van het succininezuur.
Het zout is bekend sinds onheuglijke tijden en vormt een van de secundaire producten van wijnuitwerking. Het wordt gekristalliseerd als een wit sediment gedoopt als "wijndiamanten", die zich ophopen in de kurk of op de bodem van de vaten en flessen. Dit zout is kalium biitaratraat (of kaliumzuur tartrato).
Wijnsteenzuur zouten hebben gemeen de aanwezigheid van één of twee kationen (na+, K+. NH4+, AC2+, enz.) Omdat het door zijn twee protonen vrij te geven, het negatief geladen blijft met een lading van -1 (zoals bij de biterrato -zouten) of -2.
Op zijn beurt is deze verbinding het onderwerp geweest van studie en onderwijs van organische theorieën die verband houden met optische activiteit, meer precies met stereochemie.
Waar is wijnsteenzuur?
Tartaarszuur is een onderdeel van vele planten en voedsel, zoals abrikoos, avocado's, appels, tamarindos, zonnebloempitten en druiven.
Tijdens het verouderen van de wijnen wordt dit zuur - tot koude temperaturen - gecombineerd met kalium om te kristalliseren als Tartrato. In rode wijnen is de concentratie van deze Tartrats minder, terwijl ze in witte wijnen overvloediger zijn.
Tartraten zijn zouten van witte kristallen, maar wanneer ze onzuiverheden van de alcoholische omgeving afsluiten, verwerven ze roodachtige of paarse tonen.
Kan u van dienst zijn: verplaatsingsreactieWijnsteenzuurstructuur
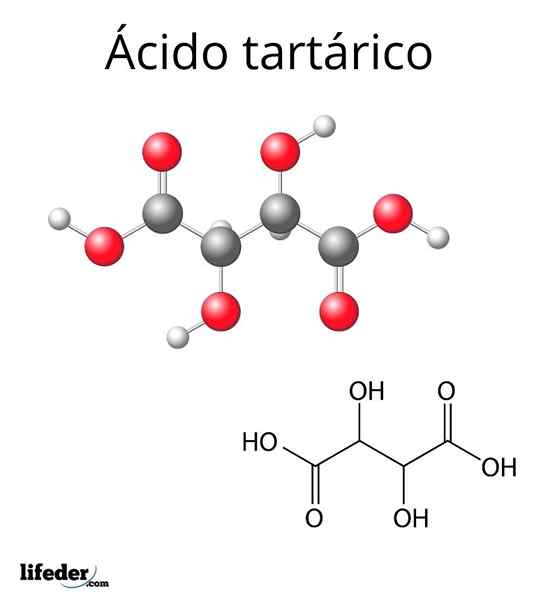
 Moleculaire structuur van wijnsteenzuur
Moleculaire structuur van wijnsteenzuur De moleculaire structuur van wijnsteenzuur wordt weergegeven in het bovenste beeld. De carboxylgroepen (-COOH) bevinden zich aan de zijkant en worden gescheiden door een korte twee koolstofketen (C2 en C3)).
Op zijn beurt is elk van deze koolstofatomen gekoppeld aan een H (witte bol) en een OH -groep. Deze structuur kan de C -link draaien2-C3, dus het genereren van verschillende conformaties die het molecuul stabiliseren.
Dat wil zeggen, de centrale link van het gebroken molecuul als een roterende cilinder, die op de hoogte is van de ruimtelijke dispositie van de groepen -cooh, h en oh (Newman -projecties).
Bijvoorbeeld, in de afbeelding wijzen de twee OH -groepen in tegengestelde richtingen, wat betekent dat ze zich in anti -posities met elkaar bevinden. Hetzelfde geldt voor groepen -COOH.
Een andere mogelijke conformatie is die van een paar overschaduwde groepen, waarin beide groepen in dezelfde richting zijn georiënteerd. Deze conformaties zouden geen belangrijke rol spelen in de structuur van de verbinding als alle koolstofatomen groepen C2 en C3 Ze waren hetzelfde.
Zoals in deze compound zijn de vier groepen verschillend (-cooh, oh, h en de andere kant van het molecuul), zijn koolstoffen asymmetrisch (of chirals) en vertonen de beroemde optische activiteit.
De manier waarop groepen in koolstofatomen zijn gerangschikt2 en C3 van wijnsteenzuur bepaalt enkele verschillende structuren en eigenschappen voor dezelfde verbinding; dat wil zeggen, staat het bestaan van stereoisomeren toe.
Tartarkezuurtoepassingen
In de voedingsindustrie
Het wordt gebruikt als een eulse -stabilisator in bakkerijen. Het wordt ook gebruikt als een ingrediënt voor gist, jam, gelatine en frisdranken. Het vervult ook functies als een verzurend, bibliotheek en bieder van ionen.
Het kan u van dienst zijn: natriumbromide (NABR)Tartarinezuur wordt gevonden in deze voedingsmiddelen: zoete koekjes, snoepjes, chocolaatjes, gasvormige vloeistoffen, bakkerijproducten en wijnen.
In de uitwerking van de wijnen wordt het gebruikt om ze meer evenwichtig te maken, vanuit het smaakpunt, door de pH hiervan te verlagen.
In de farmaceutische industrie
Het wordt gebruikt bij het creëren van pillen, antibiotica en bruisende pillen, evenals in medicijnen die worden gebruikt bij de behandeling van hartaandoeningen.
In de chemische industrie
Het wordt gebruikt in fotografie, evenals in galvanotechniek en is een ideale antioxidant voor industriële vetten.
Het wordt ook gebruikt als een metaalionen ontvoerder. Als? Hun banden op een zodanige manier roteren dat u de zuurstofatomen van de carbonylgroep, rijk aan elektronen, rond deze positief geladen soorten kunt vinden.
In de bouwsector
Vertrek het proces van het verharden van het gips, cement en gips, waardoor de manipulatie van deze materialen efficiënter wordt.
Tartarinezuurseigenschappen

De meest voorkomende wijnsteenzuurtoepassingen zijn:
- Tartaarse zuur wordt op de markt gebracht in de vorm van kristallijn poeder of enigszins ondoorzichtige witte kristallen. Het heeft een aangename smaak, en deze woning is een indicatie van een wijn van goede kwaliteit.
- Smelt bij 206 ºC en brandt bij 210 ºC. Het is erg oplosbaar in water, alcoholen, basisoplossingen en borax.
- De dichtheid is 1,79 g/ml bij 18 ºC en presenteert twee zuurgraadconstanten: PKA1 en PKA2. Dat wil zeggen, elk van de twee zure protonen heeft zijn eigen neiging om zichzelf te bevrijden in de waterige omgeving.
- Net als -coh- en OH -groepen, kan het worden geanalyseerd door infraroodspectroscopie (IR) voor hun kwalitatieve en kwantitatieve bepalingen.
- Andere technieken zoals massaspectroscopie en nucleaire magnetische resonantie, maken de vorige analyse van deze verbinding mogelijk.
Stereochemie

Tartaarszuur was de eerste organische verbinding waarmee een enantiomere resolutie werd ontwikkeld. Wat betekent dit? Het betekent dat de stereoisomeren handmatig kunnen worden gescheiden dankzij het onderzoekswerk van de biochemist Louis Pasteur, in 1848.
En wat zijn de stereoisomeren van wijnsteenzuur? Dit zijn: (r, r), (s, s) en (r, s). R en S zijn de ruimtelijke configuraties van koolstofatomen C2 en C3.
Wijnsteenzuur (r, r), het meest "natuurlijke", roteert het gepolariseerde licht rechts; Wijnsteenzuur (s, s) wordt links gebroken, in tegenstelling tot de kloknaalden. En ten slotte breken wijnsteenzuur (R, S) het gepolariseerde licht niet, die optisch inactief zijn.
Louis Pasteur, met behulp van een microscoop en een pincet, gevonden en gescheiden wijnsteenzuurkristallen die "rechts" en "links -gehandte" patronen toonden, zoals in het superieure beeld.
Op deze manier zijn de "rechtse" kristallen die gevormd door de enantiomeer (r, r), terwijl de "links -gehandte" kristallen die van de enantiomeer (s, s) zijn.
De kristallen van wijnsteenzuur (R, S) verschillen echter niet van anderen, omdat ze tegelijkertijd bekwame en linkse kenmerken vertonen; Daarom konden ze niet worden "opgelost".
Referenties
- Wikipedia. (2018). Wijnsteenzuur. Opgehaald van.Wikipedia.borg
- Pubchem. (2018). Wijnsteenzuur. Hersteld van PubChem.NCBI.NLM.NIH.Gov.
- Wijn begrijpen tarteert. Hersteld van Jordanwinery.com
- Actief. Wijnsteenzuur. Hersteld van Actipedia.borg
- Pochteca. Wijnsteenzuur. Pochteca hersteld.com.mx
- Dhanesshwar Singh et al. (2012). Over de oorsprong van de optische inactiviteit van meso-tartarinezuur. Afdeling Chemie, Manipur University, Canchipur, Imphal, India. J. Chem. Apotheker. Rundvlees., 4 (2): 1123-1129.

