Gluconzuurstructuur, eigenschappen, synthese, gebruik
- 2861
- 49
- Glen Armstrong
Hij Gluconzuur Het is een organische verbinding die biochemisch optreedt door de oxidatie van glucose door het oxidase -glucose -enzym. Aanvankelijk wordt glucone-Δ-lactone gevormd, dat vanwege de werking van het lactase-enzym, of spontaan, transformeert in gluconzuur.
Gluconzuur is een niet -toxische verbinding die aanwezig is in honing, wijn, fruit, enz. Het wordt de zure versie van glucose. Het is erg oplosbaar in water en in het algemeen weinig oplosbaar in organische oplosmiddelen.

Glyconzuur werd ontdekt door Hlasiwetz en Habermann, in 1870, door glucose te oxideren met chloor. Tientallen jaren later, in 1922, bepaalde Molliard de aanwezigheid van gluconzuur in een kweekmedium van de sterigmatocystis nigra fungus, nu bekend als een. Niger.
De belangrijkste industriële vorm van de productie van gluconzuur is de ondergedompelde gisting van glucose gemedieerd door de schimmel tot. Niger. Bacteriën van het geslacht Pseudomonas worden echter ook gebruikt bij de fermentatie van glucose, en gerelateerde genres zoals Gluconobacter, Acetobacter, enz.
[TOC]
Gluconzuurstructuur
 Verschillende representaties voor het gluconzuurmolecuul. Bron: Yikrazuul / Public Domain.
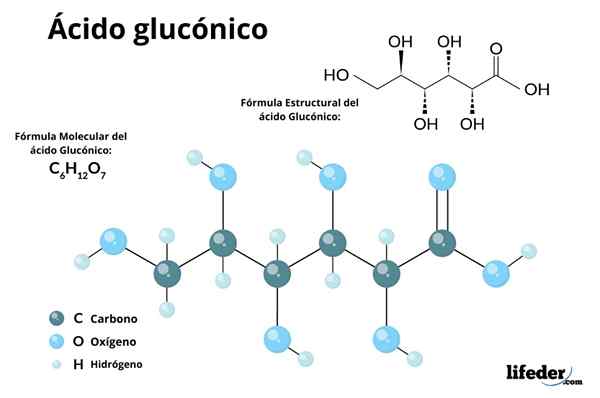
Verschillende representaties voor het gluconzuurmolecuul. Bron: Yikrazuul / Public Domain. Het eerste beeld toonde de structurele formule voor de open gluconzuurketen. Maar net als glucose sluit het molecuul van dit zuur af om een piranosring te vormen, zoals weergegeven in het superieure beeld door verschillende modellen of projecties. Van links naar rechts: Tollens, Haworth, voorzitter en absolute stereochemische projectie.
Merk op hoeveel het lijkt op glucose, met het enige verschil dat het einde -ch2Oh heeft roesten aan -cooh; Dat wil zeggen, het is opgehouden een alcohol te zijn om te transformeren in een carbonzuur. Dit extreme is degene die wordt geschonken door de ion h+ en definieert daarom de zuurgraad van gluconzuur.
Kan u van dienst zijn: ethyletherEigenschappen
Chemische formule
C6H12OF7
Molaire massa
196,155 g/mol
Fysiek uiterlijk
Kleurloze of licht gele kristallen. Evenzo, wanneer het oplost, genereert het een kleurloze vloeistof met geelachtige kleuringen, waarvan de consistentie die van een siroop is.
Smaak
Enigszins zuur.
Smeltpunt
131 ºC. Boven deze temperatuur begint af te breken om koolstofdioxide af te geven, daarom wordt het kookpunt niet overtuigend gerapporteerd.
Oplosbaarheid in water
316 g/l A 25 ºC
Oplosbaarheid in andere oplosmiddelen
Enigszins oplosbaar in alcohol, maar onoplosbaar in ether en in veel organische oplosmiddelen.
Dikte
1,23 mg/ml
Octanol/waterpartitiecoëfficiënt
Log p = - 1,87 (geschat)
Dissociatie constant
Ka = 2,5 · 10-4 bij 25 ºC
Zuurgraad (PKA)
3.6 tot 25 ºC
Brekingsindex
1.4161
Gluconzuursynthese
Synthese- of productiemethoden van gluconzuur kunnen worden geclassificeerd als chemische methoden en biologische methoden.
Chemische methoden
Onder deze methoden hebben we het volgende:
-Chemische oxidatie van glucose door een hypochlorietoplossing.
-Hydrolyse van a-D-glucose met een mengsel van bromide en zwavelzuur.
-Bestraling van D-glucose met straling van het gamma-type.
De Cannizaro -reactie toegepast op glucose, in alkalische omstandigheden, is de sorbitolverbindingen en gluconzuur afkomstig. Gluconzuur kan ook worden gesynthetiseerd, direct oxideren van glucose in aanwezigheid van de paladiumkatalysator.
Biologische methoden
Glucosefermentatie voor gluconzuursynthese wordt gebruikt, uitgevoerd door filamenteuze schimmels, zoals een. Niger, of door bacteriën van verschillende genres, waaronder pseudomonas en Zymomonas.
De aanwezigheid van gluconzuur in een kweekmedium. Niger, uit Molliard in 1922, leidde ertoe dat de gisting van glucose door de actie van de schimmel tot. Niger kan een handige methode voor productie zijn, dit zoete zuur. In feite gebruikt deze methode momenteel.
Het kan u van dienst zijn: de 20 soorten chemie en hun weigeringDe voorwaarden van de cultuur van. Niger voor glucosefermentatie omvat: een hoge opgeloste zuurstofconcentratie en een pH tussen 5,5 en 6,5. Deze pH blijft in dit interval door aggregatie van calciumcarbonaat als een neutraliserend middel.
De concentratie van glucose in het gewas is hoog (110-250 g/l), terwijl de concentratie van stikstof en fosfor laag is (< 20 mmol/L). Asimismo, se necesita una baja concentración de iones metálicos. Siguiendo estas condiciones, la fermentación de la glucosa es completada en un 90% en menos de 24 horas.
Toepassingen
Artsen en dierenartsen
Gluconzuur is een onmisbaar reagens voor het verkrijgen van calciumgluconaat. Dit zout wordt gebruikt bij de behandeling van patiënten met een hypocalciëmie. Ook wordt het in de vorm van gel gebruikt bij de behandeling van brandwonden geproduceerd door hydrofiezuur.
Aan de andere kant wordt kinine gluconaat gebruikt bij de behandeling van malaria. Evenzo is ijzergluconaat gebruikt bij de behandeling van ferropenische anemieën.
Hoe dan ook, gluconzuur is een basistreagens voor de formulering van veel gluconaatzouten medicijnen.
Schoonmaak
Glyconzuur en zijn zouten hebben een chelerende actie, zodat ze metalen kunnen vangen, zoals ijzer, koper, aluminium, lanthean, onder andere. Deze woning maakt het gebruik ervan in industriële en binnenlandse schoonmaakmiddelen.
Calciumgluconaat, vanwege de eigenschap van het vormen van complexen met verschillende metalen, wordt gebruikt om metaaloxiden uit metalen oppervlakken te verwijderen of om lakken en objecten van objecten te verwijderen. Gluconzuur en zouten worden ook gebruikt in flessenspoelingsformuleringen.
Kan u van dienst zijn: chiraliteitNatriumgluconaat wordt in veel wasmiddelen gebruikt als metaalbevestiging. Gluconzuur, en verschillende van zijn zouten, worden gebruikt in de bruinings- en textielindustrie, vooral met betrekking tot het reinigen van zijn producten, vooral worden gebruikt bij de eliminatie van metaalafzettingen.
Voedsel
Glyconzuur wordt gebruikt als een gistgezel, in mengsels voor het bereiden van cakes, en als een zuurcomponent in droge mengdesserts. Glucone-Δ-lactone wordt in de voedingsindustrie gebruikt als een zacht zuurstof.
Gluconzuur voorkomt troebelheid bij drankjes en klontvorming vanwege de aanwezigheid van calciumverbindingen. Verbetert de smaak van voedsel en verleent ze een bitterzoete smaak, terwijl ze ook helpt bij het beheersen van de bitterheid die er in sommige van hen aanwezig is.
Andere gebruiken
Een gluconaat werkt als een vertraging van het betonnen instellingsproces, dat de nodige tijd mogelijk maakt voor een correcte lediging van beton, waardoor de productie van hoge temperaturen wordt vermeden die scheurenvorming kunnen veroorzaken.
En ten slotte worden gluconzuur en sommige van zijn zouten gebruikt als componenten van sommige celkweekmedia.
Referenties
- Morrison, r. T. en Boyd, R, n. (1987). Organische chemie. 5e editie. Redactionele addison-wesley inter-Amerikaan.
- Carey F. (2008). Organische chemie. (Zesde editie). MC Graw Hill.
- Graham Solomons T.W., Craig B. Friteuse. (2011). Organische chemie. (10e editie.)). Wiley Plus.
- Wikipedia. (2020). Gluconzuur. Opgehaald uit: in.Wikipedia.borg
- Nationaal centrum voor biotechnologie -informatie. (2020). Gluconzuur. PubChem -database., CID = 10690. Hersteld van: pubchem.NCBI.NLM.NIH.Gov
- Elsevier B.V. (2020). Gluconzuur. Wetenschappelijk. Opgehaald uit: Scientedirect.com
- Anastassiadis, s. et al. (2006). Continue gluconzuurproductie door aureobasidium pullulans met en zonder biomassa -retentie. [PDF]. Electronic Journal of Biotechnology ISSN: 0717-3458. Pontificale katholieke Universiteit van Valparaíso, Chili.
- « De 10 meest populaire Chileense legendes
- Biot-Savart Law-formule, demonstratie, toepassingen, oefeningen »

