Zure anhydriden hoe worden gevormd, toepassingen en voorbeelden

- 3964
- 1002
- Glen Armstrong
De Zure anhydriden Ze worden als van groot belang geacht bij de grote verscheidenheid aan verbindingen van organische oorsprong die bestaan. Deze worden gepresenteerd als moleculen met twee zure groepen (organische substituenten waarvan de formule RCO is, waarbij r een koolstofketen is) verenigd met hetzelfde zuurstofatoom.
Er is ook een klasse zure anhydriden die vaak wordt gevonden: carbonbonanhydriden, genoemd omdat het startzuur een carbonzuur is. Om die van dit type te benoemen waarvan de structuur symmetrisch is, moet alleen een vervanging van termen worden gemaakt.

De zure expressie moet worden vervangen in de nomenclatuur van het oorspronkelijke carbonzuur door de anhydride -term, wat "zonder water" betekent, zonder de rest van de naam van het gevormde molecuul te wijzigen. Deze verbindingen kunnen ook worden gegenereerd op basis van een of twee zure groepen van andere organische zuren, zoals fosfonzuur of sulfonzuur.
Evenzo kunnen zuuranhydriden worden veroorzaakt op basis van een anorganinezuur, zoals fosforzuur. De fysische en chemische eigenschappen ervan, de toepassingen en andere kenmerken zijn echter afhankelijk van de uitgevoerd synthese en de anhydride -structuur.
[TOC]
Hoe worden zure anhydriden gevormd?
Sommige zuuranhydriden zijn afkomstig van verschillende manieren, hetzij in het laboratorium of in de industrie. In industriële synthese wordt azijnzuuranhydride als een voorbeeld genomen, dat voornamelijk wordt geproduceerd door het carbonilatieproces van het methylacetaatmolecuul.
Een ander voorbeeld van deze synthese is dat van anhydride maleico, dat wordt gegenereerd door de oxidatie van het benzeenmolecuul of butaan.
Het kan u van dienst zijn: zinkhydroxide (Zn (OH) 2)In de synthese van zuuranihydriden in het laboratorium wordt de nadruk echter gelegd op de uitdroging van de overeenkomstige zuren, zoals de productie van het ethanische anhydride, waarbij twee moleculen van ethainezuur worden gedehydrateerd om aanleiding te geven tot de genoemde verbinding.
Een intramoleculaire uitdroging kan ook optreden; Dat wil zeggen, binnen hetzelfde molecuul van een zuur met twee carboxyl (of dicarbonylische) groepen, maar als het tegenovergestelde optreedt en een zuuranhydride hydrolyse lijdt, wordt de regeneratie van de zuren die het ontstaan,.
Zure anhydriden waarvan de acylsubstituenten gelijk zijn, terwijl in anhydriden van dit type als gemengd worden beschouwd, zijn deze moleculen verschillend verschillend.
Deze soorten worden echter ook gegenereerd wanneer een reactie optreedt tussen een zure halur (waarvan de algemene formule een (rcox)) is met een carboxylaatmolecuul (waarvan de algemene formule r'cooo-))))))))))))). [2]
Algemene formule
De algemene formule van zuuranhydriden is (RC (O))2Of, die beter wordt waargenomen in het beeld dat aan het begin van dit artikel wordt geplaatst.
Voor azijnzuuranhydride (van azijnzuur) is de algemene formule bijvoorbeeld (ch3CO)2Of, op dezelfde manier schrijven voor veel andere soortgelijke zuuranhydriden.
Zoals hierboven vermeld, hebben deze verbindingen bijna dezelfde naam van hun voorloperzuren, en het enige dat verandert is de term zuur door anhydride, omdat dezelfde regels van nummering van atomen en substituenten moeten worden gevolgd om te slagen met hun nomenclatuur.
Toepassingen
Zure anhydriden hebben veel functies of toepassingen, afhankelijk van het veld dat wordt bestudeerd, omdat ze een hoge reactiviteit hebben, kunnen ze voorlopers zijn of deel uitmaken van veel belangrijke reacties.
Kan u van dienst zijn: pyrolyseEen voorbeeld hiervan is de industrie, waarbij azijnzuuranhydride in grote hoeveelheden wordt geproduceerd omdat het de eenvoudigste structuur is die kan worden geïsoleerd. Dit anhydride wordt gebruikt als een belangrijk organisch reagens, zoals acetaatesters.
Industrieel gebruik
Aan de andere kant wordt de anhydride maleico getoond met een cyclische structuur, die wordt gebruikt bij de productie van dekking voor industrieel gebruik en als een voorloper van sommige harsen door het copolymeterisatieproces met stretus -moleculen. Bovendien dient deze substantie als een Dienophile wanneer de Diels-Alder-reactie wordt uitgevoerd.
Evenzo zijn er verbindingen met twee zure anhydriden -moleculen in hun structuur, zoals ethystarbonylisch of dianhydride dianhydrid.
Daarnaast is er een gemengd anhydride genaamd 3'-fosfodenosín-5'-fosfosulfaat, van fosforische en zwavelzuren, die het meest voorkomende co-enzym vormen in biologische sulfaatoverdrachtsreacties.
Voorbeelden van zuuranhydriden
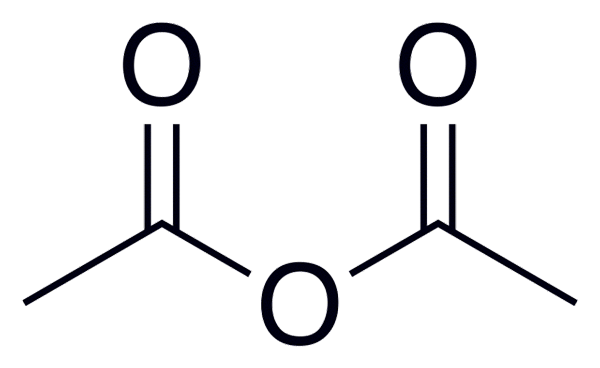 Azijnzuuranhydride
Azijnzuuranhydride Hieronder is een lijst met de namen van sommige zure anhydriden, om enkele voorbeelden te geven van deze belangrijke verbindingen in organische chemie die verbindingen van lineaire structuur of ringen van verschillende leden kunnen vormen:
- Azijnzuuranhydride.
- Propanoïsche anhydride.
- Benzoïsche anhydride.
- Maleïschanhydride.
- Succinisch anhydride.
- Fthalical anhydride.
- Naftalte -tracarbonylisch dianhydride.
- Ethytertarbony -dianhydride.
- Benzoquinonteterarbonbonbonbon.
Net zoals deze anhydriden met zuurstof worden gevormd, worden andere verbindingen gegeven waar een zwavelatoom zuurstof kan vervangen, zowel in de carbonylgroep als centrale zuurstof, zoals: bijvoorbeeld:
Kan u van dienst zijn: acetanylide (c8h9no)- Tioacetisch anhydride (kies3C (s)2OF)
Er is zelfs het geval van twee zure moleculen die banden vormen met hetzelfde zwavelatoom; Deze verbindingen worden genoemd Tioanhydrides, namelijk:
- Azijnzuur tioanhydride ((ch3CO))2S)
Referenties
- Wikipedia. (2017). Wikipedia. Opgehaald van.Wikipedia.borg
- Johnson, a. W. (1999). Uitnodiging voor organische chemie. Hersteld uit boeken.Google.co.gaan.
- Acton, Q. NAAR. (2011). Zuuranhydride Hydrolas: vooruitgang in onderzoek en toepassing. Hersteld uit boeken.Google.co.gaan
- Bruckner, r., En harmata, m. (2010). Organische mechanismen: reacties, stereochemie en synthese. Hersteld uit boeken.Google.co.gaan
- Kim, J. H., Gibb, h. J., en iannucci, aan. (2009). Cycliezuuranhydriden: aspecten van de menselijke gezondheid. Hersteld uit boeken.Google.co.gaan

