Amfoters die zijn, typen en voorbeelden
- 2105
- 367
- Nathan Wiegand
De Amfosters Het zijn de verbindingen of ionen die de eigenaardigheid hebben om zich te kunnen gedragen als een zuur of als basis, volgens de Bronsted en Lowry -theorie. Zijn naam komt van het Griekse woord Amfoteroi, wat "beide" betekent.
Veel metalen vormen amfoteros -oxiden of hydroxiden, waaronder koper, zink, tin, lood, aluminium en beryllium. Het amfoter kenmerk van deze oxiden hangt af van de oxidatietoestanden van het oxide in kwestie. Aan het einde van de artikelvoorbeelden van deze stoffen zijn opgenomen.

Metaaloxiden die kunnen reageren met zuren en basen om zouten en water te produceren, staan bekend als amfoteros -oxiden. Lood- en zinkoxiden zijn zeer goede voorbeelden, onder andere verbindingen.
[TOC]
Wat zijn de amfoter?
Volgens de theorie van Bronsted en Lowry zijn zuren die stoffen die protonen doneren, terwijl de basen die zijn die de protonen accepteren of nemen.
Een molecuul genaamd amfotaat zal reacties hebben waarin het protonen verwerft, omdat het ook de mogelijkheid zal hebben om ze te doneren (hoewel het niet altijd zo is, zoals in de volgende sectie zal worden gezien).
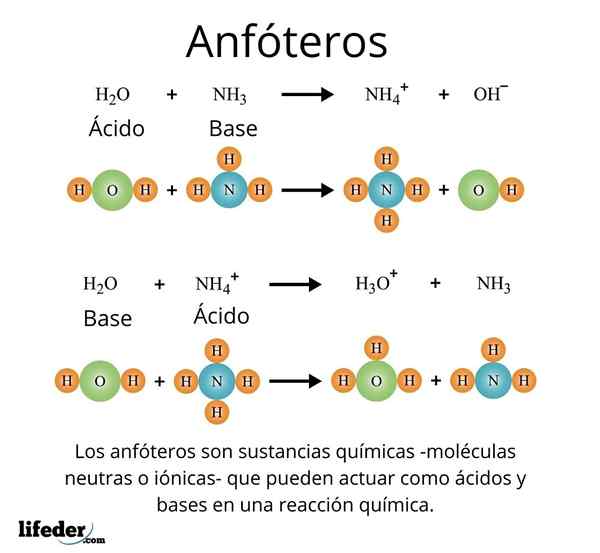
Een belangrijk en goed beoordeeld geval is dat van het universele oplosmiddel, water (h₂o). Deze stof reageert gemakkelijk met zuren, bijvoorbeeld in reactie met zoutzuur:
H2O + HCl → H3OF+ + Klet-
Maar op zijn beurt heeft hij ook geen problemen met een basis, zoals in het geval van ammoniak:
H2O + NH3 → NH4 + Oh-
Met deze voorbeelden kan worden waargenomen dat water volledig werkt als een amfotaatsubstantie.
Soorten amfoters
Hoewel amfotente stoffen moleculen of ionen kunnen zijn, zijn er moleculen die het beste de amfotente -eigenschappen aantonen en helpen om dit gedrag beter te bestuderen: amfrofrofotische stoffen. Dit zijn moleculen die specifiek een proton kunnen doneren of accepteren om als zuur of base te fungeren.
Kan u van dienst zijn: Rodio: Geschiedenis, eigenschappen, structuur, gebruik, risicoHet moet worden verduidelijkt dat alle amfotische stoffen amfotisch zijn, maar niet alle amfoters zijn amfiprtisch; Er zijn amfotoro's die geen protonen hebben, maar ze kunnen zich op andere manieren als zuren of basen gedragen (zoals de theorie van Lewis).
Onder de amfiprtische stoffen zijn water, aminozuren en bicarbonaat- en sulfaationen. Op zijn beurt worden amfrofotische stoffen ook gesubclassificeerd volgens hun vermogen om protonen te doneren of op te leveren:
Protogene of amfiprytische zuurstoffen
Zijn degenen die een grotere neiging hebben om een proton te geven dan er een te accepteren. Onder deze zijn zwavelzuur (h2SW4) en azijnzuur (cho3Onder andere COOH).
Basic protofiele of amfotische stoffen
Zij zijn die om een proton te accepteren vaker voorkomend dan het opleveren. Onder deze stoffen kunt u ammoniak vinden (NH3) en ethylendiamide [c2H4(NH2))2].
Neutrale stoffen
Ze hebben hetzelfde gemak of vermogen om een proton te accepteren om het op te geven. Onder deze zijn water (h2O) en kleine alcoholen (-roh), vooral.
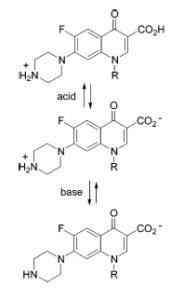 Ampotero -karakter van chinolonen
Ampotero -karakter van chinolonen Voorbeelden van amfotente stoffen
 Amphotero -spanning
Amphotero -spanning Nu hebt u de amfotent -stoffen al beschreven, het is noodzakelijk om de voorbeelden aan te geven van reacties waarin deze kenmerken worden gepresenteerd.
Het ion van carbonzuur presenteert een basisgeval van een amfiprtische stof; Dan worden hun reacties weergegeven wanneer het als een zuur werkt:
HCO3- + Oh- → CO32- + H2OF
De volgende reactie treedt op wanneer deze als basis werkt:
HCO3- + H3OF+ → h2CO3
Er zijn ook veel andere stoffen. Hiervan zijn de volgende voorbeelden:
Amfoteros oxiden
Zinkoxide, zoals reeds vermeld, is een amfotero maar geen amfiprtische stof. Vervolgens wordt aangetoond waarom.
Kan u van dienst zijn: Justus von LiebigGedragen als zuur:
ZnO + H2SW4 → ZnSo4 + H2OF
Gedragen als basis:
ZnO + 2naOH + H2O → NA2[Zn (OH)4]
Loodoxide (PBO), aluminium (AL2OF3) en tin (SNO) hebben ook hun eigen amfotent -kenmerken:
Gedragen als zuren:
PBO + 2HCL → PBCL2 + H2OF
Naar de2OF3 + 6hcl → 2alcl3 + 3H2OF
Sno + hcl ↔ sncl + h2OF
En als bases:
PBO + 2NAOH + H2O → NA2[PB (OH)4]
Naar de2OF3 + 2naOH + 3H2O → 2NA [AL (OH)4]
Sno + 4NaOH + H2Of ↔ na4[Sn (oh)6]
Er zijn ook amfoteros -oxiden uit de Gallië, de Indiaan, de schandio, het titanium, het circonium, het vanadium, het chroom, het ijzer, de kobalt, het koper, het zilver, het goud, de Germanio, de antimoon, de bismuth, de bismuth, de bismuth, de bismuth, de bismuth, de bismuth, de bismuth, de bismuth. en de Telurio.
Anfoter hydroxiden
Hydroxiden kunnen ook amfotent -kenmerken presenteren, zoals in gevallen van aluminiumhydroxide en beryllium. Beide voorbeelden worden hieronder waargenomen:
Aluminiumhydroxide als zuur:
AL (oh)3 + 3hcl → alcl3 + 3H2OF
Aluminiumhydroxide als basis:
AL (oh)3 + NaOH → Na [AL (OH)4]
Berylliumhydroxide als zuur:
Be (oh)2 + 2HCl → BECL2 + H2OF
Berylliumhydroxide als basis:
Be (oh)2 + 2naOH → NA2[Be (oh)4]
Verschillen tussen amfotero's, amfiprtische, amfolieten en apratici
Het is noodzakelijk om te weten hoe het concept van elke term te onderscheiden, omdat de gelijkenis ervan verwarrend kan worden.
Het is bekend dat amfotoro's stoffen zijn die zich als zuren of basen gedragen in een reactie die een zout en water produceert. Ze kunnen dit doen voor donatie of vastleggen van een proton, of gewoon door een elektronisch koppel te accepteren (of het te geven) volgens de theorie van Lewis.
Aan de andere kant zijn amfotische stoffen die amfoters die werken als zuren of basen met de donatie of verzameling van een proton, volgens de wet van Bronsted-Lowry. Alle amfotische stoffen zijn amfotisch.
Kan u van dienst zijn: benzoine: structuur, eigenschappen, gebruik en risico'sAmpolitische verbindingen zijn amfotente moleculen die bestaan als zwitterions en hebben dipoolionen in bepaalde ph -pH. Ze worden gebruikt als dempende middelen in bufferoplossingen.
Ten slotte zijn de squeeze -oplosmiddelen degenen die geen protonen hebben om toe te geven en ze ook niet kunnen accepteren.
Referenties
- Amfoterisch. (2008). Wikipedia. Verkregen van in.Wikipedia.borg
- Anne Marie Helmestine, p. (2017). Wat betekent amfoterisch in de chemie?. Verkregen van ThoughtCo.com
- Bicpuc. (2016). Amfoterische verbindingen. Verkregen van Medum.com
- Chemicool. (S.F.)). Definitie van amfoterisch. Verkregen van Chemicool.com.
- « Het meest populaire typische Colombia
- Keuze van het onderwerp van onderzoek Hoe, belang, voorbeelden worden gedaan »

