Alilo Alilic Unit, carbocatie, radicaal, voorbeelden

- 4036
- 694
- Kurt Aufderhar Jr.
Hij Alilo of 2-gevangenis is een organische groep of substituent wiens structurele formule cho is2= Ch-ch2-. Het bestaat uit een vinylfragment, ch2= CH- en een methyleengroep, -CH2-. Het bestaat uit een alkeniele groep, specifiek afgeleid van de propeno, cho2= Ch-ch3.
De term 'Alilo' is te wijten aan de botanische naam die wordt gebruikt om naar knoflook te verwijzen: Allium sativum, wiens oliën in 1892 het samengestelde dialil van disulfide werden geïsoleerd, h2C = CHCH2SSCH2CH = CH2, verantwoordelijk in een deel van zijn karakteristieke geuren. In feite zijn veel alilische verbindingen, dat wil zeggen degenen die de Alilo -groep hebben, te vinden in knoflook en groenten.
 Alilo Group
Alilo Group De bovenste afbeelding toont de skeletformule van de Alilo -groep. Voorbij de sinuositeiten aan de rechterkant hebben we de rest van het molecuul; Als dit alquilica is, wordt het weergegeven met het R -symbool.
Het is gemakkelijk om Alilo te herkennen omdat het veel lijkt op de vinylgroep. Alilo kan echter ook cyclisch zijn en onopgemerkt blijven in verbindingen zoals Cyclops.
Een voorbeeld van een allylische verbinding is bondgenoot alcohol, h2C = CHCH2Oh. Hydogenen van het vinylfragment kunnen worden vervangen en een Alilo blijven. Dus de 3-methyl-2-Bunt-1-ol, (Cho3))2C = CHCH2Oh, het is ook een bondgenootalcohol. Daarom is het bestaan van cyclische Alilos mogelijk.
[TOC]
Allyische eenheid en zijn onderdelen
Belangrijker dan de Alilo -groep, het is de Allyic -eenheid die hetzelfde is voor alle Allic -verbindingen. Dit is: C = C-C. Het einde C = C komt overeen met vinylcarbons. Alle atomen die aan deze twee koolstofatomen zijn gekoppeld, ontvangen ook de naam van vinylsubstituenten. Als ze bijvoorbeeld hydrogenen zijn, cho2= Ch, we praten over vinylhydrogenen.
Ondertussen komt de extreme C aan de andere kant overeen met de Allic Carbon. Alle atomen of groepen die aan deze koolstof zijn gekoppeld, worden allische substituenten genoemd. Daarom zijn Allyic -verbindingen precies iedereen die een functionele groep heeft (OH, S, F, COOH, enz.) Allyische koolstof gekoppeld.
Kan u van dienst zijn: natriumcitraat (C6H5O7NA3): structuur, gebruik, eigenschappenVinyl -koolstofatomen hebben SP -hybridisatie2, Dus ze zijn meer elektronegatief dan Allyic Carbon, Spo3. Dit elektronegativiteitsverschil verhoogt de zuurgraad van bondgenoothydrogenen, de vorming van bondgenoot Carbanion is waarschijnlijk. Maar winstgevender in termen van organische synthese, het is allylische carbocatie, die hieronder zal worden uitgelegd.
Carbocatie
Resonantiestructuren
 Allyic Carbocation Resonance Structures. Bron: oplossing/cc by-s (https: // creativeCommons.Org/licenties/by-sa/3.0)
Allyic Carbocation Resonance Structures. Bron: oplossing/cc by-s (https: // creativeCommons.Org/licenties/by-sa/3.0) In de bovenste afbeelding wordt bondgenootcarbocatie getoond. Merk op dat de positieve belasting, (+), eerst verschijnt op Allische koolstof. Onmiddellijk zullen de dubbele bindingselektronen worden aangetrokken tot deze belasting, zodat ze in de richting van het bondgenoot -koolstofatoom gaan bewegen.
Bijgevolg hebben we twee resonantiestructuren (links van de afbeelding). Nu bevindt de positieve belasting zich op een van de vinyl -koolstofatomen. Nogmaals, de elektronen van de dubbele binding van de Allic -zijde zullen opnieuw worden aangetrokken door de positieve belasting en zullen terugkeren naar hun initiële positie. Dit wordt steeds opnieuw herhaald, met onvoorstelbare snelheden.
Het resultaat: de positieve belasting, +1, wordt verplaatst of verspreid tussen de drie atomen van de Allic -eenheid; maar zich alleen concentreren op de twee koolstofatomen van de uiteinden. Aldus behoudt een van de vinyl -koolstofatomen een belasting van 1/2 +, terwijl Allyl Carbon blijft met de andere helft van de belasting, waardoor +1 wordt toegevoegd.
Een meer geschikte manier om bondgenootcarbocatie weer te geven, is via de resonantiehybride (recht van de afbeelding). Aldus wordt waargenomen dat de positieve belasting over de allicale eenheid wordt verdeeld.
Het kan u van dienst zijn: aluminiumchloride (ALCL3)Stabiliteit en verdeling van positieve belasting
De democatie van de positieve belasting geeft stabiliteit bondgenootcarbocatie. Het is zozeer dat het wordt gelijkgesteld met een secundaire carbocatie in termen van stabiliteit.
In de afbeelding, omdat het alleen de alllic -eenheid is, wordt aangenomen dat de verdeling van de positieve belasting gelijkwaardig is aan beide koolstofatomen (+1/2 voor elk). Maar dit wordt niet vervuld voor alle Allic -verbindingen. Er zullen dus min of meer positieve carbocaties zijn; wat betekent dat ze min of meer reactief zullen zijn.
Overweeg bijvoorbeeld het Alilo -kation:
H2C = ch-ch2+ ↔ H2C+-CH = CH2
De twee resonantiestructuren zijn gelijk door de positieve belasting te verdelen. Het gebeurt echter niet hetzelfde met het kation 1.1-dimethylil:
H2C = CH-C+(Ch3))2 ↔ H2C+-CH = C (Ch3))2
In de structuur van links wordt de positieve belasting meer gestabiliseerd door de aanwezigheid van de twee methylgroepen, die een deel van hun negatieve bondgenoot -koolstofdichtheden doneren.
Ondertussen dragen vinylhydrogenen niets bij aan de positieve belasting op vinyl -koolstof. Daarom zal de structuur van links meer bijdragen aan de resonantiehybride van dit bondgenootkation.
Het is cruciaal om in gedachten te houden dat het resonantie hybriden zijn die het dichtst bij de echte toestand van deze carbocaties staan, en niet hun structuren afzonderlijk.
Radicaal
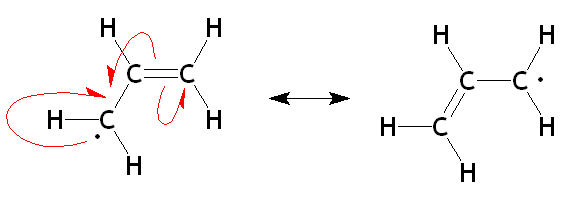 Alilo radicale resonantiestructuren. Bron: organaute/cc by-sa (https: // creativeCommons.Org/licenties/by-sa/3.0)
Alilo radicale resonantiestructuren. Bron: organaute/cc by-sa (https: // creativeCommons.Org/licenties/by-sa/3.0) In het bovenste beeld worden nu de twee resonantiestructuren van de bondgenootradicaal in de respectieve allylische eenheid getoond. Merk op dat de aard van zijn ontwikkeling hetzelfde is als voor carbocatie: het verdwenen elektron (·) wordt gedemocaliseerd tussen de twee koolstofatomen van de uiteinden. Daarom heeft elk "elektronmedium" (1/2 ·).
Kan u van dienst zijn: kation: training, verschillen met anion en voorbeeldenWat wordt uitgelegd voor carbocatie en radicale alilische ones is ook van toepassing op zijn respectieve carbanion, waar elk van de twee genoemde koolstofatomen een half negatieve belasting zal hebben (-1/2).
Voorbeelden van alilische verbindingen
Ze zullen worden vermeld om verschillende voorbeelden van alilische verbindingen te voltooien. In elk van hen zal de Allic -eenheid aanwezig zijn:
-Alilo chloride, h2C = ch-ch2-Klet
-Bondgenoot methylsulfide, h2C = ch-ch2-S-CH3 (Een andere verbindingen die verantwoordelijk zijn voor de geur van knoflook)
-Alicina, h2C = ch-ch2-S (O) -S -CH2-CH = CH2
-Crotilische alcohol, cho3CH = Ch --ch2Oh (merk op dat een van de vinylhydrogenen wordt vervangen door een methyl)
-Alilo Acetate, h2C = ch-ch2-Oc (o) ch3
-Alilo Bromide, h2C = ch-ch2-BR
-Alilamina, h2C = ch-ch2-NH2 (Basiseenheid voor complexere alilamines die worden gebruikt als anti -fungiciden)
-Dimethylalil pyrofosfaat, (ch3))2C = ch-ch2-OPO2-O-po3
In het volgende paar alilamines, flunarizine en naftifine, beide met farmacologische effecten, kunnen we de Alilo -groep waarderen:
 Structurele formules van twee Alilamines. Bron: HBF878 / CC0.
Structurele formules van twee Alilamines. Bron: HBF878 / CC0. In beide is het aan de rechterkant: die dubbele binding die is ingediend tussen de piperazine -ringen (de zeshoekig met twee stikstofatomen) en de benzeen. Merk op dat het essentieel is om de Alilo te identificeren.
Referenties
- Morrison, r. T. en Boyd, R, n. (1987). Organische chemie. 5e editie. Redactionele addison-wesley inter-Amerikaan.
- Carey F. (2008). Organische chemie. (Zesde editie). MC Graw Hill.
- Graham Solomons T.W., Craig B. Friteuse. (2011). Organische chemie. (10e editie.)). Wiley Plus.
- Wikipedia. (2020). Allyl Group. Opgehaald uit: in.Wikipedia.borg
- Elsevier B.V. (2020). Allyl Compound. Wetenschappelijk. Opgehaald uit: Scientedirect.com
- Gamini Gunawardena. (5 juni 2019). Allylische koolstof. Chemistry Libhethexts. Hersteld van: chem.Librhetxts.borg
- « Historische kostenkenmerken, voor-, nadelen, voorbeelden
- Cross Referenties Concept, functies, voorbeelden »

