Uretano -structuur, eigenschappen, het verkrijgen, gebruiken
- 4259
- 64
- Aaron Okuneva
Hij Uretano Het is een organische chemie -term die normaal wordt gebruikt om naar te verwijzen Ethylcarbamaat, of naar de functionele groep Carbamate. Daarom wordt ethylcarbamaat meestal beschouwd als standaard urethaan, dat een zeer oplosbare verbinding in water is, gebruikt als een oplosmiddel in organische synthesereacties.
Ethylcarbamaat wordt ook gebruikt als pesticide en fungicide. Tot 1943 was het als antineoplastisch gebruikt. Maar bij het ontdekken van de carcinogene werking bij experimentdieren werd deze toepassing weggegooid.
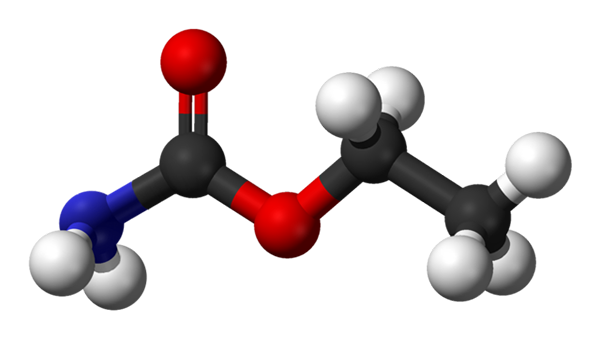
 Weergave met bollen en staven van de ethyl- of urethaancarbamaatmolecuul. Bron: Kemikungen / Public Domain
Weergave met bollen en staven van de ethyl- of urethaancarbamaatmolecuul. Bron: Kemikungen / Public Domain Het urethaan wordt industrieel geproduceerd door de hete reactie van ureum met ethanol. Het is een vluchtige en ontvlambare verbinding die een stoomdichtheid presenteert die drie keer hoger is dan de lucht. Bovendien ervaart de urethaan sublimatie.
Het polyurethaan daarentegen is een polymeer waarvan de industriële productie is gericht op het verkrijgen van schuimen, gebruikt in meubels en als isolatoren in koelkasten. Ondanks zijn naam is polyurethaan op zichzelf geen polymeer van Uretan, maar wordt ze gevormd door verschillende organische eenheden.
Uretano, in de vorm van carbamaat (h2Ncoo-), het dient alleen als een vakbondsbrug tussen de chemische eenheden die het polyurethaan vormen.
[TOC]
Urretan structuur
In het eerste beeld hebben we de moleculaire structuur van het urethaan. Aan de linkerkant hebben we de carbamato -groep: r2Ncoo-, met zijn alkylgroepen R vervangen door H, en het segment gekookt tot de ethylsubstituent. Zoals te zien is, is het een eenvoudig molecuul, dat niet alleen veel polymerisatie -opties biedt.
Urethaaneigenschappen
Namen
-Uretano
-Ethylcarbamaat (IUPAC -naam)
Kan u van dienst zijn: deuterium-Ethylster van carbaminezuur
-Ethyluretan
Chemische formule
C3H7NEE2 of NH2COOC2H5
Molaire massa
89.094 g/mol
Fysiek uiterlijk
Witte of kleurloze kristallen. Wit korrelige natuurpoeder.
Smaak
Verfrissende zoutoplossing
Geur
Toilet
Dikte
1.056 g/cm3
Smeltpunt
46 tot 50 ºC
Kookpunt
182 tot 185 ºC
Oplosbaarheid in water
4.8 · 105 mg/l A 15º C. Het is erg oplosbaar, omdat het een nogal polaire moleculaire is.
Oplosbaarheid in andere oplosmiddelen
1 gram uretano wordt afzonderlijk opgelost in: 0.8 ml alcohol, 1.5 ml ether, 0.9 ml chloroform, 2.5 ml glycerol en 32 ml olijfolie.
Dampdichtheid
3.07 in de luchtrelatie als eenheid.
Dampdruk
3 PA A 20 ºC.
Octanol/waterpartitiecoëfficiënt
Log p = - 0,15
ontstekingspunt
92 ºC
Brekingsindex
1.4144 tot 51 ºC
Sublimatie
Sublimeert snel bij een temperatuur van 103 ºC en bij een druk van 54 mm Hg.
Reactiviteitsprofiel
Het urethaan is onverenigbaar met alkalis, zuren, koraalhydraten, kamfer, mentol en timol. Het is ook onverenigbaar met antipirine en salol. Reageert met fosfor pentachloride om een explosief te produceren.
Het verkrijgen van
Synthese
Het urethaan wordt geproduceerd door de reactie, heet, van ureum met ethylalcohol:
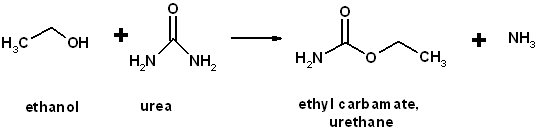 Vergelijking voor de reactie tussen ethanol en ureum. Bron: Geen machine-leesbare auteur verstrekt. Oldsci verondersteld (op basis van claims op het auteursrecht). / Publiek domein
Vergelijking voor de reactie tussen ethanol en ureum. Bron: Geen machine-leesbare auteur verstrekt. Oldsci verondersteld (op basis van claims op het auteursrecht). / Publiek domein Uretano wordt ook geproduceerd door de reactie van ethylchloroformat met ammoniak.
Aanwezigheid in gefermenteerde drankjes en voedsel
De Uetano aanwezig in sommige gefermenteerde dranken komt van de reactie van het ureum, afkomstig van het metabolisme van het arginine -aminozuur en vrijgegeven door gisten, met ethylalcohol. Vervolgens is de Uretano een lateraal product van de gisting van de glucosegisten die in de vruchten aanwezig zijn.
Kan u van dienst zijn: koolstofhybridisatie: concept, typen en hun kenmerkenDe urethaanproductiereactie in alcoholische dranken is spontaan, hoewel de vorming ervan wordt begunstigd door de aanwezigheid van een licht met een golflengte tussen 375 en 475 nm.
Alcoholische drankenproducenten bepalen de aanwezigheid van Uretan.
Toxiciteit
Naast het aangetoond worden van de carcinogene werking van het urethaan in experimentendieren, was het mogelijk om talloze toxische effecten op mensen te benadrukken. Het is schadelijk door inademing, huidabsorptie of inname.
Het urethaan produceert enthousiasme van de keel, waterige of bloeddiarree, buikpijn, verminderde vorming en uitscheiding van urine, bloeddruk, cardiovasculaire instorting, delirium, aanvallen, spierzwakte met respiratoire insufficiëntie en uiteindelijk depressie van het zenuwstelsel en het beengrouw.
Toepassingen
Geneesmiddel
Eerder werd de Uretan gebruikt bij de behandeling van sommige soorten kankers, vooral die van chronische leukemie en multipel myeloom. In 1943 werd bewijsmateriaal verkregen dat de Uretano integendeel een carcinogene actie had, dus dit gebruik werd weggegooid.
Het werd ook gebruikt als analgetic, een applicatie die ook werd verlaten. In Japan werd het gebruik echter tot 1975 geplaatst om postoperatieve pijn te verlichten.
Uretano wordt momenteel gebruikt als anesthetica bij dieren die worden gebruikt bij experimentele activiteiten, in sommige gevallen een anesthetische actie die zich meer dan 24 uur uitstrekt.
Het urethaan was onderdeel, samen met de sulfonamide, van een sclereuze oplossing die werd gebruikt bij de behandeling van spataderen.
Kan u van dienst zijn: chemische bindingPolyurethanen
 Een van de toepassingen van polyurethanen is om als materiaal te dienen voor de skate wielen. Bron: aqazi111/cc by-sa (https: // creativeCommons.Org/licenties/by-sa/3.0)
Een van de toepassingen van polyurethanen is om als materiaal te dienen voor de skate wielen. Bron: aqazi111/cc by-sa (https: // creativeCommons.Org/licenties/by-sa/3.0) Polyurethanen zijn polymeren die zoals gebruikelijke monomeren de diol en diisocianaat hebben. Dat wil zeggen, het polyurethaan is geen polymeer van het urethaan (ethylcarbamaat), maar van een andere chemische verbinding aangeduid als urethaan: carbamaat (h2Ncoo-), die dient als een verband tussen de chemische eenheden die het polyurethaan vormen.
Ze worden gebruikt als schuim bij de vervaardiging van druk aanpasbare stoelen, in isolatiepanelen van koelapparatuur in stijve schuim, zoals afdichtingen en microcellulaire schuimverbindingen.
Ze worden ook gebruikt bij de productie van grote wielen en banden, gebruikt op mechanische trappen, winkelwagentjes in supermarkten, skate wielen. Bovendien worden polyurethanen gebruikt bij de productie van ophangbussen voor auto's.
Ze worden gebruikt in verbindingen om elektrische materialen te bedekken, in oppervlakte -coatings en afdichtingsmiddelen, als basis voor het plaatsen van tapijt, en als harde plastic stukken. Ze worden ook gebruikt bij de uitwerking van kledingonderdelen, zoals de coating van de beha's.
Anderen
Uretano wordt gebruikt bij de productie van aminorresins. Deze worden gebruikt als lijmstoffen bij de vervaardiging van hout en aanrechtvormige agglomeraten, gebruikt bij de bouw van woningen en meubelproductie.
Uretano wordt gebruikt als oplosmiddel in organische synthesereacties. Het wordt ook gebruikt als een fungicide en pesticide, evenals in de textielindustrie voor de ontwikkeling van producten die betrokken zijn bij permanente dringen.
Referenties
- Graham Solomons T.W., Craig B. Friteuse. (2011). Organische chemie. (10e Editie.)). Wiley Plus.
- Carey F. (2008). Organische chemie. (Zesde editie). MC Graw Hill.
- Morrison en Boyd. (1987). Organische chemie. (Vijfde editie). Addison-Wesley IberoAmericana.
- Wikipedia. (2020). Lijst met polyurethaantoepassingen. Opgehaald uit: in.Wikipedia.borg
- Meg Michelle. (24 april 2017). Wat is uretane? Hersteld van: wetenschap.com
- Polymer Science Learning Center. (2020). Polyurehane maken. Hersteld van: PSLC.WS

